Мартов А.Г., Круглов В.А., Асфандияров Ф.Р., Выборнов С.В., Ольховская С.А., Круглова Е.Ю.
Мочекаменная болезнь (МКБ) — одно из частых заболеваний, которое занимает ведущее место в структуре урологической патологии. Пациенты с МКБ составляют 30–40% всего контингента урологических стационаров [1].
В последние десятилетия в лечении мочекаменной болезни произошли значительные изменения, связанные с внедрением в широкую урологическую практику высокоточных методов диагностики заболевания и малоинвазивных методов удаления мочевых камней, однако это не снизило актуальности проблемы уролитиаза [2]. Практически во всех странах мира, в том числе и в России, констатируется тенденция к росту заболеваемости, что связывают с произошедшими изменениями в характере и качестве питания людей, увеличением числа неблагоприятных экологических и социальных факторов, оказывающих как прямое, так и опосредованное действие на организм человека [3-9]. Ряд авторов отмечают единство некоторых звеньев патогенеза МКБ с такими социально значимыми заболеваниями как сахарный диабет, ожирение, метаболический синдром и артериальная гипертензия [10,11]. При этом наибольший процент пациентов с МКБ – это люди молодого и среднего возраста от 20 до 45 лет, то есть наиболее трудоспособные и социально активные [4,12-13].
В настоящее время основными методами удаления мочевых камней почек и мочеточников можно считать трансуретральную нефро и уретеролитотрипсию, перкутанную нефролитотрипсию и дистанционную литотрипсию (ДЛТ) [1]. Однако хорошо известно, что при использовании этих методов или их сочетания, далеко не во всех случаях непосредственно интраоперационно удается добиться так называемого «состояния полного освобождения от камней» («stone free rate» – SFR) [1,14].
Поэтому ведущей проблемой послеоперационного периода часто становится возможность самостоятельного отхождения фрагментов конкремента. Эта возможность определяется множеством трудно учитываемых в своей совокупности факторов. К таковым можно отнести количество, размер, локализацию, структурную плотность, химический состав и длительность нахождения камня, длину шеек чашечек, чашечно-лоханочный угол, степень нарушения уродинамики и проходимость верхних мочевыводящих путей, степень воспалительных изменений в мочевой системе, а также ряд иных факторов [1,15-16].
Другой, более отсроченной, проблемой лечения МКБ является рецидивное камнеобразование. Риск рецидива на протяжении всей жизни составляет в среднем 5–15%, а в течение 10 лет после самостоятельного отхождения или оперативного вмешательства частота повторного образования конкремента достигает 30-40% [1,17]. Таким образом, как бы эффективно не была проведена операция по удалению камня, без последующей комплексной и индивидуально подобранной метафилактики конечный результат лечения будет неудовлетворительным [1,4,18].
Традиционно на разных этапах лечения пациентов с МКБ важная роль отводится фитопрепаратам [19-21].
Лекарственные растения использовались для лечения всеми народами мира независимо от времени и места их обитания. В России препараты растительного происхождения составляют приблизительно 40% от общего количества используемых в практической медицине лекарств. Каждый третий лечебный препарат на мировом рынке – растительного происхождения. В США, где традиционно принято использовать синтетические препараты, более 26% лекарств содержат лекарственные растения. Гораздо шире они используются в Европейских странах, а в странах юго-восточной Азии (Индия, Китай, Пакистан и др.) растительные препараты имеют большее значение, чем синтетические лекарства [22].
В специальной литературе применение фитопрепаратов обосновано и для целей предоперационной подготовки, и в послеоперационном периоде, а также для длительной профилактики и метафилактики мочекаменной болезни, что во многом определяет результаты лечения в долгосрочной перспективе [1,19-20,23].
Существенной особенностью метафилактики МКБ является необходимость проведения длительных курсов терапии [24]. Для многих синтетических препаратов это невозможно в связи с усиливающимся проявлением их побочных эффектов при удлинении сроков применения. Хотя препараты из растений так же имеют нежелательные эффекты, выраженность их проявлений гораздо меньше и в связи с этим фитотерапия при уролитиазе во многом более предпочтительна [5,25]. Ценность фитопрепаратов в урологии также заключается в широте терапевтического действия растительных компонентов. Для них характерны антимикробный, противовоспалительный, антиоксидантный, спазмолитическом и обезболивающий, мочегонный, литолитический, литокинетический и другие эффекты [19-20,26].
В настоящее время уверенно идентифицированы основные классы биологически активных веществ (БАВ) растительного происхождения, с которыми ассоциируются вышеназванные эффекты. Среди таковых наибольшее практическое значение имеют алкалоиды, терпены – группа, включающая эфирные масла, полифенольные соединения, среди которых наиболее многочисленными и значимыми являются флавоноиды – мощные регуляторы ферментной активности, витамины и минеральные вещества [27].
Целью данного проспективного исследования было изучение клинической эффективности и безопасности применения комплекса растительных экстрактов в лечении пациентов с резидуальными камнями почек и мочеточников после выполненной литотрипсии.
Таблица 1. Состав активных компонентов Нерей
| Растительное сырье | мг/капсулу |
|---|---|
| Сухой экстракт листьев брусники обыкновенной | 70 |
| Сухой экстракт корня петрушки | 60 |
| Сухой экстракт листьев березы повислой | 60 |
| Сухой экстракт створок фасоли обыкновенной | 40 |
| Сухой экстракт травы горянки | 10 |
| Сухой экстракт цветков ромашки аптечной | 10 |
| Сухой экстракт плодов бузины черной | 6 |
МАТЕРИАЛЫ И МЕТОДЫ
Для проведения исследования в клинической практике нами был выбран фитокомплекс «Нерей».
«Нерей» (ООО «КоролёвФарм») – новое оригинальное комбинированное растительное средство на отечественном рынке лечения и профилактики мочекаменной болезни. В его состав входят створки фасоли обыкновенной (Faseolus vulgaris), сухие экстракты листьев березы плосколистной (Betula platyphylla), корня петрушки кудрявой (Petroselinum crispum), листьев брусники обыкновенной (Vaccinium vitisidaea), травы ромашки лекарственной (Matricaria chamomilla), травы сухой горянки (Epimedium grandiflorum) травы и плодов бузины черной (Sambucus nigra) (таблица 1).
Исходя из заявленного производителем состава лекарственного сырья, можно предполагать высокое содержание флавоноидов, эфирных масел, арбутина и, соответственно, выраженный диуретический, литокинетический, противовоспалительный и антибактериальный эффекты.
Мочегонное и литокинетическое действие препарата обусловлено комплексным эффектом эфирных масел и флавоноидов, которые с одной стороны вызывают вазодилятацию и улучшение кровоснабжение почечного эпителия, уменьшение реабсорбции клетками почечных канальцев солей натрия и воды, а с другой – снижают тонус гладких мышц, устраняя болевые ощущения и способствуя продвижению конкремента по мочевым путям.
Противовоспалительная активность флавоноидов связана с воздействием на различные звенья цепи воспалительной реакции и реализуется за счет ингибирования индукции тканевых медиаторов воспаления – цитокинов и метаболитов арахидоновой кислоты [27]. Также описано подавление флавоноидами активности бактериальной гиалуронидазы. Однако в большей степени антибактериальный эффект фитокомплекса связан с присутствием в составе листьев брусники обыкновенной, содержащей большое количество арбутина. Арбутин – хорошо изученный гликозид фенольного типа, представляет собой один из наиболее мощных природных антисептиков. Известно, что в процессе гидролиза арбутин трансформируется в гидрохинон, который выводится с мочой и обеспечивает выраженное антимикробное действие в мочевыводящих путях.
В исследование были включены 94 пациента, проходивших лечение в урологической клинике ФГБОУ ВО «Астраханский государственный медицинский университет» на базе ГБУЗ АО «АлександроМариинская областная клиническая больница» с мая 2018 г по январь 2019 г., у которых после выполнения различных вариантов литотрипсии были диагностированы резидуальные камни почек и мочеточников.
Среди пациентов было 50 мужчин, средний возраст которых составил 42,9±17,4 года и 44 женщины – средний возраст 40,5±18,4 года.
При поступлении в стационар для установления диагноза и определения тактики лечения все пациенты подвергались клиническим, лабораторным, ультразвуковым, рентгенологическим и инструментальным методам исследования. Данные обследования включали выяснение жалоб больных, сбор анамнеза заболевания и жизни и результаты физикального исследования. Лабораторная диагностика включала клинический анализ крови и мочи, биохимический анализ крови с определением содержания мочевины, креатинина, электролитов, а также бактериологическое исследование мочи с определением чувствительности микроорганизмов к антибактериальным препаратам. Проводилось ультразвуковое исследование органов мочевыделительной системы, обзорная урография, компьютерная томография (КТ), выделительная урография при отсутствии противопоказаний. Оценку частоты и интенсивности болевого синдрома при почечной колике и ее субъективную оценку осуществляли с помощью 10-балльной числовой рейтинговой шкалы для боли (Numeric rating Scale for pain, NRS).
Фрагменты камня, полученные при оперативном лечении или самостоятельном отхождении, подвергали анализу с целью идентификации его минерального состава.
Критериями исключения являлись беременность и лактация, анурия, гнойный обструктивный пиелонефрит, отсутствие резидуальных камней после выполненного оперативного пособия.
Больным были выполнены следующие виды литотрипсии:
- 18 пациентов (19,3%) имели камни почек более 1 см в диаметре или коралловидные камни, им была выполнена перкутанная нефролитотрипсия, нефростомия.
- 20 пациентов (21,5%) имели камни почек менее 1 см в диаметре, и в этом случае выполнялась ДЛТ почки под рентгеновским или ультразвуковым наведением.
- у 56 пациентов (59,2%) были диагностированы камни мочеточника. С учетом локализации конкрементов в мочеточнике, их рентгненопозитивности, плотности и размеров принималось решение о выборе оперативной тактики. 40 пациентам этой группы была выполнена трансуретральная уретеролитотрипсия, 16 – ДЛТ камней мочеточника (рис. 1).
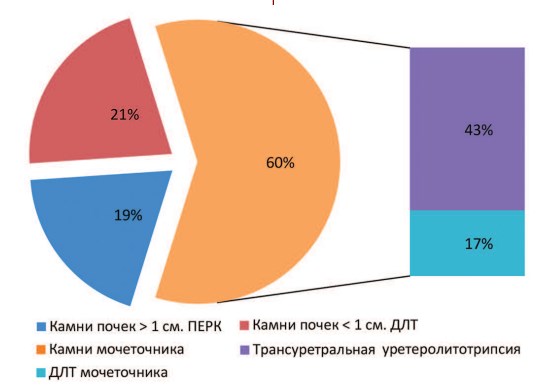
Рис. 1. Формы мочекаменной болезни и выполненные оперативные пособия
Лейкоцитурия в ОАМ была выявлена у 83,9% пациентов, бактериурия в диагностически значимом титре (105 КОЕ/мл для кишечной палочки) – у 48,4 % пациентов, они получали противовоспалительную антибактериальную терапию в соответствии с данными посева мочи и определения чувствительности к антибиотикам.
Пациенты, включенные в исследование, были разделены на две равные группы, симметричные по основным клинико-диагностическим характеристикам. Пациентам первой (основной) группы выполнялись оперативные пособия, проводилась традиционная патогенетическая, симптоматическая терапия и назначался фитокомплекс Нерей по 1 капсуле (400 мг) 2 раза в день с момента установления диагноза и в течение всего времени нахождения в стационаре. Пациентам второй (контрольной) группы Нерей не назначался.
динамике оценивались результаты комплексного лечения пациентов обеих групп по следующим критериям:
- субъективное состояние пациента, частота возникновения почечных колик, степень выраженности болевого синдрома при отхождении камней;
- динамика изменений в общеклиническом анализе крови и мочи (степень лейкоцитурии, кислотность мочи, концентрация и тип минеральных солей) и при микробиологическом исследовании мочи (степень бактериурии);
- количество пособий ДЛТ и количества импульсов в каждом из сеансов дробления;
- сроки освобождения мочевых путей от фрагментов после оперативного лечения;
- данные ультразвукового, рентгенологического и КТ контроля состояния мочевых путей.
Статистическая обработка полученных данных проводилась по методу Стьюдента, различия в показателях считали достоверными при p<0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
После выполненных оперативных вмешательств у пациентов, включенных в исследование, размер резидуальных камней варьировал от 0,2 до 1,0 см. Крупные фрагменты конкрементов (более 0,5 см) были подвергнуты в дальнейшем повторной дистанционной литотрипсии или трансуретральной уретеролитотрипсии. Пациенты с более мелкими фрагментами получали консервативную терапию.
Частота почечных колик и степень выраженности болевого синдрома оценивалась во время беседы врача с пациентом при помощи рейтинговой шкалы для боли (от 0 до 10 баллов). Так, среди пациентов первой группы частота почечных колик составила 40% наблюдений; пациенты отмечали, как правило, однократные почечные колики, легко купирующиеся применением спазмолитических препаратов, в то время как в контрольной группе колики возникали в 93% наблюдений, при этом они имели рецидивирующий характер (рис. 1). Выраженность болевого синдрома по 10 балльной шкале составила 5,01±1,9 в первой группе и 7,78±2,1 во второй группе.
Таким образом, частота почечных колик и их выраженность была меньше у пациентов, принимающих Нерей. Включение данного препарата в комплекс терапии позволяет уменьшить потребность в применении спазмолитических и обезболивающих лекарств, положительно сказывается на субъективных ощущениях пациентов в послеоперационном периоде.
На фоне приема фитокомплекса отхождение мелких фрагментов камней как по нефростоме, так и при самостоятельном мочеиспускании, было отмечено в 74,6% случаев, в контрольной группе – лишь в 37,6% наблюдений. При этом наибольшая эффективность была отмечена в группе пациентов с камнями и «каменными дорожками» нижней трети мочеточника, и достигала 86,2% в первой группе, против 50,6% – в контрольной. Сроки отхождения фрагментов конкрементов были на 49,8% меньше в основной группе. Полное освобождение от камней достигнуто в 70,2% наблюдений в 1 группе, в 24,7% – в контрольной (рис. 2).
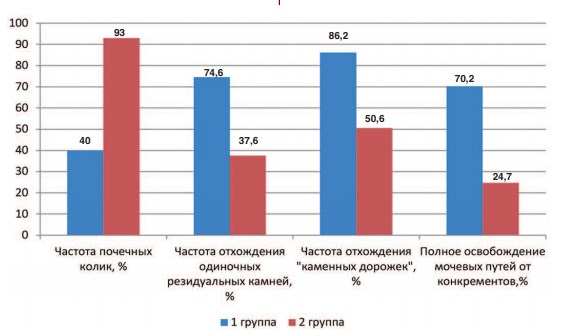
Рис. 2. Результаты применения фитокомплекса Нерей. Спазмолитический и литокинетический эффекты
Эффективность ДЛТ в обеих группах оценивалась с помощью количества пособий ДЛТ и количества импульсов в каждом из сеансов дробления. Так, среднее количество импульсов, потребовавшихся для дезинтеграции камня в первой группе больных, где назначали Нерей, составило 2050±150, в то время как пациентам второй группы было необходимо в среднем на 610±105 импульсов больше, чем в 1-й группе, причем разница имела достоверный характер. При этом на каждого больного пришлось 1,9 сеанса ДЛТ, из них пациентам первой группы, получавшим фитокомплекс Нерей, — в среднем 1,2 вмешательства, а в контрольной группе этот показатель составил 1,8.
Риск развития острого пиелонефрита после дистанционного или контактного дробления камня связан не только с возможной обструкцией мочеточника его фрагментами, но и с выходом микроорганизмов из внутренних слоев разрушенного конкремента в просвет мочевыводящих путей. Поэтому мы изучали влияние фитокомплекса на степень лейкоцитурии и бактериурии. При контрольном лабораторном обследовании было выявлено, что Нерей не оказывает выраженного эффекта на результат посева мочи. Однако в общем анализе мочи отмечалось достоверное (р<0,05) снижение лейкоцитурии и увеличение количества солей (уратов, фосфатов, оксалатов).
В биохимическом анализе крови и мочи не было выявлено достоверных изменений в показателях уровня азотистых шлаков и рН мочи. На фоне всего периода приема препарата пациенты отмечали увеличение диуреза (на 45,6% по сравнению с пациентами контрольной группы), отсутствие побочных эффектов лечения, непосредственно связанных с применением фитокомплекса Нерей.
Таким образом, на основании полученных результатов исследования, можно сделать следующие выводы:
- Применение фитокомплекса Нерей снижает частоту и интенсивность почечных колик у пациентов, имеющих резидуальные камни после выполненных оперативных вмешательств;
- Применение растительного комплекса Нерей способствует более быстрому отхождению мелкихкамней и «каменных дорожек», полному освобождению мочевых путей от фрагментов конкрементов;
- Применение фитокомплекса Нерей на фоне антибактериальной терапии способствует снижению лейкоцитурии, бактериурии и элиминации возбудителя;
- Фитокомплекс Нерей способствует активному отхождению солей всех химических типов – оксалатов, уратов и фосфатов;
- Применение фитокомплекса Нерей не оказывает влияния на изменения параметров функционального состояния почек, а также основных показателей обмена камнеобразующих веществ, рН мочи;
- На фоне приема фитокомплекса Нерей отмечается повышение диуреза, что сопровождается снижением относительной плотности мочи;
- Применение фитокомплекса Нерей не сопровождается нежелательными побочными эффектами.
ЗАКЛЮЧЕНИЕ
Проведенное исследование показало эффективность применения препарата Нерей в комплексном лечении пациентов, страдающих уролитиазом и перенесших различные виды оперативных вмешательств по удалению камней почек и мочеточников. Применение данного фитокомплекса особенно показано при микролитах почек и мочеточников, при формировании «каменных дорожек», так как способствует снижению количества и выраженности почечных колик и более быстрому и полному отхождению фрагментов разрушенных конкрементов.
Нерей обладает выраженными диуретическими, спазмолитическими, противовоспалительными и антибактериальными свойствами, эффективно способствуя устранению инфекционно-воспалительных осложнений мочекаменной болезни, характеризуется хорошей переносимостью и не имеет побочных эффектов.
ЛИТЕРАТУРА
- Шестаев А.Ю., Протощак В.В., Паронников М.В., Киселев А.О. Комбинированный (цитратный и растительный) препарат уриклар в дистанционной литотрипсии и метафилактике мочекаменной болезни. Урологические ведомости 2018;8(1):19-25. DOI: 10.17816/ uroved8119-25.
- Яненко Э.К., Меринов Д.С., Константинова О.В. Епишов В.А., Калиниченко Д.Н. Современные тенденции в эпидемиологии, диагностике и лечении мочекаменной болезни. Экспериментальная и клиническая урология 2012;(3):19-24.
- Каприн А.Д., Аполихин О.И., Сивков А.В., Москалева Н.Г., Солнцева Т.В., Комарова В.А. Анализ уронефрологической заболеваемости и смертности в Российской Федерации за 2003-2013 гг. Экспериментальная и клиническая урология 2015;(2):4-12.
- Черепанова Е.В., Дзеранов Н.К. Метафилактика мочекаменной болезни в амбулаторных условиях. Экспериментальная и клиническая урология 2010;(3):33-39.
- Гайбуллаев А.А., Кариев С.С., Турсунов Б.Ш. Применение комбинированных растительных мочегонных препаратов при уролитиазе. Экспериментальная и клиническая урология 2013;(4):76-81.
- Константинова О.В., Яненко Э.К., Шадеркина В.А. Метафилактика мочекислых камней почек. Экспериментальная и клиническая урология 2016;3:116-118.
- Beltrami P, Ruggera L, Guttilla A, Iannetti A, Zattoni F, Gigli F, et al. endourological treatment of renal matrix stones. Urol Int 2014;93(4):394-8.
- Sánchez-Martin FM, Millán Rodriguez F, Esquena Fernández S, et al. Incidence and prevalence of published studies about urolithiasis in Spain. A review. Actas Urol Esp 2007;31(5):511-20.
- Yasui T, Ando R, Okada A, Tozawa K, Iguchi M, Kohri K. Epidemiology of urolithiasis for improving clinical practic. Hinyokika Kiyo 2012;58(12):697-701.
- Cho ST, Jung SI, Myung SC, Kim TH. Correlation of metabolic syndrome with urinary stone composition. Int J Urol 2013;2(20):208-213.
- Константинова О.В., Шадеркина В.А. Опыт медикаментозного лечения пациентов с мочекислой формой мочекаменной болезни. Экспериментальная и клиническая урология 2015;(1):78-80.
- Сивков А.В., Черепанова Е.В., Шадеркина В.А. Применение фитопрепаратов на основе терпенов при мочекаменной болезни. Экспериментальная и клиническая урология 2011;(1):69-72.
- Авдошин В.П., Андрюхин М.И., Исрафилов М.Н. Комплексное лечение и метафилактика уратного и смешанного уролитиаза: метод. пособие для врачей. – М.: Спецкнига, 2013 32 с.
- Мартов А.Г., Гордиенко А.Ю., Москаленко С.А., Пенюкова И.В. Дистанционная и контактная уретеролитотрипсия в лечении крупных камней верхней трети мочеточника. Экспериментальная и клиническая урология 2013;(2):82-85.
- Khairy-Salem H, el-Ghoneimy M, el-Atrebi M. Ureteroscopy in management of large proximal ureteral calculi: is there still a role in developing countries? Urology 2011;5(77):1064-1068.
- Skolarikos A, Mitsogiannis H, Deliveliotis C. Indications, prediction of success and methods to improve outcome of shock wave lithotripsy of renal and upper ureteral calculi. Arch Ital Urol Androl 2010;1(82):56-63.
- Вощула В.И. Мочекаменная болезнь: этиотропное и патогенетическое лечение, профилактика. Минск: ВЭВЭР, 2006; 286 с.
- Лопаткин Н.А., Трапезникова М.Ф., Дутов В.В., Дзеранов Н.К. Дистанционная ударно-волновая литотрипсия: прошлое, настоящее, будущее. Урология 2007;(6):3-13.
- Блюмберг Б.И., Основин Р.Н., Фомкин Р.Н. Фитотерапия уратного нефролитиаза. Клиническая нефрология 2013;(1):71-72.
- Дзеранов Н.К., Константинова О.В., Москаленко С.А., Бешлиев Д.А., Бутин П.С., Дрозжева В.В., Конькова Т.А. Роль фитотерапии в до- и послеоперационном периоде у пациентов с мочекаменной болезнью. Урология 2005;(2):18-20.
- Сивков А.В., Дзеранов Н.К., Черепанова Е.В., Константинова О.В., Голованов С.А., Шадеркина В.А. Результаты применения препарата Роватинекс у больных, страдающих уролитиазом. Экспериментальная и клиническая урология 2011;(4):38-45.
- Гуденко Ю.А., Казанская И.В., Лобжанидзе З.Д. Применение препарата Роватинекс в детской урологии. Экспериментальная и клиническая урология 2013;(3):61-65.
- Глыбочко П.В., Аляев Ю.Г., Рапопорт Л.М., Цариченко Д.Г., Фролова Е.А. Cовременная консервативная (цитратная) терапия при уратных камнях мочеточников. Урология 2014;(5):10-13.
- Кариев С.С. Выбор продолжительности курсов фитотерапии оксалатного уролитиаза. Вестник Южно-Казахстанской медицинской академии 2008;3(40):50-56.
- Türk C, Knoll T, Petrik A, Sarica K, Skolarikos A, Straub M, et al. Guidelines on Urolithiasis. European Association of Urology 2015. Available from: http://uroweb.org/wp-content/uploads/22-Urolithiasis_ LR_full.pdf
- Анафин Т.Г., Досхожаев Б.К., Шалекенов С.Б.. Опыт применения препарата уриклар в комплексном лечении хронического пиелонефрита. Вестник казахского национального медицинского университета 2016;(3):61-67.
- Азарова О.В., Галактионова Л.П. Флавоноиды: механизм противовоспалительного действия. Химия растительного сырья 2012;(4):61-78.
Статья опубликована в журнале "Экспериментанльная и клиническая урология" №1 2019, стр. 82-89













Комментарии