Azadeh Elmi, Abdol-Mohammad Kajbafzadeh (kajbafzd@sina.tums.ac.ir), Ali Tourchi, Saman Shafaat Talab, Shadi Abdar Esfahani
Перевод и адаптация статьи: Сайт "Экстрофия мочевого пузыря и эписпадия" совместно с Татьяна Гарманова (НИИ урологии)
Детский урологический исследовательский центр, Детский центр научно-инновационный центр, Тегеранский Университет Медицинских наук, Тегеран, Иран
THE JOURNAL OF UROLOGY® Ноябрь 2011 г.
Цель: Дети с комплексом экстрофия мочевого пузыря – эписпадия (КЭМПЭ), проходившие эндоуретральную аутогенную миобластную трансплантацию (АМТ) для лечения недержания мочи, были оценены в течение 4-х летнего диспансерного наблюдения на предмет безопасности, эффективности и долговечности процедуры и связанного с лечением качества жизни.
Материалы и методы: Семеро мальчиков проходили аутогенную миобластную трансплантацию в период с мая по декабрь 2006 года. Все пациенты имели постоянную мочевую инконтиненцию после реконструкции шейки мочевого пузыря и инъекций увеличивающих объем агентов. Пациенты наблюдались в течение 4 лет после АМТ на предмет клинических результатов и цистометрических, уродинамических, уретроцистоскопических и урофлоуметрических показателей. Также оценивалось связанное со здоровьем качество жизни перед лечением и при финальном диспансерном наблюдении.
Результаты: Не было выявлено никаких признаков мочевой обструкции. Пятеро детей (71%) полностью удерживали мочу и двое (29%) были социально сухими с полной дневной сухостью при финальном наблюдении. Связанное со здоровьем качество жизни было значительно улучшено. Уродинамические исследования показали прогрессивный рост объема мочевого пузыря (p < 0.001). Среднее детрузорное давление точки утечки показало рост на 27 см H2O (158%) за 4 года дальнейших клинических наблюдений. Урофлоуметрические параметры опорожняемого объема мочи и средний максимальный уровень потока был значительно улучшен (p < 0.001). Это новое лечение представляет обещающий терапевтический подход у пациентов с мочевой инконтиненцией.
Выводы: Четырехлетние результаты демонстрируют, что аутогенная миобластная трансплантация при мочевой инконтиненции у детей с экстрофией мочевого пузыря – эписпадией является относительно надежной, воспроизводимой, безопасной и эффективной процедурой с минимальной заболеваемостью. Необходимы дальнейшие попытки с большим количеством пациентов.
Удержание мочи остается вызывающей целью в лечении детей с комплексом экстрофия мочевого пузыря – эписпадия. Большинство детей с этой кондицией проходят несколько хирургических процедур для менеджмента несостоятельности сфинктера, включая реконструкцию шейки мочевого пузыря, слинговую операцию и помещение искусственного сфинктера (1,2). Пациенты, у которых сохраняется инконтиненция, проходят реконструкцию мочевого резервуара. Заявленный уровень успеха в достижении континенции при нормальном опорожнении варьируется от 21% до 83% (3). Эти результаты могут включать пациентов с отведением мочи или тех, которые прошли аугментацию мочевого пузыря.
Эндоскопические инъекции увеличивающих объем агентов зарекомендовали себя как терапевтический подход для лечения мочевой инконтиненции (4). Эти процедуры кажутся экономичными, с более короткой госпитализацией и меньшим количеством основных осложнений. С другой стороны, деградация, миграция, реабсорбция, избыточное введение, обструкция выхода мочевого пузыря и гиперчувствительность часто отмечаются как осложнения после введения агентов.
Недавние исследования на людях и животных открыли роль скелетных мышц, полученных из стволовых клеток, для лечения мочевой инконтиненции (5-8). Мышечные клетки-предшественники (миобласты) характеризуются возможностью пролиферации (роста), дифференциации и финального расплавления для формирования новых волокон, ответственных за мышечные сокращения. Одной важной чертой этих клеток является то, что они не развиваются до требуемой реконструкции благодаря постмитатической природе миотуб (9).
Мы ранее предлагали подход использования АМТ для лечения инконтиненции мочи у детей с КЭМПЭ. Предварительные данные подтвердили эффективность и надежность АМТ для улучшения структуры и сократительной функции сфинктера при мочевой инконтиненции (10). Однако по нашим данным, долгосрочные результаты основанной на клетках терапии при мочевой инконтиненции еще не изучались у детей. Мы представляем наши открытия за 4-х летний период послеоперационного наблюдения касаемо связанного со здоровьем качества жизни, а также надежности, долгосрочности и эффективности аутогенного миобласта для лечения мочевой инконтиненции у детей с КЭМПЭ.
Пациенты и методы
Изначальное исследование включало 1 девочку и 7 мальчиков со средним возрастом 8,8 лет, которым предполагалось сделать аутогенную миобластную трансплантацию в период между маем и декабрем 2006 г. (10). Все пациенты были перенаправлены к нам после многочисленных неудачных вмешательств, включая закрытие мочевого пузыря, остеотомию лонных костей, реконструкцию шейки мочевого пузыря и операции на эписпадию.
Данное исследование было одобрено институциональным наблюдательным советом, и от родителей было получено письменное информированное согласие. Каждый пациент прошел цистоскопические инъекции от 7х106 до 4х107 аутогенных клеток в 8-10 мест в области наружного сфинктера (10).
Эффективность лечения была оценена у семи мальчиков на протяжении 4 лет. Лечение девочки расценили как полную неудачу из-за первичного провального лечения инконтиненции, и пациент был потерян для дальнейших наблюдений.
Оценка включала классификацию уровней инконтиненции, дневник мочеиспусканий, посев мочи, ультразвуковое исследование почек, цистограмму при мочеиспускании и уродинамические исследования. Дневная континенция была определена как сухие интервалы после сознательного (добровольного) мочеиспускания (11). Континенция была определена как дневная и ночная сухость в течение периодов более 3-х часов с мочеиспусканием через уретру. Уровень инконтиненции был основан на шкале от 0 до 3 (10). Пациенты считались социально сухими, если сухие периоды составляли более трех часов в дневное время с или без ночной инконтиненции или чистой интермиттирующей катетеризации.
Пациенты оценивались с помощью ультразвука в 1, 6 и 12 месяцев и далее дважды в год. Для определения функционального объема мочевого пузыря использовалась цистометрия. Исследования уродинамики и урофлоуметрии также исполнялись на ежегодной основе. Уродинамическое исследование (Duet®) было выполнено у всех детей в соответствии с Международным протоколом сообщества по континенции квалифицированной клинической детской медицинской сестрой - специалистом по уродинамике. Детрузорное давление точки утечки было определено как давление подтекания мочи вокруг катетера. Были определены максимальное давление детрузора при мочеиспускании и максимальный уровень потока.
В соответствии с нашим предыдущим исследованием, мы определили нормальную податливость мочевого пузыря как конечное наполняемое давление менее чем 20 см H2O, а стабильность мочевого пузыря как отсутствие несдерживаемых сокращений детрузора (более чем 15 см H2O) во время наполнения. Нормальное мочеиспускание считалось как нормальная динамика наполнения (податливость и стабильность мочевого пузыря) наряду с очевидными сокращениями детрузора при мочеиспускании. Одновременно выполнялась урофлоуметрия у всех детей, и был определен максимальный Qmax. В конце первого и четвертого годов выполнялась уретроцистоскопия для оценки любых дальнейших аномалий, воспалительных процессов или новообразований.
В целом не существует принятого результативного критерия для оценки успешности лечения. В данном исследовании были оценены три критерия до и после терапии для оценки успешности. Во-первых, инконтиненция была классифицирована согласно сухим интервалам по оценке в анкетах-опросниках пациентов. Далее, был оценен уровень качества жизни по качеству жизни с инконтиненцией до и через 4 года наблюдений после АМТ для оценки результатов терапии миобластами. Для определения уровня качества жизни использовались опросники самохарактеристик Kid-KINDL (для детей 8-12 лет) и Kiddo-KINDL (для 13-16 лет) и версия KINDL для родителей (детей от 8 до 16 лет). Эти три опросника состоят из 24 пунктов с 6 величинами. Общая сумма всех 24 отвеченных вопросов ранжируется от 24 до 100. Баллы переводятся в оценки между 0 и 100 (12), при этом большие баллы означают более высокий уровень качества жизни. И наконец, показатели уродинамики оценивали с помощью урофлоуметрии и исследования показателей давление-поток.
Все статистические анализы выполнялись с помощью SPSS®, версия 16.0. Переменные сравнивались по критерию хи-квадрата. Парный t-критерий Стьюдента использовался для сравнения постоянных переменных, и тест рангов Вилькоксона использовался для непараметрических статистических сравнений до и после лечения. Данные выражены как средние +-SD, и вероятность р < 0.05 считалась статистически значимой.
Результаты
Демографические и клинические характеристики детей до аутогенной трансплантации миобласта и после среднего дальнейшего клинического наблюдения в 15,3 месяцев и 4 года выделены в Таблице 1. Континенция была существенно улучшена у всех пациентов при финальном исследовании. До проведения аутогенной трансплантации миобласта 2 пациента (29%) были полностью инконтинентны и 5 (71%) были часто мокрыми с сухими интервалами менее 30 минут. На 15 месяце после клеточной инъекции 4 пациента стали социально континентны и 3 стали полностью сухими. В текущем наблюдении 5 мальчиков (71%) были полностью сухими и опорожнялись через уретру без интермиттирующей катетеризации, и 2 (29%) были социально континентны (разряд 1). Было три эпизода бектериурии у 2 пациентов, хотя не было свидетельств обструкции выхода или гидронефроза. Примечательно, что во время этого периода не наблюдалось свидетельств воспалений или гранулемы/формирования масс при цистоскопической оценке.
Таблица 1. Демографические и клинические характеристики пациентов
| Кол-во эпизодов недержания/недель | |||
| Пациент № - возраст | До операции | 15 мес. после операции | 48 мес. после операции |
| 1—19 | 2 | 0 | 0 |
| 2—11 | 3 | 1 | 0 |
| 3—10 | 2 | 0 | 0 |
| 4—15 | 3 | 1 | 1 |
| 5—10 | 2 | 1 | 0 |
| 6—10 | 2 | 1 | 1 |
| 7—12 | 2 | 0 | 0 |
В Таблице 2 представлены результаты опросников качества жизни KINDL до и через 4 года после процедуры. Средний +/-SD общий балл связанного со здоровьем качества жизни, заявленный у детей, не отличался значительно от оценок родителей при начальной оценке. В течение 4-летнего дальнейшего клинического наблюдения уровень качества жизни, связанного со здоровьем, был существенно улучшен (от 50,7 +/- 3,81 до 72,95 +/- 4,54), так же как и по данным родителей (от 51,42 +/- 3,78 до 67,14 +/- 7,56). Однако, дети выразили большее влияние на качество жизни, чем родители (р < 0,03). На этом уровне все родители были удовлетворены статусом континенции у их детей и заявили значительный рост индивидуальной и социальной активности пациента.
Таблица 2. Рузультаты на основе KINDL связанного со здоровьем качества жизни опросника
| Средний SD +/- до операции | Средний SD +/- 4 года после операции | Средняя SD +/- разница | Вероятность р | |
| Пациенты | ||||
| Физическое самочувствие | 39.43 +/- 6.63 | 72.14 +/- 8.09 | 32.72 +/- 8.26 | 0.001 |
| Эмоциональное самочувствие | 45.00 +/- 10.00 | 68.57 +/- 11.44 | 23.57 +/- 5.56 | 0.001 |
| Самооценка | 52.14 +/- 7.56 | 75.71 +/- 10.18 | 23.57 +/- 4.75 | 0.001 |
| Семья | 53.57 +/- 7.48 | 72.58 +/- 9.51 | 19.28 +/- 10.97 | 0.001 |
| Друзья | 43.57 +/- 11.80 | 67.14 +/- 11.50 | 23.57 +/- 6.27 | 0.001 |
| Каждодневное функционирование | 67.86 +/- 9.06 | 82.14 +/- 9.06 | 14.29 +/- 5.35 | 0.001 |
| Общий балл | 50.57 +/- 3.81 | 72.95 +/- 4.54 | 22.38 +/- 3.16 | 0.001 |
| Родители | ||||
| Физическое самочувствие | 41.43 +/- 6.90 | 69.14 +/- 9.84 | 27.71 +/- 7.73 | 0.001 |
| Эмоциональное самочувствие | 47.14 +/- 7.56 | 69.29 +/- 12.05 | 22.14+/- 10.35 | 0.001 |
| Самооценка | 47.14 +/- 6.99 | 74.29 +/- 9.76 | 27.14 +/- 10.74 | 0.001 |
| Семья | 50.00 +/- 6.45 | 71.43 +/- 6.27 | 21.43 +/- 10.70 | 0.002 |
| Друзья | 49.29 +/- 13.05 | 71.42 +/- 8.02 | 22.14 +/- 11.85 | 0.003 |
| Каждодневное функциониро-вание | 62.15 +/- 9.94 | 73.57 +/- 8.02 | 11.42 +/- 9.88 | 0.022 |
| Общий балл | 51.42 +/- 3.78 | 67.14 +/- 7.56 | 15.71 +/- 5.35 | 0.001 |
Объем мочевого пузыря показал значительный повышающийся тренд в исследованиях в период наблюдения (29,64% в 6 месяцев, 47% в 12 месяцев и 59% в 4 года, Таблица 3). Отмечен годовой рост объема мочевого пузыря на 69,3 мл в течение первого года после процедуры и на 21,84 мл каждый год в течение 4-х лет наблюдений. До операции все пациенты имели нормальную податливость мочевого пузыря, которая оставалась неизмененной в течение 4 лет наблюдений. В настоящее время все пациенты имеют нормальное сокращение детрузора и мочеиспускание.
Таблица 3. Результаты клинического дальнейшего наблюдения
|
Средний +/-SD объем мочевого пузыря (мл) |
Среднее +/-SD детрузорное давление точки утечки (см H2O) |
Средний +/-SD Qmax (мл/сек) |
| До операции | 140 +/- 30.10 | 17 +/- 4.10 | 9 +/- 5.00 |
| 6 мес. после операции | 181 +/- 41.30* | 38 +/- 6.80* | 14 +/- 4.30† |
| 12 мес. после операции | 206 +/- 49.30* | 40 +/- 8.10* | 16 +/- 5.90† |
| 4 года после операции | 222 +/- 43.31* | 45 +/- 8.90* | 17 +/- 6.50* |
* p <0.001 в сравнении с до операции |
|||
† p = 0.001 в сравнении с до операции |
|||
Уродинамическое исследование продемонстрировало постоянный рост в среднем детрузорном давлении точки утечки в течение наблюдений, развивая 125%-ый прирост в 6 месяцев, 135% в 12 месяцев и 158% за 4 года (Таблица 3). Из урофлоуметрических параметров статистически значимый рост Qmax наблюдался в 6 месяцев в сравнении с долечебным (р < 0,001). Аналогичный тренд наблюдался в 1 год и в 4 года (Таблица 3).
Дискуссии
Лечение инконтиненции остается вызовом в менеджменте детей с КЭМПЭ (1, 2). Поперечнополосатые мышцы наружного сфинктера играют главную роль в поддержании континенции во время наполнения мочевого пузыря. Детям с КЭМПЭ не достает этой функции из-за неэффективности сфинктерных структур (10).
В последнее десятилетие АМТ была предназначена как улучшенная альтернатива для лечения мочевой инконтиненции. Эти клетки могут проходить обновление и плавление для формирования новых волокон, способных к мышечному сокращению (8). Некоторые исследования описали успешные краткосрочные результаты терапии миобластами и фибробластами при женском стрессовом недержании мочи и после простатэктомии (7).
Мы ранее верифицировали эффективность эндоуретральной АМТ в рамках статуса континенции и уродинамических и урофлоуметрических параметров у 7 мальчиков и 1 девочки с КЭМПЭ (10). Миобласты были получены из биопсии скелетных мышц. Клеточные популяции характеризовались оценкой экспрессии генов Рах7 при иммунофлюоресценции. Онтогенез культур определялся с использованием anti-MyoD и анти-десминовых антител. Мы отметили значительный тренд улучшения в статусе континенции в течение 15 месяцев клинических наблюдений у 7 мальчиков. Мы наблюдали зависимое от времени улучшение континенции после АМТ со существенным ростом объема мочевого пузыря и с сохранением его податливости. Все 7 мальчиков достигли нормального мочеиспускания с очевидным сокращением детрузора.
У пациента-девочки не наблюдалось никакого существенного улучшения, несмотря на некоторые положительные изменения уродинамических показателей. Широкая шейка мочевого пузыря и относительно фиброзная уретра могут объяснить неуспех лечения у данного пациента. В текущем клиническом наблюдении не были учтены данные по этому пациенту.
Основные беспокойства по поводу основанной на стволовых клетках регенерации тканей вызывают риски клеточной миграции, трансдифференциации, формирования новообразований и риски апоптоза (гибели клеток) - все это может ограничить сохранность клеток и выживаемость трансплантата. Неинвазивная система клеточного трекинга для мониторинга в реальном времени за трансплантированными клетками не была еще ратифицирована в клинических условиях. Для этой цели долгосрочные исследования, оценивающие возможные функциональные результаты этих клеток, могут быть очень полезными. В этой связи мы оценили критические характеристики менеджмента инконтиненции с клинической точки зрения в течение 4-х лет наблюдений. Наше исследование показало, что дети с КЭМПЭ, страдающие от постоянного недержания мочи, после реконструкции шейки мочевого пузыря и даже инъекций увеличивающих объем агентов, могут получить лечение с помощью АМТ с постоянными значительными результатами и существенным эффектом на связанное со здоровьем качество жизни. Следует отметить, что в течение 4-х лет после клеточной трансплантации, не было свидетельств неблагоприятного эффекта от такой клеточной терапии, включая мочевую обструкцию, инфекции и развитие новообразований. Это открытие предлагает приемлемо надежный очерк для дальнейших клинических применений аутогенных миобластов с приемлемой технической доступностью.
В данном исследовании 5 пациентов (71%) были полностью континенты через 4 года и 2 пациента (29%) продемонстрировали социальную сухость. Прогрессивное улучшение в параметрах континенции было существенно выше, чем во всех основных предыдущих работах, эксплуатирующих роль увеличивающих объем материалов при инконтиненции мочи (13-15). Это динамическое улучшение является важной характеристикой миобластов в лечении инконтиненции в сравнении с другими типичными увеличивающими объем агентами, которые ассоциируются с прогрессивным снижением в параметрах инконтиненции во время первого года после инъекции.
Детрузорное давление точки утечки было использовано как мера сфинктерного сопротивления на детрузорное давление, и давление менее 40 см H2O считалось инконтинентным на базе работы МакКормака и др. (McCormack et al) (16). В нашем долгосрочном клиническом наблюдении после операции детрузорное давление точки утечки зафиксировало продолжающееся увеличение, что подтверждает, что рост детрузорного давления точки утечки ассоциируется с лучшими результатами удержания при КЭМПЭ.
Одним из ключевых моментов, влияющих на нормальное восстановление у пациентов с КЭМПЭ является баланс между сопротивлением выхода мочевого пузыря и факторами объема, податливостью и эффективным мочеиспусканием. Важными осложнениями после большинства процедур, направленных на совершенствование сопротивления выхода мочевого пузыря, являются слабая податливость мочевого пузыря, малый объем и ненормальная функция детрузора (11). Все пациенты в нашем исследовании имели нормальную податливость мочевого пузыря без признаков нестабильности мочевого пузыря. Прогрессивный рост был замечен в Qmax и объеме мочевого пузыря, возможно благодаря эффективным сокращениям детрузора и функциональном увеличении выходного сопротивления соответственно. Рост в выходном сопротивлении мочевого пузыря и податливости мочевого пузыря мог быть благодаря уникальным свойствам миобластов при интеграции в сфинктер уретры.
Хотя пациенты с КЭМПЭ подвергаются различным вмешательствам для улучшения общего состояния, было проведено мало исследований уровня связанного со здоровьем качества жизни детей с этой аномалией (17-19). При измерении качества жизни у этих пациентов, кажется, неизбежно необходимым оценивать разные вмешательства для сравнения разных тактик лечения для предоставления ценной информации при консультировании родителей о будущем их детей. Мочевая инконтиненция ассоциируется со сниженным качеством жизни. У серии подростков с КЭМПЭ Додсон и др. (Dodson et al) отметил, что пациенты с мочевой инконтиненцией имеют более низкий средний балл по родительскому эмоциональному влиянию, чем дети с удержанием (20).
Оценка детского качества жизни связанного со здоровьем является вызовом. Опросники с собственными отчетами, кажутся, наиболее близкими к детскому опыту, хотя когда ребенок растет с этой аномалией, он или она могут не иметь примеров для сравнения. В связи с этим была разработана версия для родителей. Однако оценки качества жизни могут различаться между родителями и детьми и могут даже противоречить друг другу.
Мы измеряли собственные и родительские оценки качества жизни в наших сериях. Качество жизни было оценено с использованием опросников Kid-KINDL, Kiddo-KINDL и KINDL для родителей (21). Следует отметить, что существенный рост качества жизни через 4 года после клеточной трансплантации сопровождался благоприятными изменениями в статусе континенции и уродинамических показателях. Пациенты и родители сообщили о значительном влиянии после 4-х лет. Однако дети заявили о более низком качестве жизни, чем родители, до интервенции, так же как и более высоком качестве жизни после интервенции.
Мы верим, что показаниями для АМТ при КЭМПЭ является постоянная мочевая инконтиненция после реконструкции шейки мочевого пузыря (см. рисунок). Тем не менее, этот метод кажется менее эффективным или даже противопоказанным для пациентов со значительным повреждением верхних мочевых путей, воспалительными процессами или тяжелым шрамированием задней уретры и шейки мочевого пузыря.
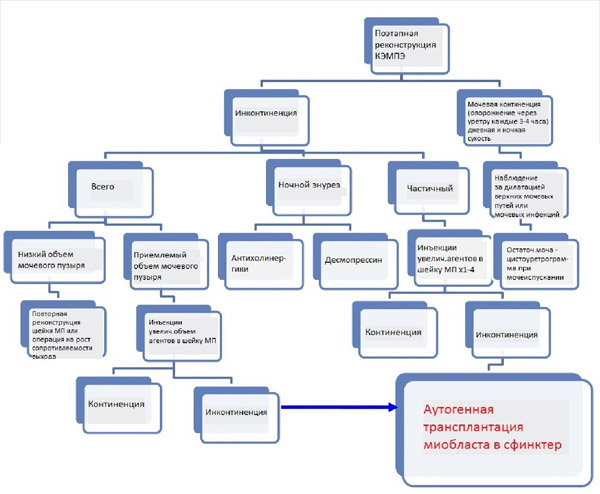
Для данной серии существуют некоторые ограничения. Данное исследование было выполнено без контрольной группы, хотя низкая распространенность КЭМПЭ ограничивает возможность контроля исследования единственной операцией. Не представлены данные о внутренних и внешних наблюдателях, поскольку все инъекции были выполнены одним хирургом. Вдобавок, так как только 1 девочка с КЭМПЭ прошла АМТ, роль клеточной терапии у девочек с КЭМПЭ остается невыясненной. Однако эффект тестотерона на мышечные клетки может быть причиной для успеха у мальчиков, проходящих АМТ. Необходимы дальнейшие попытки с большими популяциями и более длительными периодами дальнейших клинических наблюдений.
Выводы
Долгосрочные результаты подтверждают, что АМТ при мочевой инконтиненции у детей с КЭМПЭ является относительно надежной, безопасной, долгосрочной и воспроизводимой процедурой, выполняемой амбулаторно, имеет минимальную заболеваемость (смертность) и чрезвычайно эффективна. Наши данные показывают, что эта новая модель лечения могла бы представлять общепризнанный, обещающий терапевтический подход для пациентов с мочевой инконтиненцией, когда имеется достаточный объем мочевого пузыря и нет детрузорной нестабильности или тяжелого пузырно-мочеточникового рефлюкса.









Комментарии