Л. Г. Спивак, Д. В. Платонова, Д. В. Еникеев, Л. М. Рапопорт, А. З. Винаров, Ю. Л. Демидко
- Кафедра урологии лечебного факультета ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» Минздрава России (Сеченовский Университет), Москва, Россия
Введение. Эректильная дисфункция (ЭД) – продолжающаяся более 6 мес. неспособность достигать эрекции, достаточной для проведения полноценного полового акта, и/или поддерживать ее [1]. Эректильная дисфункция (прежнее название – импотенция) – широко распространенная патология. Она вызывает беспокойство примерно у половины мужчин в возрасте от 40 до 70 лет. Эректильная дисфункция снижает качество жизни, поскольку сопровождается повышенной тревожностью, сниженной самооценкой, неуверенностью в себе и напряженностью в отношениях с половыми партнерами.
Эрекция – нейроваскулотканевой феномен, связанный с гормональным контролем. Он включает расширение кавернозных артерий, расслабление гладкой мускулатуры трабекул и активацию веноокклюзионного механизма кавернозных тел [2, 3].
Эректильная дисфункция определяется как постоянная неспособность достигать и поддерживать эрекцию, достаточную для успешного полового акта. Несмотря на то что ЭД – это доброкачественное расстройство, она может негативно влиять на физическое и психосоциальное здоровье, а также отражаться на качестве жизни пациентов и их партнерш [4]. Появляется все больше доказательств того, что ЭД может быть ранним проявлением ишемической болезни сердца (ИБС) и других системных сосудистых заболеваний. Таким образом, ЭД не следует рассматривать только с точки зрения качества жизни. Ее можно считать предупредительным сигналом, указывающим на наличие сердечно-сосудистого заболевания и локального проявления распространенной сосудистой патологии – эндотелиальной дисфункции, атеросклероза, сахарного диабета [5–9]. Так, из 154 мужчин, обратившихся за помощью в связи с ЭД, у 44% была диагностирована артериальная гипертензия (АГ) и у 23% – сахарный диабет [10]. Е. Ricci et al. [11] считают, что частота выявления гиперхолестеринемии у пациентов с ЭД в 2 раза выше, чем у таковых без нарушений эрекции. Атеросклеротические изменения в пенильном сосудистом русле приблизительно в 40% случаев обусловливают развитие ЭД у мужчин в возрасте старше 50 лет. Нередко различные проявления атеросклероза, например ИБС, и ЭД развиваются параллельно, поскольку факторы риска дисфункции эндотелия коронарных и пенильных кровеносных сосудов одинаковы. Не случайно сердечно-сосудистые заболевания достоверно чаще встречаются среди пациентов с АГ и ЭД, чем среди больных АГ без нарушений сексуальной функции [12]. Исследование S. A. Hall et al. [13] продемонстрировало связь дислипидемии и ЭД. По мнению авторов, прогноз для жизни больного, имеющего дислипидемию и ЭД, менее благоприятен по сравнению с пациентом без ЭД. Именно поэтому наиболее предпочтительными были бы лекарственные средства, способные также влиять и на липидный обмен, тем самым устраняя не только следствие, но и причину возникновения сексуальных нарушений.
Для ЭД, как уже отмечалось выше, характерна высокая распространенность в популяции, увеличивающаяся с возрастом. Эректильной дисфункцией страдают более 10% мужчин в возрасте 21 года, а к 40–50 годам почти в половине случаев у мужчин могут наблюдаться нарушения эрекции той или иной степени выраженности [14]. Эта проблема весьма распространена в развитых странах. Средняя распространенность ЭД в США и Европе – 45%, при этом отмечается стойкая тенденция к увеличению данного показателя с возрастом. До 30,8% мужчин страдают ЭД в 30-летнем возрасте, а к 70 годам их количество достигает 76% [15].
Эректильная функция является ключевым индикатором качества жизни многих мужчин. Для большинства из них именно нарушение в сексуальной сфере наносит намного более значимый урон качеству жизни, нежели симптомы нарушенного мочеиспускания, вызванные аденомой простаты или другими причинами.
К сожалению, прогнозы распространенности ЭД в будущем также неутешительны. Так, если в 1995 г. ЭД была диагностирована у 152 млн мужчин, то к 2025 г., по прогнозам ВОЗ, число таких мужчин достигнет 322 млн [16].
В 2012 г. в России было проведено исследование, определившее, что почти половина (49,7%) мужчин в возрасте 20–45 лет имеет симптомы ЭД различной степени тяжести. А ведь это мужчины в самом активном возрасте, который к тому же соответствует репродуктивному [17].
В настоящее время для лечения ЭД используются преимущественно препараты, получаемые методом химического синтеза. Это прежде всего лекарственные средства первой линии – ингибиторы фосфодиэстеразы 5-го типа (иФДЭ5). Они обладают высокой эффективностью, однако при их применении может возникать ряд нежелательных явлений (НЯ), специфичных как для группы иФДЭ-5 в целом (приливы, головная боль), так и для отдельных препаратов в частности (например, миалгия и боль в спине при применении тадалафила) [18]. В связи с этим актуальным становится применение растительных негормональных препаратов, обладающих достаточной эффективностью и большей безопасностью. К данной группе можно отнести лекарственные средства растительного происхождения Трибестан («Софарма АО», Болгария) и ЭФФЕКС Трибулус (ЗАО «Эвалар», Россия), изготовленные на основе сухого экстракта травы якорцев стелющихся (Tribulus terrestris).
Таблица. Распределение пациентов
| Распределение пациентов | Количество пациентов (%) |
|---|---|
| Скринировано | 175 (100,0) |
| Рандомизировано (FAS) | 173/175 (98,9) |
| Не включено в исследование: | 2/175 (1,1) |
| отзыв информированного согласия | 2/2 (100,0) |
| Группа I (ЭФФЕКС Трибулус) | 87/173 (50,3) |
| Группа II (Трибестан) | 86/173 (49,7) |
| Популяция для анализа безопасности (ITT) | 173/173 (100,0) |
| Пациент выполнил все визиты и процедуры настоящего исследования (PP) | 152/173 (87,9) |
| Не включено в PP-популяцию: | 21/173 (11,1) |
|
7/21 (33,3) |
|
1/21 (4,8) |
|
13/21 (61,9) |
Примечание. НЯ – нежелательные явления.
Несмотря на широкое применение Tribulus terrestris в народной медицине преимущественно в качестве лекарственного средства от бесплодия и ЭД, до середины ХХ в. не проводилось контролируемых исследований, способных доказать его эффективность и безопасность. Масштабные клинические исследования Tribulus terrestris и его основного действующего вещества, протодиосцина, связаны с появлением на рынке препарата Трибестан, который представляет собой сухой экстракт травы якорцев стелющихся (Tribulus terrestris) – 250 мг в 1 таблетке с содержанием суммы фуростаноловых сапонинов в пересчете на протодиосцин не менее 112,5 мг. Трибестан в качестве препарата растительного происхождения был зарегистрирован в 1981 г. и одобрен для использования в клинической практике в Европе (в том числе в России) и в США. Согласно данным доклинических и клинических исследований, Трибестан стимулирует сперматогенез [19], способствует повышению уровня тестостерона, улучшению эректильной функции, усилению либидо [20]. Кроме того, препарат обладает гиполипидемическим эффектом [21].
Препарат ЭФФЕКС Трибулус (ЗАО «Эвалар», Россия) – отечественный аналог препарата Трибестан. ЭФФЕКС Трибулус изготовлен из сухого экстракта травы якорцев стелющихся (Tribulus terrestris) – 250 мг в 1 таблетке с содержанием суммы фуростаноловых сапонинов в пересчете на протодиосцин и сухое вещество 45% (112,5 мг). Идентичный состав по стандартизированному активному веществу протодиосцину позволяет рассматривать данные препараты как эквивалентные.
В данной статье мы имеем честь представить результаты открытого проспективного сравнительного рандомизированного многоцентрового клинического исследования эффективности и безопасности препаратов ЭФФЕКС Трибулус и Трибестан для пациентов с ЭД. Результаты, полученные в ходе исследования, имеют важное значение для выбора качественных, эффективных и безопасных препаратов для лечения ЭД врачами в повседневной практике.
Цель исследования: провести сравнительную оценку эффективности и безопасности применения препаратов ЭФФЕКС Трибулус (ЗАО «Эвалар», Россия) и Трибестан («Софарма АО», Болгария) пациентами с ЭД.
Материалы и методы. Медицинским экспертом исследования стал Спивак Леонид Григорьевич, к.м.н., доцент кафедры урологии ФГАОУ ВО «Первый МГМУ им. И. М. Сеченова» (Сеченовский Университет) Минздрава России.
В клиническом исследовании приняли участие 11 ведущих российских урологических центров с участием главных исследователей С. Х. Аль-Шукри, С. И. Гамидов, В. Г. Гомберг, В. В. Дутов, М. С. Евдокимов, О. Ф. Каган, Г. Г. Кривобородов, Л. Г. Спивак, К. П. Тевлин, В. Х. Хейфец, И. С. Шорманов.
Перед включением в исследование провели с пациентами беседу и предоставили им письменную информацию о задачах и методах проведения исследования, а также об ожидаемой пользе и возможном риске, связанных с участием в исследовании, добровольном характере участия в исследовании, о том, что пациент имеет право отказаться от участия в исследовании в любой момент, что этот отказ не повлияет на качество предоставляемой ему медицинской помощи и не повлечет потери выгод, на которые пациент имеет право. Согласие пациента получали до проведения процедур, предусмотренных дизайном исследования, за исключением таковых, данные о которых были получены как анамнестические (например, данные предыдущих обследований).
Первичным критерием оценки терапевтической эквивалентности/эффективности служит динамика результатов тестирования по показателю «эректильная функция» шкалы МИЭФ. К вторичному критерию оценки терапевтической эквивалентности/эффективности относится динамика результатов тестирования по показателям «удовлетворенность половым актом», «оргазмическая функция», «либидо», «общая удовлетворенность» шкалы МИЭФ (Международный индекс эректильной функции).
Основные методы оценки результатов нашего исследования:
- динамика результатов тестирования по шкалам
- МИЭФ (Международный индекс эректильной функции);
- AMS (The Aging Males’ Symptoms scale);
- СФМ (Сексуальная формула мужская) и по опроснику;
- GAQ (Global Assessment Question);
- критерии оценки безопасности (в скобках указаны сроки регистрации соответствующих параметров):
- частота и выраженность НЯ (на протяжении всего периода исследования)
- данные клинического и биохимического анализов крови, ОАМ (предварительное обследование пациента, визит 5);
- данные ЭКГ (предварительное обследование пациента, визит 5);
- частота и выраженность нежелательных реакций на препарат (переносимость терапии – визиты 3 и 5).
Исследование проведено в условиях амбулаторного приема пациентов врачом. Общая продолжительность участия пациента в исследовании составила 14 нед., длительность наблюдения пациента в период приема исследуемого препарата/ препарата сравнения – 13 нед. В течение 1 мес. после прекращения приема исследуемого препарата/препарата сравнения пациент имел возможность обратиться к врачу-исследователю. Оценка состояния пациента произведена на пяти визитах
На первом визите (за неделю до начала терапии) проведена оценка соответствия пациентов критериям включения/ невключения.
В исследование включены пациенты с установленным диагнозом ЭД, не обусловленной органическими нарушениями или болезнями (код по МКБ-10: F52.2) легкой, умеренно-легкой и умеренной степени тяжести (11–25 баллов по показателю «эректильная функция» шкалы МИЭФ) в возрасте старше 18 лет при наличии подписанного информированного согласия и письменного согласия пользоваться барьерными методами контрацепции.
Основные критерии невключения: органические поражения клапанов сердца и сосудов, сопровождавшиеся декомпенсированной коронарной и сердечной недостаточностью, индекс массы тела (ИМТ) >40 кг/м2 , СД 1 типа (инсулинозависимый), декомпенсированный СД 2 типа и другие стандартные критерии невключения. Следует отметить, что одним из критериев невключения были гипотестостеронемия при содержании общего тестостерона в сыворотке крови <8 нмоль/л, а также органические и сосудистые нарушения в половых органах.
Также при первом визите проведен комплекс инструментальных и лабораторных исследований.
Данный комплекс включал:
- сбор анамнеза, осмотр с оценкой общего состояния, жалоб, клинических симптомов (ЧДД, ЧСС, АД), антропометрические измерения; - сбор информации о предшествовавшей и сопутствующей терапии;
- УЗИ сосудов полового члена с фармакопробой;
- ЭКГ;
- клинический анализ крови;
- общий анализ мочи;
- биохимический анализ крови (глюкоза, HbA1c, ТГ, ОХС, ХС ЛПНП, ХС ЛПВП, АЛТ, АСТ, общий и прямой билирубин, креатинин);
- определение общей и свободной фракции тестостерона;
- определение содержания других гормонов: ФСГ, ЛГ, эстрадиола, пролактина, ГСПГ, ПСА, ТТГ.
Кроме того, при первом и всех последующих визитах проведена оценка эректильной функции и качества половой жизни пациентов при помощи опросников МИЭФ, AMS, СФМ, GAQ.
На втором визите осуществлены рандомизация пациентов, назначение терапевтического курса и выдача препарата (ЭФФЕКС Трибулус или Трибестан).
На третьем (5 нед. от начала терапии) и четвертом (9 нед. от начала терапии) визитах проведена промежуточная оценка эректильной функции и качества половой жизни при помощи вышеуказанных опросников. Также на третьем визите осуществлено титрование дозы и учет принятого пациентами количества препарата, на четвертом – оценка комплаентности.
На пятом (13 нед. от начала терапии – окончание курса лечения) визите вновь проведены оценка эректильной функции и качества половой жизни при помощи опросников, а также приведенного выше комплекса инструментальных и лабораторных исследований.
Всего в исследование были включены 173 пациента, из них 87 (50,3%) были рандомизированы в группу I (ЭФФЕКС Трибулус), 86 (49,7%) – в группу II (Трибестан). Полностью завершили исследование, выполнив все процедуры, 152 пациента (см. таблицу). Средний возраст пациентов составил 42,2±11,5 лет в группе I и 42,8±11,2 года в группе II (p>0,05, критерий Манна–Уитни). Пациенты, включенные в исследование, имели склонность к полноте. Так, ИМТ в группе I составил в среднем 26,32±3,19 кг/м2 , в группе II – 27,14±5,10 кг/м2 . Анализ данных по истории основного заболевания (ЭД) показал, что пациенты обеих групп имели сходные показатели (p>0,05). Ни у одного пациента обеих групп не отмечено осложнений основного заболевания, однако 14 (16,1%) пациентов группы I и 22 – группы II имели сопутствующие заболевания, наиболее часто встречающимися из которых оказались вторичная гипертензия (n=10), хронический простатит (n=5) и хронический гастрит (n=4). Среди пациентов обеих групп 70% не курили, 45% не употребляли алкоголь. Половина пациентов обеих групп отмечала свою низкую физическую активность. В целом следует отметить, что проведенный сравнительный межгрупповой анализ изучаемых в нашем исследовании характеристик пациентов показал, что по всем анализируемым показателям группы были статистически достоверно однородными, что свидетельствует об адекватности приведения рандомизации. Это касалось всех исходных параметров, включая лабораторные тесты, показатели допплерографии, которую проводили в первую очередь для исключения ЭД, связанной с нарушением венозного оттока.
Всем пациентам был назначен единый режим дозирования препаратов: по 1 таблетке 3 раза в сутки (суточная доза – 750 мг) в течение 5 нед. На третьем визите в случае необходимости увеличивали дозу до 2 таблеток 3 раза в сутки (суточная доза 1500 мг) в течение 8 нед.
Статистические методы. Для анализа параметров эффективности в данном исследовании была использована популяция всех включенных в исследование пациентов (FAS, Full analyses set), а также пациентов, закончивших исследование без существенных отклонений от Протокола (PP, per protocol).
Для анализа параметров безопасности была использована популяция пациентов, которые приняли хотя бы одну дозу исследуемого препарата или препарата сравнения и для которых имелись данные по оценке безопасности, по крайней мере измеренные в одной временной точке после приема препарата (ITT, intention-to-treat analyses).
В отчете приведена описательная статистика, характеризующая пациентов, включенных в исследование. Для каждого демографического параметра (масса тела, возраст, рост, индекс массы тела [ИМТ], лабораторных [анализ крови, анализ мочи] и жизненно важных показателей [АД, ЧСС, ЧД, температура тела]), а также для параметров эффективности (показатель «эректильная функция» шкалы МИЭФ, результаты тестирования по шкалам AMS, СФМ, опроснику GAQ, показатели содержания общей и свободной фракции тестостерона в крови) и безопасности (частота развития НЯ/СНЯ) в зависимости от типа переменной вычислены:
- Минимальное значение (Min);
- Максимальное значение (Max);
- Арифметическое среднее (M);
- Стандартное отклонение (SD);
- 95% доверительный интервал (ДИ) для среднего;
- Медиана (Me);
- Межквартильный размах (IQR);
- Частота (%).
При анализе данных проведено предварительное тестирование той или иной переменной на нормальность распределения с помощью тестов Шапиро–Уилка, а также теста на асимметрию и эксцесс. В случае нормального распределения для статистического анализа применялись параметрические тесты: t-тест, парный t-тест. При значительном отклонении от нормальности (p<0,05) использованы непараметрические тесты: Манна–Уитни, Уилкоксона. Кроме того, для оценки динамики параметров эффективности использовано построение модели обобщенного линейного регресса (GLM).
Сравнительная оценка динамики показателя «эректильная функция», а также других показателей шкалы МИЭФ была дополнительно проведена путем построения модели обобщенного линейного регресса (GLM). В качестве зависимой переменной в этих моделях использовано абсолютное значение соответствующего показателя, в качестве независимых переменных были протестированы «время» (номер визита), «группа» (1 – для исследуемого препарата; 2 – для препарата сравнения), а также их парное взаимодействие «группа*время». Динамика каждого из показателей представлена графически в разделе «Результаты».
Для оценки параметров безопасности, представляющих категориальные данные (частота развития НЯ, частота развития отклонений по данным ЭКГ и данных физикального осмотра) был использован χ2 -критерий и при необходимости точный тест Фишера (если количество случаев было менее 5). Проверка на отсутствие статистически значимых различий между визитом 1 и визитом 5 по параметрам безопасности, представляющим численные переменные (лабораторные показатели, жизненно важные функции) была проведена при помощи параметрического (парный t-тест Стьюдента) или непараметрического тестов (критерий Уилкоксона) в зависимости от типа распределения данных. Межгрупповое сравнение разности указанных показателей между визитами 5 и 1 проведено с помощью t-теста (либо теста Манна–Уитни). Поправка на множественность сравнения делалась с помощью метода Бонферрони.
Все применяемые гипотезы носили двусторонний характер, и во всех случаях уровнем статистической значимости принято значение p<0,05. Статистическая обработка данных была проведена с помощью программы Stata14
Результаты. В настоящем исследовании эффективность лечения пациентов оценивали прежде всего с помощью шкалы МИЭФ, которая включает пять основных показателей: эректильную функцию, удовлетворенность половым актом, оргазмическую функцию, либидо, общую удовлетворенность.
Согласно рекомендациям регуляторных органов, для анализа основной считается FAS-популяция, включающая всех рандомизированных пациентов.
Показатель «эректильная функция» шкалы МИЭФ протоколом исследования был определен в качестве первичного критерия эффективности. Данный показатель увеличился в группе I с 19,2±3,6 балла на визите 1 до 25,0±3,9 – на визите 5. В группе II аналогичные показатели составили 19,0±3,4 и 24,1±5,2 балла соответственно. В обеих группах отмечено планомерное повышение данного показателя от визита к визиту. Таким образом, среднее увеличение показателя «эректильная функция» на визите 5 относительно визита 1 составило 5,7±4,6 балла в группе I и 5,2±4,3 – в группе II (t-тест, p=0,467; рис. 1).
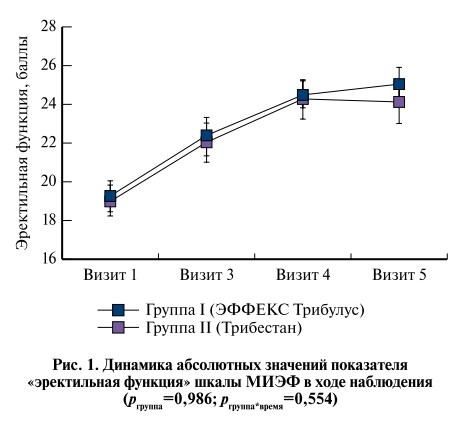
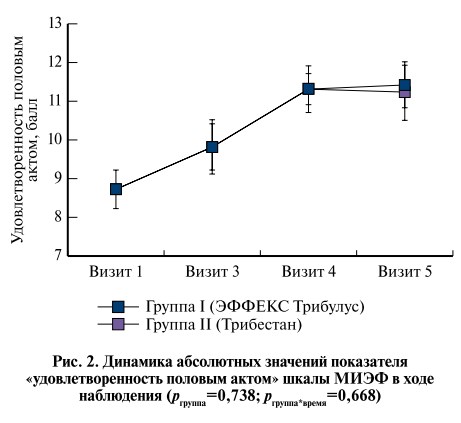
Проведенный анализ не выявил статистически значимых различий в динамике ни по одному из представленных показателей шкалы МИЭФ (pгруппа>0,05, pгруппа*время>0,05). При этом в каждой из групп наблюдалось направленное статистически значимое увеличение всех показателей шкалы МИЭФ (pвремя<0,05) (рис. 2–5).
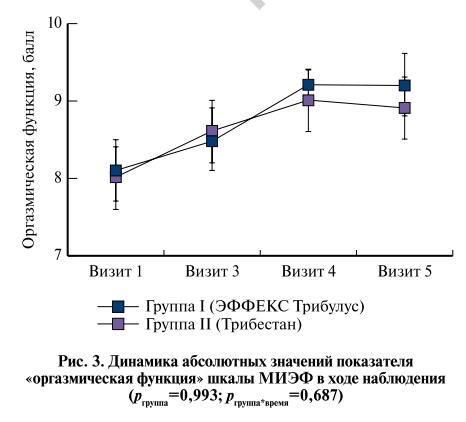
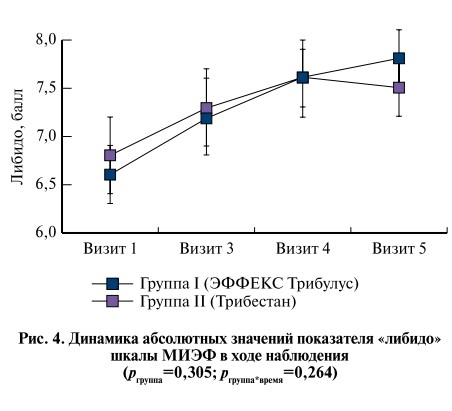
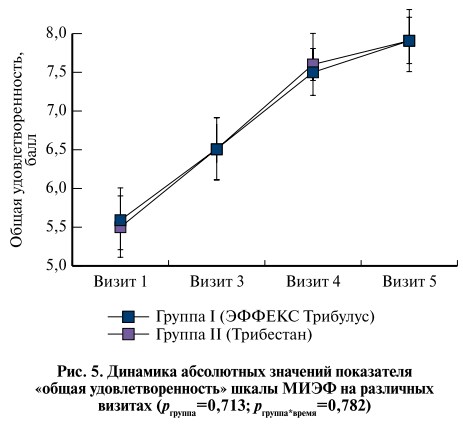
Попарное межгрупповое сравнение с помощью критерия Манна–Уитни также не выявило статистически значимых различий между группами как для FAS-, так и для PP-популяции (PP-популяция – популяция пациентов, завершивших исследование в соответствии с протоколом).
Вторичными показателями эффективности в данном исследовании стали результаты тестирования по шкалам AMS и СФМ. Значение показателя шкалы AMS в группе I снизилось с 32,93±10,04 балла на визите 1 до 25,02±7,62 – на визите 5, в группе II соответствующие показатели составили 31,78±10,37 и 24,55±7,31 балла (рис. 6). Показатель СМФ, напротив, увеличился с 22,36±4,85 до 27,16±4,80 балла в группе I и с 22,13±3,69 до 26,10±5,69 – в группе II (рис. 7)
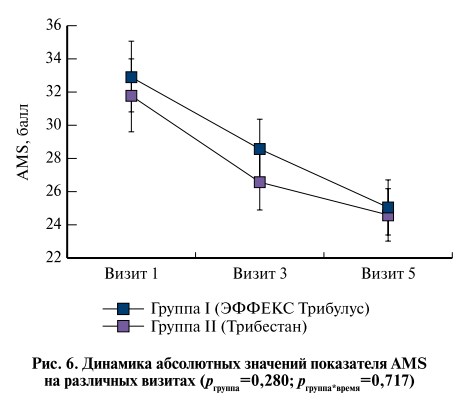
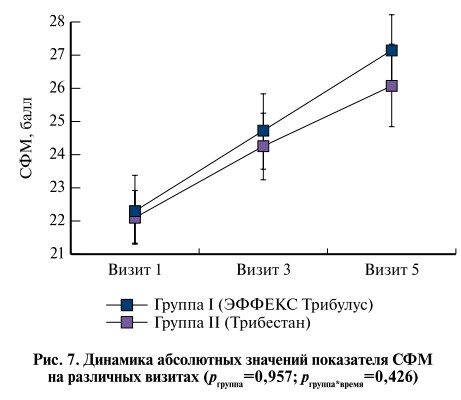
Проведенный анализ с помощью GLM не выявил статистически значимых различий в динамике показателей AMS и СМФ (pгруппа>0,05, pгруппа*время>0,05). Как и для показателей МИЭФ, в обеих группах отмечена положительная динамика показателей AMS и СМФ от визита 1 к визиту 5 (pвремя0,05).
Анализ данных по итогам заполнения пациентами опросника GAQ был проведен с помощью χ2 -критерия. Доля пациентов, ответивших «Да» на визите 5, составила 90,2% в группе I и 90,5% в группе II (p>0,05).
Немаловажным аспектом проведения любого клинического исследования является изучение безопасности назначаемой терапии и анализ НЯ, возникших в ходе исследования. В данном исследовании было зарегистрировано 7 НЯ: 5 – в группе I и 2 – в группе II. Два НЯ (оба в группе II) имели среднюю степень тяжести, пять НЯ – легкую. Два НЯ (повышение уровней АЛТ и АСТ) были зарегистрированы на последнем визите 5 по результатам биохимического анализа крови, поэтому были отмечены как сохраняющиеся до конца исследования. Остальные 5 НЯ разрешились без последствий для пациентов. Длительность всех НЯ не превышала 7 дней.
Только одно из зарегистрированных НЯ – аллергический дерматит – имело, по мнению врача-исследователя, связь с приемом исследуемого препарата (ЭФФЕКС Трибулус). Прием исследуемого препарата был полностью прекращен. Данное НЯ имело легкую степень тяжести и разрешилось без последствий через 7 дней после появления. Два отмеченных клинически значимых отклонения лабораторных показателей (повышение уровней АЛТ и АСТ) были зарегистрированы как НЯ, имевшие легкую степень тяжести и не связанные с приемом исследуемого препарата, по мнению врачаисследователя. В ходе исследования не было выявлено ни одного клинически значимого изменения жизненно важных показателей ни в одной из групп. Также между группами не было выявлено статистически значимых различий по доле пациентов с наличием отклонений по данным объективного осмотра и ЭКГ.
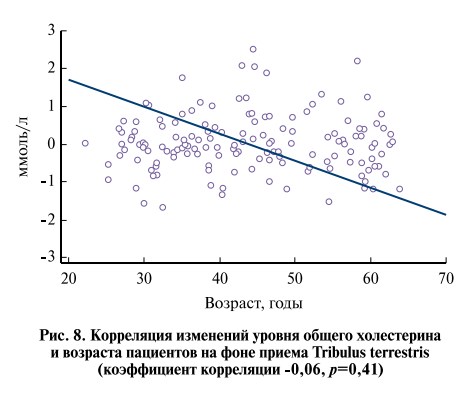
Таким образом, проведенный анализ позволяет заключить, что оба препарата имеют схожий профиль безопасности. На рис. 8 отдельно представлена динамика уровня холестерина на фоне приема Tribulus terrestris.
Анализ взаимосвязи между уровнем холестерина и приемом исследуемого препарата показал, что с увеличением возраста происходит более выраженное снижение уровня холестерина на фоне приема Tribulus terrestris (рис. 8).
Изучая изменения данных параметров в ходе исследования, можно сделать вывод: в обеих группах происходило снижение холестерина у мужчин в возрасте старше 45 лет, что свидетельствует о позитивном влиянии обоих изучаемых препаратов на липидный обмен. Что касается комплаентности, то ее анализ не выявил статистически значимых различий в приверженности лечению среди пациентов двух групп (p>0,05).
Заключение. Проведенное исследование позволяет заключить, что препарат ЭФФЕКС Трибулус (ЗАО «Эвалар», Россия) характеризуется сопоставимой эффективностью и профилем безопасности по сравнению с препаратом Трибестан («Софарма АО», Болгария) при применении пациентами с ЭД старше 18 лет.
ЛИТЕРАТУРА/REFERENCES
- NIH Consensus Development Panel of Impotence. Impotence. JAMA. 1993;270:83–90.
- Kogan M.I. Erectile dysfunction (current opinion). Rostov-on-Don. 2005. 336. Russian (Коган М.И. Эректильная дисфункция (текущее мнение). Ростовна-Дону. 2005. 336).
- Krotovsky G.S. Treatment of vascular impotence. M., 1998. 159 c. Russian (Кротовский Г.С. Лечение сосудистой импотенции. М., 1998. 159 c.).
- Loran O.B., Segal A.S., Shcheplev P.A. Prostaglandin E1 in the diagnosis and treatment of erectile dysfunction. Urology and nephrology. 1995,4:35–38. Russian (Лоран О.Б., Сегал А.С., Щеплев П.А. Простагландин Е1 в диагностике и терапии нарушений эрекции. Урология и нефрология. 1995;4:35–38).
- Mazo E.B., Gamidov S.I. Erectile disfunction. M.: Bech. 2004. 120 c. Russian (Мазо Е.Б., Гамидов С.И. Эректильная дисфункция. М.: Beчe. 2004. 120 c.).
- Pushkar D.Yu., Vertkin A.L. Erectile dysfunction: cardiological aspects. М.:: MEDpress-inform. 2005. Russian (Пушкарь Д.Ю., Верткин А.Л. Эректильная дисфункция: кардиологические аспекты. М.: МЕДпресс-информ. 2005).
- Pushkar D.Yu., Segal A.S., Bagayev A.G., Nosovitsky P.B. Iohimbine in the treatment of erectile dysfunction. Urology. 2002;6:34–37. Russian (Пушкарь Д.Ю., Сегал А.С., Багаев А.Г., Носовицкий П.Б. Иохимбин в терапии эректильной дисфункции. Урология. 2002;6:34–37).
- Urology: a textbook for universities / Ed. acad. RAMS N.A. Lopatkina. Moscow: GEOTAR-Media, 2005. Russian (Урология: учебник для вузов / Под ред. акад. РАМН Н. А. Лопаткина. М.: ГЭОТАР-Медиа, 2005).
- Benet A.E., Melman A. The epidemiology of erectile dysfunction. Impotence. Urol. Clin. N. Amer. 1995;22:699–709.
- Walczak M.K., Lokhandwala N., Hodge M.B., Guay A.T. Prevalence of cardiovascular risk factors in erectile dysfunction. J. Gend. Specif. Med. 2002;5(6):19–24.
- Ricci E., Parazzini F., Mirone V. et al. Current drug use as risk factor for erectile dysfunction: results from an Italian epidemiological study. Int. J. Impot. Res. 2003;15:221–224.
- Burchardt M., Burchardt T., Anastasiadis A.G., Kiss A.J., Shabsigh A., de La Taille A., Pawar R.V., Baer L., Shabsigh R. Erectile dysfunction is a marker for cardiovascular complications and psychological functioning in men with hypertension. Int. J. Impot. Res. 2001;13(5):276–281.
- Hall S.A., Kupelian V., Rosen R.C., Travison T.G., Link C.L., Miner M.M., Ganz P., McKinlay J.B. Is hyperlipidemia or its treatment associated with erectile dysfunction? Subtitle: Results from the Boston Area Community Health (BACH) Survey. J. Sex. Med. 2009;6(5):1402–1413.
- Carson C.C., Burnett A.L., Levine L.A. et al. The efficacy of sildenafil citrate (Viagra) in patients with erectile dysfunction. Urology. 2002;60(2 Suppl. 2):12–27.
- Rosen R., Altwein J., Boyle P. et al. Lower urinary tract symptoms and male sexual dysfunction: the multinational survey of the aging male (MSAM-7). Eur. Urol. 2003;44(6):637–649.
- Ayta I.A., McKinlay J.B., Krane R.J. The likely worldwide increase in erectile dysfunction between 1995 and 2025 and some possible policy consequences. BJU Int. 1999;84(1):50–56.
- Pushkar D.Yu., Kamalov A.A., Al-Shukri S.H., Erkovich A.A., Kogan M.I., Pavlov V.N., Zhuravlev V.N., Bernikov A.N. Epidemiological study of the prevalence of erectile dysfunction in the Russian Federation. Urologiia. 2012;6:5–9. Russian (Пушкарь Д.Ю., Камалов А.А., Аль-Шукри С.Х., Еркович А.А., Коган М.И., Павлов В.Н., Журавлев В.Н., Берников А.Н. Эпидемиологическое исследование распространенности эректильной дисфункции в Российской Федерации. Урология. 2012;6:5–9).
- Popko A.S., Lokshin K.L. Current opportunities of drug therapy for patients with erectile dysfunction. Effective pharmacotherapy. Urology and nephrology. 2016;23(3):14–16. Russian (Попко А.С., Локшин К.Л. Современные возможности медикаментозной терапии пациентов с эректильной дисфункцией. Эффективная фармакотерапия. Урология и нефрология. 2016; 23(3):14–16).
- Kumanov F. et al. A clinical trial with the medicine Tribestan. Andrologia. 1995;3:21–24.
- Adimoelja A., Adaikan P.G. Protodioscin from herbal plant Tribulus terrestris L improves the male sexual functions, probably via DHEA. 6th Biennial Asia-Pacific Meeting on Impotence in Kuala Lumpur, Malaysia (1997). Int. J. Impotence Research. 1997;9(supp 1):20.
- Guidelines for the examination of medicines. Volume I. M.: Grief and K. 2013. 328 p. Russian (Руководство по экспертизе лекарственных средств. Том I. М.: Гриф и К. 2013. 328 c.).






Комментарии