Россоловский А.Н.1,2, Чехонацкая М.Л.1,2, Захарова Н.Б. 1,2, Березинец О.Л.1,2, Емельянова Н.В.2
1 НИИ фундаментальной и клинической уронефрологии ГБОУ ВПО Саратовского ГМУ им. В.И.Разумовского Минздрава России, г.Саратов 2 Клиническая больница им. С.Р.Миротворцева ГБОУ ВПО Саратовского ГМУ им. В.И.Разумовского Минздрава России, г.Саратов Адрес: 410012, г.Саратов, ул. Большая Садовая, 137, тел. (845)669751 Эл.почта: rossol@list.ru
Введение
В последние десятилетия значительно изменились подходы к диагностике и лечению мочекаменной болезни. Разрабатываются новые и совершенствуются малоинвазивные хирургические пособия, позволяющие в большинстве случаев избежать открытых операций [1]. Несмотря на большое число современных методик, вошедших в урологическую практику за последнее десятилетие, метод дистанционной ударно-волновой литотрипсии (ДЛТ), возникший в 80-е годы прошлого века, не только не утратил своего значения, но и продолжает занимать одно из ведущих мест в лечении данного заболевания [2].
Считается, что ДЛТ является неинвазивным методом лечения, который хорошо переносится пациентами и сопровождается низким уровнем осложнений [3]. Однако многочисленными исследованиями было доказано, что ударная волна, независимо от природы генератора, все же вызывает значительные побочные эффекты. Суммируя данные различных авторов, изучавших влияние ДЛТ на почечную ткань, можно заключить, что к типичным изменениям после процедуры ДЛТ следует относить нарушения почечной микроциркуляции, деструкцию почечной ткани в зоне клубочков, отек и интерстициальные нарушения медуллярного слоя почки, разрыв капилляров, тромбоз венул, кровоизлияние и частичный некроз канальцев с исходом в нефросклероз, а в более отдаленном периоде – снижение функции почки и артериальную гипертензию [4].
Очевидно, что внедрение в клиническую практику новых информативных критериев оценки степени повреждения почечной паренхимы, сопоставимое по информативности с морфологическими исследованиями, могло бы послужить объективной основой регулирования параметров волнового воздействия и оптимизации тактики ДЛТ.
Для оценки степени выраженности почечного повреждения к настоящему времени предложено большое число прямых и непрямых маркеров. При этом традиционные показатели почечной недостаточности, такие как уровень сывороточного креатинина (сКр), скорость клубочковой фильтрации (СКФ) и данные некоторых визуализирующих методик с определением толщины слоя паренхимы, позволяют оценивать почечное повреждение на более поздних стадиях, когда почечная паренхима начинает утрачивать свои функции. Так, измерение концентрации сКр не всегда отражает объем и степень повреждения, т.к. этот показатель отстает по времени от момента повреждающего воздействия [5], а также не позволяет дифференцировать острое почечное повреждение от прогрессирующего хронического почечного заболевания [6].
Одним из ключевых маркеров широко использующемся в клинической практике для разграничений стадий хронической болезни почек и прогнозирования темпов ее прогрессирования является величина СКФ. Однако определение СКФ не всегда надежно отражает степень истинного почечного повреждения. Например, при компенсаторной гипертрофии остаточных нефронов и их сохраненной фильтрационной способности редукции СКФ может не происходить [7]. Эти данные подтверждены и в работе Waikar S.S. и соавт., которые отметили, что снижение СКФ не всегда наблюдается даже в случаях тяжелого паренхиматозного повреждения почек [8].
С внедрением в клиническую практику дуплексной допплерографии почечного кровотока с цветным картированием потока крови появилась реальная возможность количественной оценки состояния микроциркуляторного русла почки, различные варианты изменений которого могут быть как проявлением адаптации почечной гемодинамики к изменениям внутриполостного давления при МКБ, так и следствием изменений структуры почечной паренхимы. Несмотря на широкое использование ультразвуковой дуплексной допплерографии, эта методика все еще не является общепринятой для оценки функционального состояния почки. R.Ikee et al., 2005 [9] показано, что индекс резистентности может непосредственно отражать как сосудистые, так и тубулоинтерстициальные изменения в почках. Кроме того, возраст, сывороточный креатинин, экскреция β2микроглобулина с мочой, и ряд морфометрических параметров, в том числе клубочковой склероз, интерстициальный фиброз, атрофия канальцев, лимфогистиоцитарная инфильтрация и артериолосклероз показали статистически значимые корреляции с индексом резистентности.
В последние годы предложен ряд биомаркеров, экскретирующихся с мочой и позволяющих дифференцировать острое и хроническое повреждение почек на самых ранних стадиях. Большинство этих маркеров представляют собой соединения, экспрессирующиеся в канальцевом аппарате почек и в повышенных количествах выделяющихся в мочу при условии повреждения данного органа. К ним относятся интерлейкин-18 (ИЛ-18), молекула почечного повреждения-1, нейтрофил – гелатиназа-ассоциированный липокалин (neutrophil gelatinase-associated lipocalin, NGAL или липокалин-2 (Л-2)), а также ряд ферментов, в норме обычно локализующиеся в щеточной кайме проксимальных канальцев [10].
Липокалин-2, регистрируемый ранее, чем накопление креатинина сыворотки [11], является также перспективным маркером хронической болезни почек: он обратно пропорционален СКФ при почечной дисплазии, обструктивной уропатии и гломерулярных заболеваниях почек. Недавно предложена теория «горящего леса», объясняющая связь между NGAL и СКФ [12]. Рост NGAL согласно этой теории, есть не только пассивное следствие снижения почечного клиренса, но результат «горящих» (поврежденных) тубулярных клеток, тогда как рост концентрации креатинина и снижение СКФ есть всего лишь пассивный результат потери функционирующих нефронов. Поэтому NGAL является индикатором активного повреждения почечной паренхимы в реальном времени при хронической болезни почек.
Клиническое значение этих показателей при различных патологических состояниях только начинает оцениваться.
В связи с этим целью нашего исследования явилась оценка степени травматичности дистанционной ударноволновой литотрипсии с применением стандартных и новых маркеров почечного повреждения.
Материалы и методы
Обследовано 167 пациентов с МКБ. Группу контроля составили 40 практически здоровых добровольцев. Все пациенты были разделены на 2 группы. Первую группу составили 80 больных, которым провели 1 сеанс ДЛТ до достижения эффективной фрагментации конкремента. Плотность камней по данным компьютерной томографии у пациентов данной группы в среднем составила 800-1100 НU, количество импульсов за сеанс 2000-3000, мощность генератора 12-15,5 кВ.
Вторая группа включала 87 больных МКБ с камнями средней и высокой плотности (800-1300 НU и более), которым выполнено 2-4 сеанса ДЛТ в течение 1-3 мес., а количество импульсов составляло 2500-4000 за один сеанс, мощность генератора 14-18 кВ. Данная группа, в отличие от 1-й, включала значительную часть пациентов (57,5%) с анамнезом МКБ ≥ 5 лет и длительным течением хронического калькулезного пиелонефрита. Степень освобождения полостной системы от конкремента после первого сеанса в данной группе в среднем составила 52,9% и существенно зависела от плотности, размера, месторасположения и химического состава конкремента, а также длительности анамнеза МКБ.
Критериями исключения из исследования являлись: возраст старше 60 лет, острый пиелонефрит, обструкция мочевых путей, почечная недостаточность в острой и терминальной стадиях, внепочечная локализация конкрементов, а также тяжелая сопутствующая патология, в том числе выраженная артериальная гипертензия, морбидное ожирение, сахарный диабет и онкологические заболевания.
Всем пациентам проводили ультразвуковое исследование почек и их сосудов на аппарате SonoAce-9900 Prime (Medison). При оценке состояния внутрипочечной гемодинамики у больных МКБ использовали дуплексное сканирование почечного кровотока с определением систолической (Vps) и диастолической (Vpd) скоростей, индекса резистентности (Ri) и пульсового индекса (Pi).
Всем пациентам в образцах мочи методом твердофазного иммуноферментного анализа на иммуноферментном анализаторе Stat Fax 2010 (США) были исследованы маркеры острого почечного повреждения – липокалин-2(NGAL) с помощью тест наборов реактивов фирмы Biosourse (США), β2микроглобулина (β2-МГ) с помощью тест наборов реактивов фирмы Orgentec Diagnostica GmbH (Германия). Забор мочи для анализа проводили в динамике: при поступлении, на 5-7-е, 10-14-е сутки и через 1-3 месяца после ДЛТ.
Концентрацию креатинина сыворотки крови измеряли с использованием стандартных лабораторных методов. Расчет СКФ проводился с использованием уравнения Сockroft-Gault и формулы MDRD.
Статистический анализ осуществили с использованием пакета программ статистической обработки результатов StatSoft Statistica 7.0.
Результаты
При оценке функционального состояния почек традиционными методами у больных 1-й группы до ДЛТ не выявлено значительных изменений, сопровождающихся азотемией. Так, у большинства пациентов 1-й группы имелась 2-я стадия ХБП (81%) и у 19% была выявлена 1-я стадия ХБП. На 5-7-е сутки после ДЛТ у пациентов данной группы отсутствовало клинически значимое повышение сКр и снижение СКФ, что свидетельствует неизменности фильтрационной способности почек после однократного сеанса ДЛТ, определяемой стандартными методами (рисунок 1).
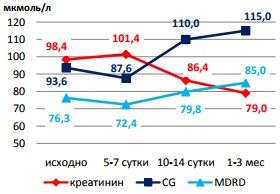
Рис. 1. Динамика показателей функционального состояния почечной паренхимы при однократном сеансе ДЛТ
При этом на 10-14-е сутки отмечали снижение сКр ниже исходного уровня, а через 1-3 месяца после вмешательства у больных 1-й группы происходила нормализация уровня сКр и СКФ. Так, сКр у больных после 1 сеанса ДЛТ через 1-3 месяца был равен в среднем 79 мкмоль/л, а СКФCG – 115 мкмоль/л и CКФMDRD = 85 мкмоль/л. Прирост СКФ через 1-3 месяца после вмешательства составил 11,7%.
Таким образом, после 1 сеанса ДЛТ и применения указанных выше параметров не отмечено достоверно значимого изменения функциональной способности почек, а улучшение фильтрационной способности происходило уже к 10-14-м суткам после процедуры и через 1-3 месяца после лечения имело место незначительное повышение скорости клубочковой фильтрации.
Вместе с тем, у пациентов 1-й группы изменения почечного кровотока в раннем периоде (3-5-е и 7-10-е сутки) после ДЛТ характеризовались снижением Vpd и повышением Ri и Pi на уровне сегментарных артерий и дуговых артерий (рисунок 2).
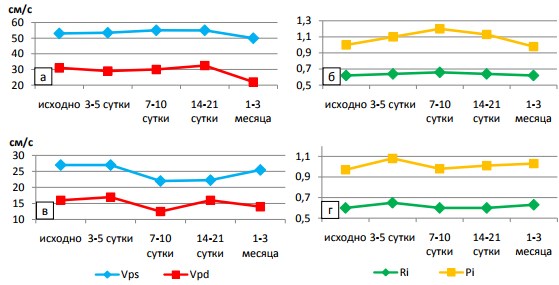
Рис. 2. Динамика параметров внутрипочечного кровотока после сеанса ДЛТ у больных нефролитиазом: а) и б) на уровне сегментарных артерий; в) и г) на уровне дуговых артерий
На 14-21-е сутки после ДЛТ у пациентов 1-й группы отмечали снижение Ri и Pi на уровне дуговых и сегментарных артерий. В то же время на уровне дуговых артерий отсутствовала полная нормализация параметров кровотока через 1-3 месяца после вмешательства.
Описанные изменения у больных 1-й группы свидетельствуют о нарушении процессов микроциркуляци в периоперационном периоде. Показатели допплерографии, используемые в качестве маркеров почечного повреждения, демонстрируют бóльшую чувствительность по сравнению с такими стандартными методами оценки как сКр и СКФ.
Изучение маркеров острого почечного повреждения (ОПП) в моче у больных 1-й группы выявило, что пики активности uNGAL совпадают с эпизодами повышения концентрации uβ2МГ. При этом на 5-7-е сутки после ДЛТ происходит значительное повышение данных показателей. В то же время уже к 10-14-м суткам после лечения исследуемые показатели снижаются до исходных значений, а в дальнейшем через 1-3 месяца отмечается быстрое снижение данных величин практически до контрольных значений (рисунок 3).
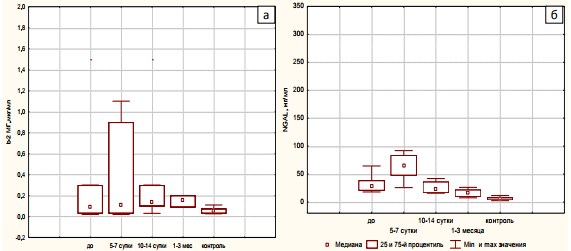
Рис. 3. а) uβ2-МГ в оценке ОПП у больных МКБ после одного сеанса ДЛТ; б) динамика uNGAL в моче у больных МКБ после ДЛТ
Кратковременное повышение концентрации маркеров ОПП после ДЛТ указывает на незначительный объем повреждения почечной паренхимы на фоне однократного сеанса ударноволнового воздействия. Кроме того, данная работа подтверждает мнение ряда исследователей, что у представленной когорты больных (1 группа) морфофункциональные изменения, возникающие в почках в течение недели после травматизации нефрона ударной волной, являются локальными и обратимыми.
Оценка функционального состояния почек до ДЛТ у больных 2-й группы выявила некоторое исходное снижение функции почек (СКФCG=88,7 мл/мин, СКФMDRD=67,6 мл/мин (рисунок 4). Так, у 34,5% больных данной группы по результатам формулы MDRD была выявлена 3-я стадия ХБП, а у 65,5% – диагностирована ХБП-2.
В то же время, несмотря на отсутствие значимого изменения функции на 5-7-е сутки после лечения, т.е. после выполнения первого сеанса литотрипсии, на 10-14-е сутки, когда у большинства пациентов 2-й группы были проведены повторные сеансы ДЛТ, было отмечено повышение уровня сКр и снижение СКФ (СКФCG=76 мл/мин, СКФMDRD=57 мл/мин). При этом через 1-3 месяца после лечения сохраняется снижение функции почек у большинства пациентов. Так, через 1-3 месяца после нескольких процедур ДЛТ СКФCG в среднем составила 78 мл/мин, а СКФMDRD=61 мл/мин (снижение СКФ составило 10% от исходной) (р≤0,05). При этом уровень сКр у больных данной группы после ДЛТ не превышал значений нормальной функции почек (в среднем 110 мкмоль/л). Кроме того, степень снижения СКФ через 1-3 месяца после лечения коррелировала с числом ударных волн (r=0,6; р=0,05) (рисунок 4).
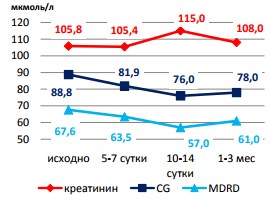
Рис. 4. Динамика показателей функционального состояния почечной паренхимы в периоперационном периоде (ДЛТ 2 и более сеансов)
Таким образом, выявленное с помощью расчетных методик снижение фильтрационной способности почек оказалось значительным и сохранялось у больных 2-й группы через 1-3 месяца после вмешательства и также требовало дальнейшего наблюдения и лечения на амбулаторном этапе.
У пациентов 2-й группы исходные изменения почечного кровотока были более выраженными: Ri на уровне дуговых артерий у пациентов 2-й группы составил в среднем 0,66 против 0,60 у пациентов 1-й группы. Такая закономерность вероятно обусловлена продолжительным анамнезом МКБ (у большинства пациентов более 5 лет) и длительным течением хронического калькулезного пиелонефрита. В раннем периоде (3-5-е и 7-10-е сутки) после ДЛТ происходило незначительное улучшение параметров гемодинамики по сравнению с исходными значениями. Так, отмечалось улучшение скоростных показателей и снижение Ri и Pi на уровне сегментарных и дуговых артерий (рисунок 5).
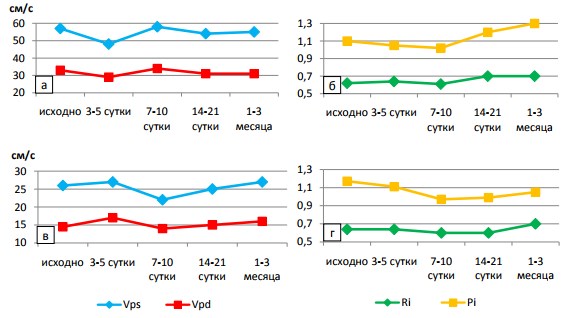
Рис. 5. Динамика параметров внутрипочечного кровотока после нескольких сеансов ДЛТ: а) и б) на уровне сегментарных артерий; в) и г) на уровне дуговых артерий
В то же время на 14-21-е сутки после вмешательства у пациентов 2-й группы вновь отмечали повышения Ri и Pi, которые на всех уровнях достигли своего максимума (Ri=0,74). Нарушения процессов микроциркуляции продолжали нарастать и сохраняться через 1-3 месяца после ДЛТ (рисунок 5). По сравнению с пациентами 1-й группы у больных 2-й группы через 1-3 месяца после ДЛТ отмечали диагностически значимое повышение Ri на сегментарных и дуговых артериях по сравнению с исходными показателями (0,70 и 0,69 против 0,61 и 0,62 соответственно). Данная тенденция, по-видимому, обусловлена повторными ударно-волновыми воздействиями, с минимальными интервалами между процедурами, что приводило к увеличению зоны повреждения паренхимы почки у больных 2-й группы.
Подобные изменения свидетельствуют о значительном нарушении процессов микроциркуляции на фоне травмы, превосходящие исходные изменения внутрипочечного кровотока. Кроме того, подобные нарушения у пациентов 2-й группы значительно прогрессировали на фоне многократных процедур литотрипсии, что может способствовать снижению функциональной способности почечной паренхимы в отдаленном периоде за счет снижения массы перитубулярных капилляров.
У больных 2-й группы на 5-7-е сутки после ДЛТ происходило значительное повышение концентрации uβ2-МГ, сохраняющееся практически неизмененным и на 10-14-е сутки после процедуры, что обусловлено дополнительной альтерацией канальцев на фоне повторных сеансов ДЛТ (рисунок 6). Кроме того, через 1-3 месяца после лечения у пациентов не только не происходило нормализации данного показателя, но и возникало незначительное повышение концентрации uβ2-МГ. Сохраняющееся через 1-3 месяца после ДЛТ канальцевое повреждение указывало на необходимость коррекции сроков повторных вмешательств и применения нефропротективных подходов в данный период времени, а также более продолжительное амбулаторное наблюдения нефрологом данной категории больных.
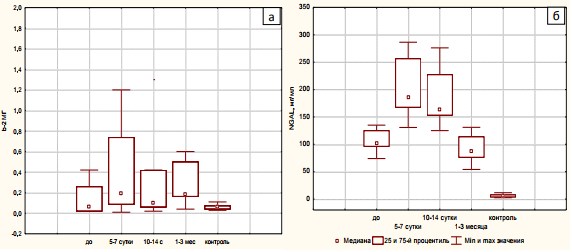
Рис. 6. а) уровни uβ2-МГ в оценке ОПП у больных МКБ после нескольких процедур ДЛТ; б) изменение концентрации uNGAL в моче у больных МКБ после нескольких сеансов ДЛТ
Таким образом, зона повреждения после повторных процедур ДЛТ значительно увеличивается по сравнению с однократным воздействием. При этом восстановление поврежденной почечной паренхимы у больных 2-й группы происходит достаточно медленно, на что указывает отсутствие достоверного снижения концентрации маркеров ОПП через 1-3 месяца по сравнению с показателями до ДЛТ. Кроме того, уровни маркеров ОПП через 1-3 месяца после нескольких сеансов ДЛТ остаются повышенными по сравнению с контролем. Изучение в динамике концентрации маркеров ОПП после ДЛТ у больных 2-й группы позволило определить наименее благоприятные с точки зрения последующих повторных воздействий интервалы времени.
Таким образом, у больных 1-й и 2-й групп имело место различной степени выраженности повреждение почечной паренхимы, приводящее у пациентов 2-й группы к снижению почечной функции через 1-3 месяца.
По данным стандартных и новых методик исследований были выявлены выраженные изменения почечной паренхимы на фоне ДЛТ-травмы, послужившие причиной значительной активации у исследуемых пациентов процессов нефрофиброза. Таким образом, колебания концентраций маркеров ОПП и показателей состояния микроциркуляторного русла отражают сущность патофизиологических изменений в результате альтерации почечной паренхимы и позволяют более четко представить механизмы нарушения почечной функций на фоне ДЛТ-травмы.
Можно заключить, что использование сКр у пациентов после ДЛТ в качестве основного маркера почечного повреждения может привести к неоправданному «завышению» оценки функциональной способности почек, существенно ухудшая при этом отдаленные результаты лечения. Имея представления об истинных значениях функциональной способности почек до ДЛТ, определяемых на основании уравнения MDRD, пациенты данной группы нуждаются в дополнительных рекомендациях. В частности, необходимо активно выявлять и нивелировать факторы, приводящие к снижению почечной функции (ликвидация воспаления, бактериурии, нормализация уродинамики).
Очевидно, что наличие информативных критериев оценки степени повреждения почечной паренхимы в ходе лечения нефролитиаза может служить основанием для определения оптимальных режимов волнового воздействия и объективизации сроков проведения повторных процедур ДЛТ.
Выводы
1. ДЛТ камней почек приводит к повреждению почечной паренхимы различной степени выраженности, возрастающей с увеличением количества сеансов литотрипсии.
2. Использование дуплексного сканирования почечного кровотока является высокоинформативным методом оценки нарушений микроциркуляции почечной паренхимы у больных после ДЛТ, лежащих в основе прогрессирования ХБП.
3. К ранним маркерам острого почечного повреждения у пациентов с мочекаменной болезнью следует относить увеличение экскреции с мочой β2-МГ и NGAL, достоверно отражающих наличие ренальных повреждений в периоперационном периоде. Высокий уровень NGAL является наиболее информативным индикатором активного повреждения почечной паренхимы на фоне имеющейся ХБП.
Литература
1. Саенко, В. Ведение больных мочекаменной болезнью в послеоперационном периоде / В. Саенко, В. Руденко, Н. Сорокин // Врач. – 2008. – №1. – С.7679.
2. Коган, М.И. Роль перкутанной нефролитотомии в лечении больных с коралловидным нефролитиазом / М.И. Коган, А.В. Хасигов, И.И. Белоусов // Саратовский научно-медицинский журнал. – 2011. – Т. 7, №2. – С.170.
3. McAteer, J. A. The acute and longterm adverse effects of shock wave lithotripsy / J. A. McAteer, A. P. Evan // Semin. Nephrol. – 2008. – Vol.28. – P.200213.
4. Гулямов, С.М. Диагностика, профилактика и лечение повреждения почки при дистанционной ударно-волновой литотрипсии : дис. … канд. мед. наук. – Спб., 2004. – С.140.
5. Lameire, N. Reflections on the definition, classification, and diagnostic evaluation of acute renal failure / N. Lameire, E. Hoste // Curr Opin Crit Care. – 2004. – Vol.10. – P.468–477.
6. Bonventre , J.V. Recent advances in the pathophysiology of ischemic acute renal failure / J.V. Bonventre , J.M. Weinberg // J Am Soc Nephrol. – 2003. – Vol.14. – P.2199–2210.
7. Becker G.J. The role of tubulointerstitial injury in chronic renal failure / G.J. Becker, T.D. Hewitson // Curr. Opin. Nephrol. Hypertens. – 2000. – Vol.9. – P.133-138.
8. Waikar, S.S. Diagnosis, epidemiology and outcomes of acute kidney injury / S.S. Waikar, K.D. Liu, G.M.Chertow // Diagnosis Clin J Am Soc Nephrol. – 2008. – Vol.3(3). – P.844–861.
9. Correlation between the resistive index by Doppler ultrasound and kidney function and histology / R. Ikee, et al. // Am. J. Kidney Dis. – 2005. – Vol.46, №4. – P.603-609.
10. Melnikov V. Y. Improvements in the diagnosis of acute kidney injury / V.Y. Melnikov, B. A. Molitoris // Saudi. J. Kidney Dis. Transpl. – 2008. – Vol.4, №19. – Р.537-544.
11. Association between increases in urinary neutrophil gelatinase-associated lipocalin and acute renal dysfunction after adult cardiac surgery/ G. Wagener, et al. // Anesthesiology. – 2006. – Vol.105. – P.485-491.
12. Mori, K. Neutrophil gelatinaseassociated lipocalin as the real-time indicator of active kidney damage / K. Mori, K. Nakao // Kidney Int. – 2007. – Vol.71. – P.967-970.
Статья опубликована в журнале "Вестник урологии". Номер №2/2014 стр. 3-12














Комментарии