Бердичевский В.Б.
«Федеральный центр нейрохирургии» г. Тюмени (Главный врач д.м.н., профессор Суфианов А.А.)
Введение. Хронический пиелонефрит является одним из наиболее распространенных заболеваний почек, при котором воспалительный процесс развивается не только как вторичный, на фоне органических обструктивных изменений в мочевыводящих путях, но и как первичное заболевание, характеризующееся функциональными расстройствами сердечного ритма и функции нижних мочевых путей. При этом, нарушения мочеиспускания играют важную роль в патогенезе микробно-воспалительного поражения почек и могут быть одним из решающих факторов в прогрессировании этого заболевания. Указанное состояние, как правило, сопровождается дискоординацией функций вегетативной нервной системы, обеспечивающей стабильную работу внутренних органов в условиях хронического микробно-воспалительного процесса в почках [1, 2, 3, 4 ].
В этой связи, чрезвычайно важным представляется комплексное исследование работы сердечно-сосудистой системы, подверженной нагрузкам в процессе реализации воспаления в почках и ритма мочеиспускания, оказывающего существенное влияние на формирования функциональных причин нарушения пассажа мочи. Именно поэтому лечение хронического необструктивного пиелонефрита должно включать в себя препараты, улучшающих функциональное показатели как сердечно-сосудистой системы, так и мочевыводящих путей. Комбинация их в комплексе с антибактериальной терапией с учетом чувствительности к ней бактериального компонента воспаления позволит улучшить результаты лечения больных с хроническим необструктивным пиелонефритом[5, 6, 7, 8].
Цель исследования. Изучить вариабельность ритма сердечной деятельности и ритма мочеиспускания у больных с хроническим пиелонефритом в фазе латентного воспалительного процесса и разработать методы их коррекции.
Материалы и методы. В настоящей работе представлены результаты клинического наблюдения и обследования 154 пациентов с хроническим необструктивным пиелонефритом. Как показали проведенные исследования, среди пациентов с впервые выявленным хроническим пиелонефритом было 83 женщины и 71 мужчина, средний возраст составил 40±5,7 лет. В ходе профилактического осмотра они предъявляли жалобы на периодические ноющие боли в поясничной области без четкой локализации, общее недомогание. Длительность субъективных ощущений заболевания составила 2,5±1,5 года. В анализах мочи выявлена значимая лейкоцитурия. После выполнения УЗИ почек, мочевого пузыря, консультации уролога, гинеколога и исключения урогинекологических причин воспаления в мочевыводящих путях, они были госпитализированы для углубленного обследования. Адренореактивность организма обследованных пациентов определяли по величине β-адренорецепции мембран эритроцитов (βАРМ) с использованием диагностического набора реактивов «АРМ-Агват» (ООО «Агат-Мед», г. Москва).Согласно условиям исследования, чем выше уровень катехоламинов в крови, тем выше значение показателя β-АРМ мембран эритроцитов отражающего их осморезистентность.
Суточное мониторирование ЭКГ (ХМ ЭКГ) выполняли, с помощью переносных суточных мониторов производства ОАО «Инкарт» (Санкт-Петербург) в течение 24 часов. Определяли средние за сутки показатели числа сердечных сокращений и временные параметры вариабельности сердечного ритма.
Специальные биохимические исследования клеточных мембран эритроцитов включали в себя: определение содержания суммарных фосфолипидов клеточных мембран эритроцитов (СФЛ) по реакции с малахитовым зеленым на неорганический фосфор и общего холестерина (ОХЛ) по методу Златкиса-Зака. Статистическая обработка результатов исследования проводилась на персональном компьютере с использованием статистического пакета прикладных программ SPSS 16.0 (SPSS Inc.) и STATISTICA 6.0. Для создания базы данных использовался редактор электронных таблиц «Microsoft Exel» 10.0 в соответ- ствии с правилами вариационной статистики. За критический уровень значимости при проверке статистических гипотез принимали р< 0,05с учетом числа степеней свободы.
Результаты и обсуждение. Исходно состояние всех пациентов расценено как удовлетворительное. В их анамнезе отсутствовали данные о ранее перенесенном остром и хроническом пиелонефрите. Заболевание развивалось исподволь и связать его возникновение с условиями труда и быта пациенты не смогли. Одновременно с появлением периодических ноющих болей в пояснице и недомогания у 124 (80,8%) пациентов отмечалось учащенное безболезненное необильное мочеиспускание. Восемь пациентов (6,1%) отметили количество мочеиспусканий менее 5в сутки, из них 6 были женщины. В 22 случаях (16,9%) нарушений мочеиспускания по мнению пациентов не наблюдалось.
Фактором беспокойства у пациентов с дисфункцией нижних мочевых путей (ДНМП) стало императивное расстройство мочеиспускания, которое характеризовалось появлением учащенного безболезненного мочеиспускания более 8 раз в сутки с элементами ургентности у 63 (45,2%) и различно выраженной инконтиненцией у 6 (3,8%) больных. Все пациенты с ДНМП осмотрены неврологом и у них были исключены нейрогенные причины. По данным экскреторной урографии расширения верхних мочевых путей и нарушений пассажа мочи не выявлено. Согласно рекомендациям Национального руководства по нефрологии (2009) и Европейской ассоциации урологов (2011), это позволило отнести впервые выявленный у наших пациентов хронический пиелонефрит к категории неосложненного. Однако у 28 (22,6%) пациентов в процессе выполнения микционной цистографии обнаружен кратковременный рефлюкс мочи в верхнюю треть мочеточника это пузырно-мочеточниковый рефлюкс I степени, которой по данным ряда исследователей имеет место более чем у 30% пациентов с неосложненным хроническим пиелонефритом.
В рамках настоящей работы нами проведено изучение сравнительных характеристик структурно-количественных показателей сердечного ритма у здоровых людей, пациентов с хроническим необструктивным пиелонефритом (ХрПН) без ДНМП и пациентов с ХрПН сочетающимся с ДНМП. Сравнительное исследование результатов ЭКГ и ХМ-ЭКГ показало, что отклонения по ЭКГ регистрируются у 26% пациентов с впервые выявленным хроническим неосложненным пиелонефритом, что в два раза чаще, чем в группе здоровых лиц. Холтеровское мониторирование ЭКГ увеличивало выявляемость этих отклонений во всех группах обследованных, что указывает на более высокую чувствительность суточного исследования функциональных показателей сердечной деятельности.
В результате проведенного анализа установлено, что дисрегуляция сердечного ритма у пациентов с хроническим неосложненным пиелонефритом относительно здоровых людей в целом наблюдается чаще. Преобладает синусовая брадикардия. При этом наличие дисфункции нижних мочевых путей увеличивает частоту этих отклонений. ХрПН сопровождается дисрегуляцией сердечного ритма характерной для повышения парасимптатического тонуса, о чем свидетельствуют наджелудочковые экстрасистолии, чаще регистрируемые на фоне ХрПН и ДНМП.
Исходя из результатов проведенного исследования, в рамках настоящей работы, пациенты с хроническим пиелонефритом в сочетании с дисфункцией нижних мочевых путей разделены на 2 группы.
В первую группу включен 61 пациент с впервые выявленным ХрПН и ДНМП, получавших двухнедельную стандартную этиологическую и патогенетическую терапию.
Во вторую группу включены 64 пациента с впервые выявленным ХрПН и ДНМП получавших аналогичную двухнедельную терапию в комплексе с одновременным приемом α1-адреноблокатора-Тамсулозинав дозе 4 мг один раз в сутки.
Три причины выбора именно этого препарата:
- α1-адреноблокаторы блокируют активацию α-адренорецепторов, вызывая стимулирующее влияние адреналина на β-адренорецепторы, опосредованно ускоряя ритм сердечных сокращений, нивелируя аритмический синдром и уменьшая артериальный вазоспазм
- α1-адреноблокаторы у больных с расстройством мочеиспускания за счет незначительной рефлекторной активации симпатической нервной системы, вызывают расслабление гладкой мускулатуры и улучшение кровоснабжения органов малого таза.
- α1-адреноблокаторы рекомендованы к клиническому применению для симптоматического лечения, как гиперрефлексии, так и гипорефлексии мочевого пузыря у пациентов с хроническим необструктивным пиелонефритом.
Оценку эффективности различных схем лечения проводили через 2 недели с учетом динамики субъективных жалоб и объективного функционального и лабораторного исследования.
Согласно комплексному изучению результатов дневников мочеиспускания, вегетативных вопросников и холтеровского мониторирования ЭКГ в группе здоровых лиц установлено, что большую часть времени (86%) здоровый человек проводит в условиях накопления, удержания и хранения мочи. Значительно меньшую часть времени (14%) , ощущая позыв на мочеиспускание, он занимается поиском условий для ее эвакуации, реализацией самого акта мочеиспускания, и социальному выходу из него для возвращения к текущим делам в условиях бессознательного накопления и хранения мочи.
Результаты спектрального анализа вариабельности вегетативной регуляции ритма сердца в процессе реализации акта мочеиспускания у здоровых людей представлены в таблице 1. Из данных таблицы видно, что в норме ощущение позыва к мочеиспусканию и пятиминутная подготовка к его реализации, протекают в условиях преобладания активности надсегментраного управления ВНС (VLF 64,6%.). На сегментарном уровне имело место доминирование парасимпатического отдела ВНС(HF20,4 и LF13,6%,LF/HF -0,6 усл. ед.). Сам процесс мочеиспускания осуществлялся в условиях снижения надсегментарной активности ВНС (VLF56,1% мс2.). При этом продолжалось нарастание активности сегментарного парасимпатического отдела ВНС (HL -36,4 и LF5,9%, LF/HF0,2 усл. ед.).
Таблица 1. Результаты спектрального анализа вариабельности сердечного ритма в процессе реализации мочеиспускания у здоровых людей(n-16)
| Параметры |
Позыв мс2% |
Мочеиспускание мс2% |
Завершение мс2% |
Удержание мс2% |
||||
| l | 2 | 3 | 4 | |||||
| ТР,мс2 | 33651198 | 100 | 1981192* | 100 | 18921101 | 100 | 29511151* | 100 |
| ULF,mc 2. | 48135 | 1,4 | 33129 | 1,6 | 2371105* | 12,6 | 147197 | 5 |
| VLF, мс2. | 21731124 | 64,6 | 11121114* | 56,1 | 14161121* | 74,8 | 4961115* | 16,9 |
| LF,mc2. | 4581120 | 13,6 | 116198* | 5,9 | 131196 | 6,9 | 16521128* | 55,9 |
| HL,mc2. | 6861118 | 20,4 | 7201127 | 36,4 | 108185* | 5,7 | 6561133* | 22,2 |
| LF/HF y.e. | 0,6 | 0,2 | 1,2 | 2,5 | ||||
| VLF/HFy.e | 3,2 | 1,5 | 13,1 | 0,8 | ||||
| ICy.e. | 3,8 | 1,7 | 14,3 | 3,3 | ||||
Примечание: * Р1-2< 0,05 различия статистически достоверны по сравнению с показателями в период позыва к мочеиспусканию;.Р2-3 < 0,05 – различия статистически достоверны по сравнению с показателями в период мочеиспускания; Р3-4 < 0,05 – различия статистически достоверны по сравнению с показателями в период завершения мочеиспускания.
Пятиминутный этап завершения акта мочеиспускания и определение дальнейшего плана поведения протекал в условиях существенного нарастания активности надсегментарного контроля ВНС(VLF74,8против56,1 %). Он так-же характеризовался сменой сегментарного доминирования парасимпатического отдела на симпатический отдел ВНС(LF -6,9%иHF5,7% , LF/HF 1.2 усл. ед.). Через час после опорожнения мочевого пузыря при суммарном доминировании активности сегментарного вегетативного контроля (VLF16,9%) процесс накопления мочи обеспечивался преимущественно симпатическим компонентом ВНС (LF55,9% иHF-22,2%, LF/HF 2,5. усл.ед.).
Продолжая изучать возможную взаимосвязь ритмов сердца и мочеиспускания, в рамках настоящего исследования проведена сравнительная холтеровская визуализация ритма сердца и накопительно-эвакуационных функций нижних мочевых путей у здоровых людей в зависимости от количества суточных мочеиспусканий. В качестве примера проведено сравнительное изучении результатов суточного мониторирования ЭКГ у здоровых лиц имеющих различный индивидуальный ритм мочеиспускания 4,-7, и -9 раз в сутки. (Рисунок 1.)
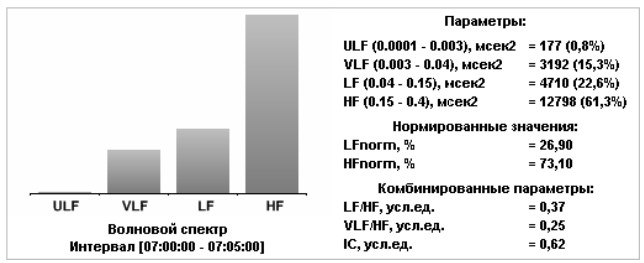
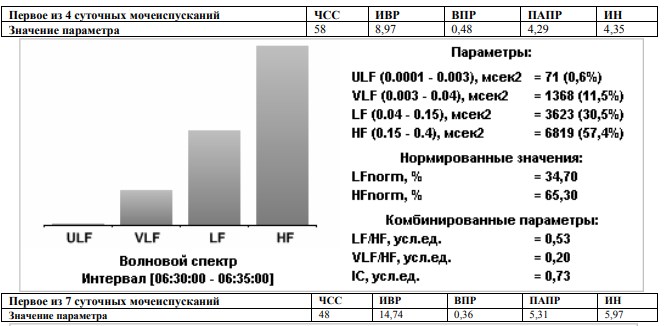
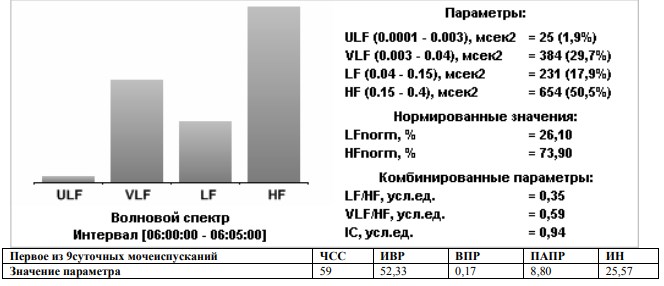
Рис. 1. Ритмологические особенности холтеровской визуализация ритма сердца и эвакуационных функций нижних мочевых путей у здоровых людей
В результате проведенного исследования установлено, что наименьший показатель надсегментарного контроля ВНС (ИН) имел место в процессе четырехразового суточного опорожнения мочевого пузыря, а наибольший при девятиразовом суточном опорожнении мочевого пузыря (4,355,97 25,57 у.е.).
Процесс опорожнения мочевого пузыря во всех случаях сопровождался доминированием сегментарного парасимпатического компонента ВНС –Hf norm (73,10 – 65,3073,90). Важно отметить, что мы не выявили гендерных особенностей в вегетативной регуляции функции внутренних органов у наших пациентов, что позволило исследования проводить в смешанных группах пациентов.
В рамках дальнейшего исследования нами проведено сравнительное изучение суточного спектрального анализа вариабельности сердечного ритма в норме и у пациентов на фоне ХрПН с ДНМП. Анализировалось раздельное влияние надсегментарного регулирования со стороны центров головного мозга (ULF иVLF), сегментарных центров спинного мозга (LF и HL) и мембранного (синаптического) восприятия сигнала по показателям β-АРМ эритроцитов. (Таблица 2.)
Таблица 2. Сравнительный спектральный анализ вариабельности сердечного ритма и β-АРМ эритроцитов в норме и на фоне ХрПН с ДНМП
| Уровни регуляции и параметры | Здоровые (п -30) мс2% | Хр.ПН с ДНМП(п-ЗО) мс2% | ||
| TFmc2 | 2544± 176 | 100 | 1822±101* | 100 |
| Головной мозг | ||||
| ULF мс2 | 54±44 | 2,1 | 196±102 | 10,8 |
| VLF, мс2 | 726±130 | 28,5 | 1252±215* | 68,6 |
| Спинной мозг | ||||
| LF,мс2.(симпатическая ВНС) | 951 ±310 | 37,5 | 85±22* | 4,7 |
| НЦмс2.(парасимпатическая ВНС) | 813±2 4 | 31,9 | 289±65* | 15,9 |
| Мембранная регуляция | ||||
| β-АРМусл. ед. | 12,4±3,5 | 6,2±2,0* | ||
Примечание: * р< 0,05 различия статистически достоверны по сравнению с нормой (критерий достоверности t–Стьюдента).
Из полученных данных видно, что, в целом, у здоровых людей в общей мощности спектра равномерно представлены все три уровня функционального контроля ВНС.
Суммарно он зависел в меньшей степени от надсегментарного (UVL2,1% плюс VLF28,5%),и в большей степени сегментарного центра регуляции ВНС. (LF-37,5% полюс HF-31,9%). Для здоровых людей характерна умеренная симпатикотония, адренореактивность мембран по критерию β-АРМ была в пределах физиологической нормы (12,4 усл. ед.),
У пациентов с впервые выявленным ХрПН с ДНМП в отличие от здоровых лиц при суточном мониторировании ЭКГ отмечен достоверно более низкий уровень общей мощности вегетативного спектра (ТF 2544236 и 1822 455 у.е., р< 0,05) с преобладанием надсегментарного уровня регулирования ВНС (VLF28,4 и 68,6%). Падение сегментарной активности было в большей степени характерно для симпатического отдела ВНС и в меньшей степени для парасимпатического отдела ВНС (LF4,7% иHF-15,9%). При этом, показательβ-АРМ, оставаясь в пределах физиологической нормы, снижался, что могло свидетельствовать о нарастании парасимпатического доминирования в мембранной регуляции внутренних органов.
Следующим этапом настоящей работы стала оценка клиникофункциональной и лабораторной эффективности стандартного лечения ХрПН с ДНМП и комбинированной терапии с включениемα1-адреноблокатора Тамсулозина. В результате проведенного исследования установлено, что в первой группе пациентов с ХрПН и ДНМП, получивших двухнедельную стандартную терапию, состояние клинико-лабораторной ремиссии к моменту окончания лечения, достигнуто у 46 (75,4%) пациентов. Сравнительный анализ структурно-количественных показателей сердечного ритма у пациентов с проявлениями его дисрегуляции после окончания стандартного лечения не выявил значимого улучшения ритмологических характеристик сердечной деятельности.
Во второй группе из 64 пациентов получавших двухнедельную стандартную терапию впервые выявленного ХрПН с ДНМПв комплексе с одновременным приемомα1-адреноблокатора Тамсулозина, состояние клиниколабораторной ремиссии к моменту окончания лечения достигнуто у 55 (85,9%) пациентов. Сравнительный анализ структурно-количественных показателей сердечного ритма у этих пациентов с ранее выявленной дисрегуляцией сердечного ритма, показал уменьшение проявлений аритмического синдрома более чем в 2 раза. Одновременно отмечено двухкратное сокращение проявлений мочепузырного рефлюкса при повторном выполнении микционной цистографии в этой группе пациентов.
Сравнительная клиническая характеристика проявлений дисфункции нижних мочевых путей у пациентов с впервые выявленным хроническим необструктивным пиелонефритом до и после различных схем терапии представлена в таблице 3.
Таблица 3. Сравнительная клиническая характеристика проявлений дисфункции нижних мочевых путей у пациентов с впервые выявленным хроническим пиелонефритом в стадии латентного течения
| Показатель | Здоровые п-30 | ХрПН до лечения п-61 | ХрПН лечение стандартное п-61 | ХрПН лечение комбинированное п63 |
| 1 | 2 | 3 | 4 | |
| Количество микций | 4,8 ± 1,1 | 11,2±1,2* | 10,9±1,1 | 7,8 ± 1,3* |
| Ночные микции | 0 | 2,0±0,5* | 1,4±1,0 | 0 |
| Инконтиненция | 0 | 0,7± 0,5* | 0,6± 0,3 | 0,5 ± 0,4 |
| Средний V мочи мл | 225,4± 43,3 | 128,2 ± 31,4* | 147,4±27,4 | 195,2± 29,4 |
| QoL, баллы | 0,7± 0,1 | 6,2 ± 1,0* | 4,4 ± 1,3 | 1,2 ± 1,4* |
Примечание: * -Р1-2< 0,05 различия статистически достоверны по сравнению со здоровыми;.Р2-3< 0,05 – различия статистически достоверны по сравнению с показателями до лечения; Р3-4< 0,05 – различия статистически достоверны по сравнению с показателями после стандартного лечения.
В результате сравнительного изучения дневников мочеиспускания у пациентов с впервые выявленным ХрПН и ДНМП до и после различных схем лечения установлено, что стандартное лечение значимо не уменьшало количества суточных и ночных микций. На фоне комбинированной терапии имело местодостоверное сокращение количества мочеиспусканий с купированием никтурии и пациенты однозначно повышали оценку качества жизни до вполне приемлемых показателей.
Сравнительный спектральный анализ вариабельности сердечного ритма и показателей β-АРМ эритроцитов у пациентов сХрПН с ДНМП на фоне проведения различных схем терапии показал, что, несмотря на положительную клинико-лабораторную динамику после стандартной терапии, продолжалось достоверное снижение уровня общей мощности вегетативного спектра (ТF 1822 101 и 1509172 у.е., р < 0,05)с сохранением надсегментарного уровня регулирования ВНС (VLF68,6 и 61,9%). Данные представлены в таблице 4.
Таблица 4. Сравнительный спектральный анализ вариабельности сердечного ритма и показателей β-АРМ эритроцитов у пациентов сХрПН с ДНМП на фоне проведения различных схем терапии
| Уровни регуляции и параметры | Хр.ПН с ДНМП до лечение мс2 % | Хр.ПН с ДНМП станд. лечение мс2% | Хр.ПН с ДНМП комб. Лечение мс2% | |||||
| 1 | 2 | 3 | ||||||
| TF мс2 | 1822± 101 | 1509± 172* | 2297± 140* | |||||
| Головной мозг | ||||||||
| ULFmc2. | 196±102 | 10,8 | 165±91 | 10 | 92±38 | 4,1 | ||
| VLF, мс2. | 1252±215 | 68,6 | 934±126 | 61,9 | 7911113 | 33,4 | ||
| Спинной мозг | ||||||||
| LF, мс2. (симпатическая ВНС) | 85±22 | 4,7 | 177±61 | 11,7 | 7161265* | 32,1 | ||
| HL, мс2. (парасимпатическая ВНС) | 289±65 | 15,9 | 233±65 | 15,5 | 6991143* | 30,4 | ||
| Периферическая мембранная адренорецепция | ||||||||
| Р-АРМусл. ед. | 6,2±4,5 | 9,814,9 | 20,514,5* | |||||
Примечание: * Р1-2< 0,05 различия статистически достоверны по сравнению с показателями до лечения; Р2-3 < 0,05 – различия статистически достоверны по сравнению с показателями после стандартной терапии.
Вместе с тем на сегментарном уровне при неизменном доминировании парасимпатического обеспечения функциональных потенций внутренних органов (HF-15,9% и 15,5%) наблюдалась достоверная активация симпатического звена ВНС (LF4,7% и 11,7%, р<0,05) с одновременной тенденцией к нарастанию показателейβ-АРМ эритроцитов(6,24,5 и9,84,9 усл. ед.).
У пациентов с ХрПН и ДНМП на фоне комбинированной терапии наблюдалась достоверное нарастание уровня общей мощности вегетативного спектра (ТF 1509±172 и 2297± 140 у.е., р<0,05) с падением надсегментарного контроля со стороны ВНС (VLF61,9 и 33,4%). Одновременно на сегментарном уровне достоверно нарастала активность как симпатической, так и парасимпатической регулирующей потенции ВНС со сменой полярности в сторону доминирования симпатического тонуса, характерного для показателей здоровых людей. (15,5% и 30,4% ,р<0,05). При этом на уровне органов «мишеней» наблюдалось достоверное нарастание показателей β-АРМ(9,8±4,9и 20,5 ±4,5усл. ед., р<0,05),косвенно указывающее на процесс стабилизации симпато-адреналового статуса этих больных.
На следующем этапе работы проведены специальные сравнительные биохимические исследования структурно-функциональной организации цитомембран эритроцитов у пациентов с впервые выявленным ХрПН и ДНМП по окончанию проведения различных схем терапии. Установлено, что в процессе реализации микробно-воспалительного процесса в почках имело место достоверное обеднение цитомембран фосфолипидами и нарастание содержания в них холестерина. При этом индекс микровязкости мембран увеличивался, что могло существенно влиять на реализацию их адренорецепции .Данные представлены в таблице 5.
Таблица 5. Показатели содержания фосфолипидов, холестерина и β-АРМ эритроцитов у пациентов с хроническим неосложненным пиелонефритом до и после различных схем терапии(Х ±m)
| Показатель | Здоровые (доноры) п=30 | ХрПН пиелонефрит до лечения п=30 | ХрПН стандартное лечение п=30 | ХрПН комбинированное лечение п=30 |
| 1 | 2 | 3 | 4 | |
| Фосфолипиды (мкмоль/мл) | 3,08±0,03 | 2,82±0,003* | 2,85±0,003 | 2,99±0,001* |
| Холестерин (мкмоль/мл) | 0,80±0,02 | 0,92±0,03* | 0,95±0,03 | 0,84±0,03* |
| ХС/ФЛ индекс вязкости | 0,25±0,02 | 0,31 ±0,02* | 0,33±0,04 | 0,27±0,03* |
| β-АРМ у.е. | 12,4±3,5 | 6,2±2,0* | 9,8±4,9 | 20,5±4,5* |
Примечание: * Р1-2< 0,05 различия статистически достоверны по сравнению со здоровыми; Р2-3 < 0,05 – различия статистически достоверны по сравнению с показателями до лечения; Р3-4 < 0,05 – различия статистически достоверны по сравнению с показателями после стандартного лечения.
На фоне проведения стандартного лечения наблюдалась тенденция к восстановлению фосфолипидного каркаса цитомембраны с обеднением ее холестерином, однако достоверного улучшения показателей микровязкости не происходило. При этом показатель β-АРМ эритроцитов повышался незначительно(6,2±2,0 усл. ед.и 9,8 ±4,9усл. ед.).
Включение в комбинированную терапию α1-адреноблокатора Тамсулазина сопровождалось достоверным улучшением микровязкости цитомембран, что могло способствовать более эффективной реакции клеток-мишеней на медиаторное воздействие, о чем косвенно свидетельствовало достоверное увеличение β-АРМ эритроцитов у этих больных (9,8 ±4,9 и 20,5±4,5 усл. ед., р<0,05).
Выводы. Следует отметить, что селективный модулятор негормональных рецепторов нижних мочевых путей α1-адреноблокторТамсулозин не обладает прямыми мембраностабилизирущими свойствами. Он избирательно и эффективно снижает проявления гиперактивности нижних мочевых путей, нивелируя проявления функционального обструктивного компонента (ПМР) поддерживающего хроническое течение микробно-воспалительного процесса в почках, что и было зафиксировано в результате специально проведенных сравнительных исследований ритмологических характеристик работы сердца, структурно-функционального состояния мембран эритроцитов и особенностей мочеиспускания в этой группе пациентов.
Литература
1. Глыбочко П.В., Аляев Ю.Г., Гаджиева З.К. Функциональное состояние нижних мочевых путей у пациенток с хроническим пиелонефритом. // Материалы пленума правления Российского общества урологов. Кисловодск, 2011, с.87-88.
2. Вегетативные расстройства. / под ред. А. М. Вейна. Медицинское информационное агентство.2000.752 с
3. Длусская И.Г. Адренорецепция мембран эритроцитов и сердечнососудистые заболевания / И.Г. Длусская, Р.И. Стрюк. // Молекулярная медицина. 2004. № 1. С. 25-26.
4. Крысова A.B. Роль альфаи бета-адренорецепторов в реализации способности адреналина изменять осмотическую резистентность эритроцитов небеременных женщин./ A.B. Крысова, A.A., В.И. Циркин //Вятский медицинский вестник. -2011. № 3-4. С. 8-13.
5. Calls J., Cases A., Lario S., et al. b-adrenergic receptor density and function in left ventricular hypertrophy in young essential hypertensives. J. Hum. Hypertens., 2000; Jan;14(1):17-21.
6. Fawzy A., Braun K., Lewis G.P. et. al. Doxazosin in the treatment of benign prostatic hyperplasia in normotensive patients: a multicenter study. J. Urol. 1995.-Vol. 154.-P. 105-106.
7. Ferdinand K.S. Update in pharmacologic treatment of hypertension. Cardiology Clinics/ 2001. №2. Vol. 19.-Р 211-215.
8. Sheridan J.F., Dobbs C., Brown D., and Zwilling B. Psychoneuroimmunology: stress effects on pathogenesis during infection. Clin. Microbiology rev., 1994, April; 7(2): 200-212.
Статья опубликована в журнале "Вестник урологии". Номер №4/2014 стр. 13-24










Комментарии