Сивков А.В., Трудов А.А., Голованов С.А., Кешишев Н.Г., Каприн А.Д.
Сведения об авторах:
- Сивков А.В. – к.м.н., заместитель директора по науке НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ AutorID 622663
- Трудов А.А. – врач-уролог НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России; Москва, Россия; РИНЦ AuthorID 787871
- Голованов С.А. – д.м.н., руководитель группы клинической лабораторной научно-лабораторного отдела НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава; Москва, Россия; РИНЦ AutorID 636685
- Кешишев Н.Г. – к.м.н., врач-уролог объединенной больницы с поликлиникой Управления делами Президента РФ; Москва, Россия; РИНЦ AuthorID 636185
- Каприн А.Д. – д.м.н., профессор, академик РАН, генеральный директор ФГБУ «НМИЦ радиологии» Минздрава России, директор МНИОИ имени П.А. Герцена, зав. кафедрой онкологии и рентгенорадиологии им. В.П. Харченко РУДН, главный внештатный онколог Минздрава России; Москва, Россия; РИНЦ AuthorID 96775
ВВЕДЕНИЕ
В развитых странах рак предстательной железы (РПЖ) является наиболее часто диагностируемым онкологическим заболеванием у мужчин. В последнее время в связи с улучшением ранней диагностики и повышением качества лечения пациенты с диагнозом РПЖ стали жить дольше [1].
В России в 2019 году состояло на учете в онкологических учреждениях 258 794 больных РПЖ. Впервые было выявлено 40 986 случаев, из них 5 и более лет наблюдали 43,0% пациентов с РПЖ. При этом, несмотря на положительную динамику выявления РПЖ на ранних стадиях, сохраняется относительно высокая доля распространенных форм заболевания. В 2019 году удельный вес РПЖ, выявленного в III и IV стадиях, из числа впервые выявленных случаев, составил 20,7% и 18,7%, соответственно [2]. Пациентам с местнораспространенным и метастатическим РПЖ назначают антиандрогенную депривационную терапию (АДТ). То есть, около 40% или более 100 000 больных РПЖ в нашей стране являются кандидатами на проведение АДТ.
Установлено, что мужчины, получающие АДТ, подвергаются риску развития побочных эффектов, в том числе остеопороза. Длительная АДТ приводит к снижению минеральной плотности костной ткани (МПКТ) и увеличивает риск переломов, что является важной медицинской и социальной проблемой [3-6].
Исследования показали, что у части пациентов потеря костной ткани, вследствие АДТ, развивается на ранних этапах лечения. Проспективное исследование скорости потери костной массы после начала АДТ у мужчин с РПЖ продемонстрировало наиболее значимое снижение МПКТ в первые 12 месяцев после начала АДТ, что подчеркивает важность ранних профилактических мероприятий. Выявлено, что скорость потери костной массы у больных РПЖ на фоне АДТ была в 5- 10 раз выше, чем у здоровых мужчин соответствующего возраста, как и у пациентов с РПЖ и нормальным уровнем тестостерона и эстрогенов [7].
Показательно, что еще до начала АДТ у мужчин с распространенным РПЖ регистрировали более высокую частоту остеопороза и остеопении, по сравнению с контрольной группой, сопоставимой по возрасту [8]. Так, из 174 пациентов с распространенным РПЖ, до начала АДТ остеопороз наблюдали у 42% (Т-критерий < – 2.5) и остеопению – у 37% (Т-критерий от – 1 до – 2,4), в сравнении с 27% остеопороза в контрольной группе соответствующего возраста (p = 0,022).
Пагубное воздействие АДТ на состояние костной ткани непосредственно связано с длительностью андрогенной депривации. Прогрессирующее снижение МПКТ наблюдали при длительном, до 10 лет, применении АДТ, что было более выражено при непрерывной АДТ или хирургической кастрации, по сравнению с интермиттирующей гормональной терапией [9].
V.B. Shahinian и соавт. оценили результаты наблюдения 50 613 пациентов с РПЖ, проживших не менее 5 лет с момента постановки диагноза. Переломы костей были зарегистрированы у 19,4% больных на фоне AДT, против 12,6% (p < 0,001) среди не получавших такого лечения [10].
Популяционное когортное исследование показало, что у мужчин с высоким исходным риском развития костных осложнений после начала АДТ возникало больше переломов [11]. Существует обратная зависимость между риском перелома и МПКТ с примерно двукратным увеличением риска перелома с каждым снижением стандартного отклонения МПКТ [12, 13]. Кроме того, остеопоротические переломы у мужчин с РПЖ коррелируют с плохими исходами выживаемости [11, 14].
Переломы, связанные с остеопорозом, имеют важное социально-экономическое значение. E. Hernlund и соавт. заявили, что в 2010 году в Евросоюзе было зарегистрировано 3,5 миллиона новых переломов на фоне остеопороза, а экономические затраты оценили в 37 млрд евро. Ожидается, что к 2025 году этот показатель и затраты возрастут еще на 25% [15].
Клиническое руководство NICE (National Institute for Health and Care Excellence) в Великобритании рекомендует учитывать риск переломов у всех мужчин, получающих AДT и проводить лечение всем пациентам с выявленным остеопорозом [16]. Аналогичным образом рекомендации Европейской ассоциации урологов (EAU), Европейского общества радиотерапии и онкологии (ESTRO) и Международного общества гериатрической онкологии (SIOG) говорят о том, что оценку МПКТ необходимо обязательно проводить до начала долгосрочной AДT [17].
Больным РПЖ для лечения остеопороза, развившегося на фоне АДТ, рекомендуют применение золедроновой кислоты (ЗК), ингибитора RANKL деносумаба и алендроната натрия [18-20]. При этом, систематический обзор 12 клинических исследований показал, что применение препаратов кальция и витамина D для профилактики остеопороза у больных РПЖ получающих АДТ, недостаточно для предотвращения потери МПКТ [21]. Схема развития костных нарушений на фоне АДТ и точки приложения препаратов, применяемых для коррекции этих нарушений, представлены на рисунке 1.
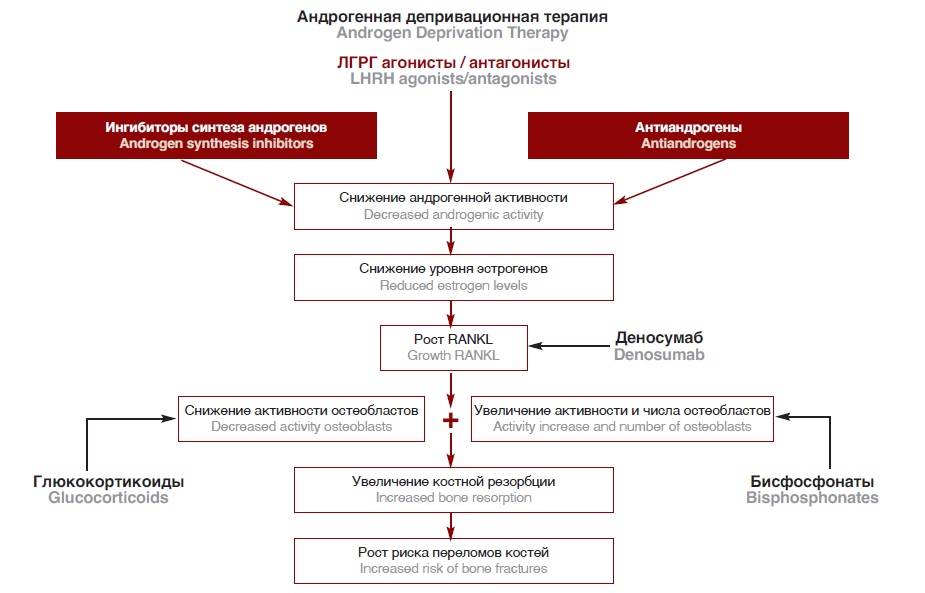
Рис. 1. Схема развития костных нарушений на фоне АДТ и точки приложения препаратов, применяемых для их коррекции [18]
Fig. 1. Scheme of the development of bone disorders against the background of ADT and points of application of drugs used for their correction [18]
Эффективность бисфосфонатов в снижении потери МПКТ у мужчин с РПЖ, получающих АДТ, изучена в нескольких рандомизированных контролируемых исследованиях.
Серией небольших работ продемонстрировано влияние бисфосфонатов на уменьшение потери МПКТ у больных РПЖ получающих АДТ. Однако важно отметить, что разнообразие дизайна исследований, изучаемых препаратов и гетерогенность популяции, делает сложным прямое сравнение их результатов. Кроме того, основной конечной точкой в большинстве этих исследований было изменение МПКТ, а не частота переломов, что имеет большее клиническое значение [22-25].
В 2012 г. Serpa Neto и соавт. провели метаанализ 15 рандомизированных контролируемых исследований применения бисфосфонатов у больных РПЖ получающих АДТ. Авторы заключили, что применение бисфосфонатов оказало существенное влияние на профилактику переломов (Risk Ratio 0,80; p = 0,005) и остеопороза (Risk Ratio 0,39; p < 0,00001), не вызвав никаких серьезных побочных эффектов [26].
Опубликовано относительно немного работ, изучавших эффективность деносумаба на МПКТ и риск переломов у пациентов с неметастатическим РПЖ, получавших АДТ. Показательным является крупное двойное слепое клиническое исследование, проведенное M.R. Smith и соавт., в котором было рандомизировано 1468 пациентов, получавших или 6-месячные подкожные инъекции деносумаба (60 мг) в течение 3 лет или плацебо. Результаты продемонстрировали значительное увеличение МПКТ поясничного отдела позвоночника через 24 месяца в группе деносумаба по сравнению с плацебо (+ 5,6% против − 1,0%, р < 0,001), с уменьшением частоты новых переломов позвонков через 36 месяцев (1,5% против 3,9% с плацебо, HR 0,38; 95% доверительный интервал от 0,19 до 0,78; р = 0,006). Эти положительные эффекты наблюдали уже через 1 месяц и сохранялись в течение 36 месяцев [27].
Однако наиболее часто для профилактики остеопороза на фоне АДТ применяют препараты золедроновой кислоты. Одним из самых крупных явилось исследование RADAR (TROG 03.04 Randomised Androgen Deprivation and Radiotherapy), включившее 1071 пациента с РПЖ (стадия Т2b-4 или T2a при Gleason > 7, ПСА > 10), подлежавших лучевому лечению, которые были разделены на 4 группы, в зависимости от проводимой лекарственной терапии. Две из них получили только АДТ, причем одна – только 6-месячный курс неоадъювантного лечения лейпрорелином, а другая – еще и дополнительный курс адъювантной терапии лейпрорелином на протяжении 12 месяцев. Оставшимся двум группам назначили такие же курсы АДТ, но помимо этого, еще и лечение ЗК (4 мг в/в один раз в 3 месяца). Среднее время наблюдения составило 5,6 лет. В течение 3-х лет инциденты с переломами грудного и поясничного отделов позвоночника наблюдали всего у 14,6% пациентов. Причем корреляция продолжительности АДТ и факта терапии ЗК оказалась близка к достоверной. Мультивариантный анализ показал, что назначение ЗК недостоверно снижало вероятность перелома позвоночника в течение 3-х лет, по сравнению с лицами не принимавшими бисфосфонаты. Кроме того, на избранной группе из 222 пациентов с использованием метода DEXA (двухэнергетическая рентгеновская абсорбциометрическая денситометрия) было продемонстрировано, что длительность АДТ влияет на степень потери МПКТ. У больных, получавших АДТ в течение 6 месяцев, через 2 года отмечено снижение МПКТ бедра, в среднем, на 2,6% (p < 0,001), хотя некоторое восстановление было очевидно через 4 года, при том, что общая потеря на 1,7% сохранилась (p = 0,001). Через 2 года снижение МПКТ у пациентов, получивших дополнительно 12 месяцев АДТ, составило 4,1% (p < 0,001), а через еще 2 года – снижение составило 3,7% относительно исходного показателя (p < 0,001). Восемнадцати месяцев применения ЗК было достаточно для предотвращения потерь МПКТ, вызванных АДТ в обеих группах. По сравнению с исходным уровнем, средняя МПКТ тазобедренного сустава увеличилась через 2 года на 0,6% (p = 0,18) и до 1,8% через 4 года (p = 0,003) в группе пациентов получивших АДТ 6 месяцев и до 0,5% (p = 0,41) и 1,2% (p = 0,09) в группе дополнительной АДТ 12 месяцев. При этом, не было выявлено достоверной разницы между группами в частоте переломов позвонков, что исследователи связали с недостаточным объемом выборки и длительностью наблюдения [28].
Таким образом, исследования показали эффективность терапии остеопороза бисфосфонатами, в особенности ЗК, с целью поддержания или увеличения МПКТ у пациентов с АДТ [29]. В частности, терапия ЗК способна существенно увеличить МПКТ даже при однократном внутривенном введении [23].
В настоящем исследовании была выбрана ЗК, как средство для предупреждения и терапии остеопороза при проведении АДТ, с учетом, в том числе, наличия отечественных импортзамещающих препаратов. При этом оценивали эффективность ЗК в предотвращении и восстановлении АДТ-индуцированной потери костной массы.
МАТЕРИАЛЫ И МЕТОДЫ
Нами обследовано 45 мужчин в возрасте от 54 до 81 года с морфологически верифицированным РПЖ (стадии T2-4 N0-1 M0), более чем за 6 месяцев до включения в исследование перенесших хирургическую кастрацию или непрерывно получавших терапию аналогами гонадотропин-рилизинг-гормона (ГнРГ).
В исследование не включали пациентов, у которых до начала АДТ имелись метастазы РПЖ, остеопоротические переломы костей в анамнезе, страдающих хронической почечной недостаточностью или принимавших бисфосфонаты.
Всем пациентам провели обследование, включавшее: сбор анамнеза, измерение роста, веса, расчет индекса массы тела, общий анализ крови, общий анализ мочи, анализ крови на уровень креатинина, простатспецифический антиген (ПСА) и тестостерон, исследование кальция в крови и моче, определение в крови основного фактора костной резорбции – CTХ-1, остеоденситометрию пяточной кости и остеосцинтиграфию с 99Tc (по показаниям).
В качестве основного маркера состояния костной резорбции, на основании анализа научной литературы, был выбран уровень фактора СТХ-1 в крови, который представляет собой концевой телопептид коллагена 1 типа (C-terminal telopeptide cross-laps) и является наиболее значимым продуктом деградации коллагена в сыворотке крови и моче [29].
Изменения метаболизма костной ткани приводят к изменению концентраций CTX-1 в сыворотке крови и моче [30]. Повышение уровня CTX-1 выше возрастной нормы в плазме крови указывает на усиление резорбции и разрушения костной ткани пациентов с РПЖ, получающих антиандрогенную терапию [31]. Доказано, что уровень CTX-1 существенно снижается на фоне антирезорбтивной терапии [32]. К особенностям CTX-1 относятся его циркадные изменения, поэтому взятие образца для анализа выполняют утром натощак [33]. Некоторые авторы указывают на CTX-1, как маркер выбора при оценке костной резорбции [29, 34].
Наиболее распространенным методом оценки МПКТ является DEXA – двухэнергетическая рентгеновская абсорбциометрия (денситометрия). Как правило, измеряют конкретные области скелета, включая проксимальный отдел бедренной кости или шейку бедренной кости и поясничный отдел позвоночника. Результаты измерений обычно представляют с помощью T-критерия в виде Т – шкалы, включающей величины стандартного отклонения (S) от среднего значения МПКТ для возраста, в котором в данном участке скелета МПКТ достигает максимума: остеопороз (< – 2,5); остеопения (от – 2,5 до – 1); норма (от -1 до +2,5) [35, 36].
В настоящем исследовании применяли другой известный метод неинвазивной скрининг-оценки МПКТ на основе двухдиапазонной рентгеновской денситометрии пяточной кости с лазерным определением области обследования (DXL) с использованием аппарата CALSCAN (Demetech AB, Sweden) и программного обеспечения DXL Calscan Workstation. В данном методе система в автоматическом режиме проводит цифровую калибровку перед каждым исследованием, что повышает точность результатов, и автоматически определяет показатели МПКТ. Время сканирования составляет менее 1 минуты. В ряде исследований была показана сопоставимость результатов, получаемых при использовании технологий DEXA и DXL при диагностике остеопороза и остеопении [37, 38].
Определение CTX-1 крови и МПКТ проводили ежемесячно.
В зависимости от характера антирезорбтивной терапии (АРТ) пациенты были рандомизированы на группы по 15 человек в каждой, получавших внутривенную инфузию ЗК в дозе 4 мг в начале исследования и через 3 месяца лечения (группа 1), по 2 мг в том же режиме (группа 2) и контрольную группу (3), в которой пациенты не получали лечения ЗК. Использовали препарат Резорба (АО «Фарм-Синтез», Россия). Длительность наблюдения составила 6 месяцев.
Статистическая обработка результатов исследований включала 2 этапа: описательная статистика и оценка значимости различий между группами пациентов, получавших терапию препаратом ЗК, в сравнении с контрольной группой. Описательную статистику выполнили путем анализа базы данных в программе Microsoft Office Excel. Она включала определение характеристик распределения исследуемых переменных соответствующим представлением в таблицах следующих параметров: выборочного среднего (М), стандартного отклонения (S), максимального (макс) и минимального (мин) значения для каждой количественной переменной. Для номинальных переменных указывали абсолютную частоту встречаемости признака и его процентную долю в выборке. Статистический анализ значимости различий проводили с помощью программного обеспечения SPSS-17. Оценка значимости различий включала: анализ исходных данных с целью проверки их однородности (отсутствие различий), между 3 группами (1 группа – терапия препаратом ЗК, 4 мг; 2 группа – терапия ЗК, 2 мг; 3 группа – контроль) и оценку динамики параметров оценки терапевтической эффективности для 3 временных точек (исходные значения, после 3 месяцев и после 6 месяцев АРТ). Учитывая, что оценку значимости различий проводили не только для 2-х значений переменных, но и для 3-х значений (3 группы и 3 временные точки) использовали статистические критерии различий для множественных выборок, а для оценки попарных различий показателей между группами и их динамики во времени выполняли апостериорный post hoc анализ. Для статистического анализа различий исследуемых параметров и их изменений использовали следующие критерии: оценка нормальности распределения – критерий Шапиро-Уилка; для количественных нормально распределенных переменных – t-критерии Стьюдента для 2-х независимых или связанных выборок; для 3-х независимых или связанных выборок – соответственно дисперсионные критерии АНОВА и АНОВА-П, при выявлении этими критериями факта различий в выборках для оценки попарных различий использовали метод Тьюки; для 2-х независимых или связанных выборок количественных переменных, имеющих отличные от нормального распределения, соответственно, использовали непараметрические критерии Манна-Уитни или Вилкоксона; для 3-х независимых выборок использовали непараметрический критерий Краскела-Уоллиса, при выявлении этим критерием факта наличия различий для оценки попарных различий использовали критерий Манна-Уитни; для 3-х связанных выборок использовали непараметрический критерий Фридмана и при проведении попарных сравнений – критерий Вилкоксона; для номинальных частотных переменных при 2-х или 3-х признаках – критерий χ2 Пирсона для 4-польных или многопольных таблиц сопряженности.
РЕЗУЛЬТАТЫ
Исходные данные пациентов
Возраст пациентов колебался от 54 лет до 81 года. Длительность предшествовавшей антиандрогенной терапии агонистами ГнРГ или максимальной андрогенной блокадой (МАБ) – от 6 до 24 месяцев. Исходные показатели ПСА колебались в пределах от 0,08 до 3,96 нг/мл, а уровень тестостерона сыворотки крови – от 0,1 до 0,78 нг/мл. Достоверных различий между группами по исходным показателям выявлено не было, р > 0,05 (табл. 1).
Таблица 1. Исходные данные пациентов
Table 1. Baseline patient data
| Показатели Parameters |
Общие данные, n = 45 All data, n = 45 |
Группа 1 ЗК (4 мг) (n = 15) Group I ZA (4 mg) (n = 15) |
Группа 2 ЗК (2 мг) n = 15 Group II ZA (4 mg) n=15 |
Группа 3 Контроль n = 15 Group 1 Control n=15 |
Критерий p p criteria |
|---|---|---|---|---|---|
| Возраст, лет., М ± S (мин; макс) Age, years., M ± S (min; max) |
67 ± 7 (54; 81) | 69 ± 7 (54; 81) | 66 ± 6 (56; 77) | 67 ± 6 (55; 79) | АНОВА, р = 0,34 |
| Длительность АДТ, мес. М ± S (мин; макс) ADT Duration, months M ± S (min; max) |
14 ± 5 (6; 24) | 15 ± 4 (7; 24) | 13 ± 4 (6; 22) | 13 ± 5 (7; 22) | АНОВА, р = 0,68 |
| АДТ агонистом ГнРГ, число пациентов, (%) ADT GnRH agonist, number of patients, (%) |
23 (51%) | 8 (53%) | 8 (53%) | 7 (47%) | X2 Пирсона, р = 0,92 |
| АДТ МАБ, число пациентов, (%) ADT MAB,number of patients, (%) |
22 (49%) | 7 (47%) | 7 (47%) | 8 (53%) | |
| ПСА (нг/мл) М ± S (мин; макс) PSA (ng/ml) M ± S (min; max) |
1,16 ± 0,93 (0,08; 3,96) |
1,19 ± 1,03 (0,16; 3,96) |
1,03 ± 0,65 (0,08; 2,57) |
1,25 ± 0,73 (0,10; 3,01) |
Кр-Уол, р = 0,85 |
| Тестостерон, нг/мл М ± S (мин; макс) Testosterone, ng/ml M ± S (min; max) |
0,31 ± 0,15 (0,10; 0,78) |
0,27 ± 0,15 (0,10; 0,78) |
0,33 ± 0,12 (0,14; 0,59) |
0,29 ± 0,16 (0,11; 0,64) |
Кр-Уол, р = 0,95 |
Важным условием адекватного анализа данных явилось отсутствие межгрупповых различий показателей, использованных для сравнительной оценки ответов пациентов на АРТ (табл. 2). Не было выявлено достоверных различий между группами по показателю МПКТ (Тшкала денситометрии), числу пациентов с признаками остеопороза или остеопении и нормальными значениями МПКТ. Также не установлено различий в показателях CTX-1. Из 45 пациентов, включенных в исследование, у 69% были выявлены повышенные значения СТХ-1.
Таблица 2. Исходные значения показателей, использованных для оценки эффективности антирезорбтивной терапии
Table 2. Initial values of indicators used to assess the effectiveness of antiresorptive therapy
| Показатели Parameters |
Общие данные, n = 45 All data, n = 45 |
Группа 1 ЗК (4 мг) (n = 15) Group I ZA (4 mg) (n = 15) |
Группа 2 ЗК (2 мг) n = 15 Group II ZA (4 mg) n=15 |
Группа 3 Контроль n = 15 Group 1 Control n=15 |
Критерий p p criteria |
|---|---|---|---|---|---|
| МПКТ, Т - шкала BMD, T - scale | -2,0 ± 0,8 (-3,5; -0,5) |
-2,0 ± 0,8 (-3,4; -0,7) |
-2,0 ± 0,7 (-3,5; -0,6) |
-1,9 ± 0,8 (-3,2; -0,5) |
АНОВА, р = 0,83 |
| Остеопороз, число пациентов, (%) Osteoporosis, number of patients, (%) |
11 (24%) | 4 (27%) | 3 (20%) | 4 (27%) | X2 Пирсона, р = 0,95 |
| Остеопения, число пациентов, (%) Osteopenia, number of patients, (%) |
31 (69%) | 10 (67%) | 11 (74%) | 10 (67%) | |
| Норма, число пациентов, (%) Norm, number of patients, (%) |
3 (7%) | 1 (6%) | 1 (6%) | 1 (6%) | |
| СТХ-1, нг/мл, М ± S (мин; макс) CTX-1, ng/ml, M ± S (min; max) |
0,834 ± 0,257 (0,578; 1,712) |
0,845 ± 0,179 (0,596; 1,671) |
0,826 ± 0,258 (0,578; 1,712) |
0,831 ± 0,222 (0,612; 1,682) |
АНОВА, р = 0,88 |
| СТХ-1 норма, число пациентов, (%) CTX-1 norm, number of patients, (%) |
14 (31%) | 5 (33%) | 5 (33%) | 4 (27%) | X2 Пирсона, р = 0,9 |
| СТХ-1 выше нормы, число пациентов, (%) CTX-1 above normal, number of patients, (%) |
31 (69%) | 10 (67%) | 10 (67%) | 11 (73%) |
При р < 0,05 – различия значимы At p < 0.05, the differences are significant
ЭФФЕКТИВНОСТЬ АНТИРЕЗОРБТИВНОЙ ТЕРАПИИ
Изменение CXT-1
Важным показателем эффективности АРТ является ее влияние на маркер костной резорбции СТХ-1. Исследование продемонстрировало статистически достоверное снижение уровне CTX-1 в группах, получавших ЗК в дозах 4 мг и 2 мг, как через 3, так и через 6 месяцев лечения (табл. 3).
Таблица 3. Сравнительная оценка динамики СТХ-1 в процессе антирезорбтивной терапии
Table 3. Comparative assessment of CTX-1 dynamics during antiresorptive therapy
| Группы Groups |
СТХ-1, нг/мл, М ± S (мин; макс) CTX-1, ng/ml, M ± S (min; max) |
Критерий p p criteria |
||
|---|---|---|---|---|
| Исходно Initial level |
3 месяца 3 months |
6 месяцев 6 months |
||
| Группа 1, ЗК (4 мг) n = 15 Group 1, ZA (4 mg) n = 15 |
0,845 ± 0,247 (0,596; ,671) |
0,215 ± 0,124 (0,084; 0,395) |
0,199 ± 0,086 (0,098; 0,351) |
F-test, р < 0,001*: W - критерий: р3-и = 0,001* р6-и < 0,001* р6-3 = 0,54 |
| Группа 2, ЗК (2 мг) n = 15 Group 2, ZA (2 mg) n = 15 |
0,826 ± 0,266 (0,578; 1,712) |
0,387 ± 0,138 (0,159; 0,616) |
0,322 ± 0,116 (0,153; 0,591) |
F-test, р < 0,001*: W - критерий: р3-и = 0,001* р6-и < 0,001* р6-3 = 0,69 |
| Группа 3, Контроль, n = 15 Group 3, Control, n = 15 |
0,831 ± 0,258 (0,612; 1,682) |
0,841 ± 0,312 (0,644; 1,748) |
0,882 ± 0,297 (0,668; 1,753) |
F-test, p = 0,31 |
| Критерий, p p criteria |
Кр-Уол, р = 0,001* M-U критерий: р1-2 = 0,001*; р1-3 < 0,001*; р2-3 = 0,001* |
Кр-Уол, р = 0,001* M-U критерий: р1-2 = 0,005*; р1-3 < 0,001*; р2-3 < 0,001* |
— | |
*р < 0,05 – различия значимы p < 0.05, the differences are significant
Уменьшение этого маркера среди пациентов, которым вводили бóльшую дозу ЗК, было также существенно больше, по сравнению группой, получавшей 2 мг препарата. Так, в группе 1 отметили снижение уровней CTX-1 через 3 и 6 месяцев в среднем на 74% и 76% соответственно. В группе 2 в эти же сроки уменьшение уровней CTX-1 в среднем составило 52% и 62% соответственно. Статистически значимого изменения показателя CTX-1 в контрольной группе не выявлено (табл. 4).
Таблица 4. Процентное изменение уровней СТХ-1 к 3 и 6 месяцам АРТ
Table 4. Percent change in CTX-1 levels at 3 and 6 months of ART
| № | Группы Groups |
Изменение СТХ-1 в % от исходного уровня, нг/мл, М ± S (мин; макс) Change CTX-1 in % of initial level, M ± S (min; max) |
Критерий p p criteria |
|
|---|---|---|---|---|
| 3 месяца 3 months |
6 месяцев 6 months |
|||
| 1 | Группа 1, ЗК (4 мг) n = 15 Group 1, ZA (4 mg) n=15 |
-74,0 ± 17,1 (-89,4; -53,3) |
-75,5 ± 12,7 (-87,1; -52,0) |
t - пар, p = 0,42 |
| 2 | Группа 2, ЗК (2 мг) n = 15 Group 2, ZA (2 mg) n=15 |
-52,2 ± 14,9 (-77,4; -35,5) |
-62,2 ± 13,7 (-81,8; -46,9) |
t - пар, p < 0,001* |
| 3 | Группа 3, Контроль, n = 15 Group 3, Control, n=15 |
-3,6 ± 9,2 (-22,7; 10,8) |
4,5 ± 9,7 (-14,6; 22,9) |
t - пар, p = 0,06 |
| Критерий, p p criteria |
АНОВА-Т: р1-2 = 0,001*; р1-3 < 0,001*; р2-3 < 0,001* |
АНОВА-Т: р1-2 = 0,005*; р1-3 < 0,001*; р2-3 < 0,001* |
— | |
* различия значимы the differences are significant
Характерно, что значительное уменьшение уровней CTX-1 с достижением «плато» наблюдали уже после первого месяца терапии в группах 1 и 2, в отличие от контрольной группы (рис. 2).
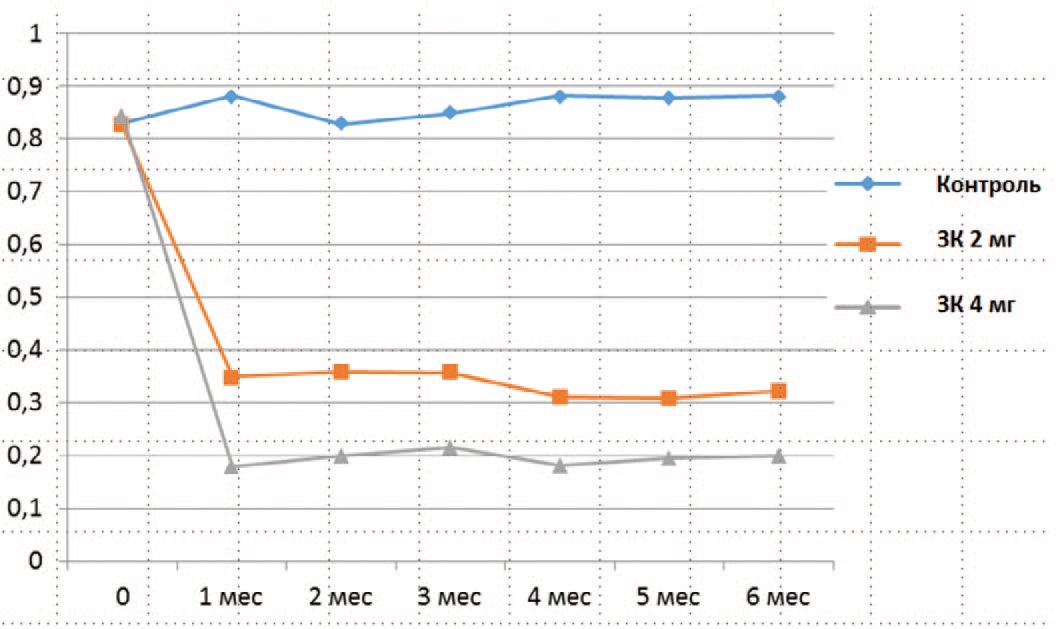
Рис. 2. Динамика уровня СТХ-1 (нг/мл) при АРТ разными дозами ЗК, в сравнении с контролем
Fig. 2. Dynamics of the level of CTX-1 (ng/ml) in ART with different doses of ZA, in comparison with the control
Согласно существующим положениям, «полным ответом» на АРТ считают достижение возрастной нормы СТХ-1, что обычно соответствует снижению СТХ-1 ≥ 50% [39]. В описываемом исследовании уже к 3 месяцу 13 из 15 пациентов, получавших 4 мг препарата, достигли 50% и более снижения СТХ-1, а к 6 месяцу все 15 больных достигли «полного ответа». Пациенты, получавшие 2 мг препарата, также ответили на АРТ и к 6 месяцам 13 из 15 достигли «полного ответа» (табл. 5). Следует отметить, что в контрольной группе снижение СТХ-1 к 6 месяцам наблюдения не было отмечено ни у одного из пациентов.
Таблица 5. Абсолютное число и доля пациентов (в %) со снижением СТХ-1 на 50% и более к 3 и 6 месяцам АРТ
Table 5. Absolute number and proportion of patients (in %) with 50% or more decrease in CTX-1 after 3 and 6 months of ART
| № | Группы Groups |
Изменение СТХ-1 в % от исходного уровня, нг/мл, М ± S (мин; макс) Change CTX-1 in % of initial level, M ± S (min; max) |
Критерий p p criteria |
|
|---|---|---|---|---|
| 3 месяца 3 months |
6 месяцев 6 months |
|||
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n = 15 |
-74,0 ± 17,1 (-89,4; -53,3) |
-75,5 ± 12,7 (-87,1; -52,0) |
X2 Пирсона, p = 0,543 |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n = 15 |
-52,2 ± 14,9 (-77,4; -35,5) |
-62,2 ± 13,7 (-81,8; -46,9) |
X2 Пирсона, p = 0,046* |
| Критерий, p p criteria |
X2 Пирсона, p = 0,046* |
X2 Пирсона, p = 0,543 |
— | |
*р < 0,05 – различия значимы p < 0.05, the differences are significant
Изменение МПКТ
Как видно из таблицы 6, исходные значения МПКТ в 3-х исследуемых группах не отличались. К 3-му месяцу исследования показатель МПКТ значимо повысился только у пациентов 1 группы (ЗК 4 мг). У пациентов 2 группы (ЗК 2 мг) – этот показатель достоверно повысился к 6-му месяцу лечения. При этом, у пациентов 1 группы через 6 месяцев показатель МПКТ достиг более высоких значений, чем у пациентов 2 группы. В противоположность росту показателя МПКТ под влиянием АРТ в группе контроля к 6-му месяцу наблюдения отмечено его значимое снижение, что указывает на дальнейшее ухудшение состояния костной ткани у пациентов, получающих АДТ без протекторной антирезорбтивной терапии.
Таблица 6. Влияние антирезорбтивной терапии на показатели МПКТ
Table 6. Effect of antiresorptive therapy on BMD
| № | Группы Groups |
Значения Т-критерия, М ± S (мин; макс) T-test values, M ± S (min; max) |
Критерий p p criteria |
||
|---|---|---|---|---|---|
| Исходно Initial level |
3 месяца 3 months |
6 месяцев 6 months |
|||
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n = 15 |
-2,0 ± 0,8 (-3,4; -0,7) |
-1,8 ± 0,8 (-3,3; -0,6) |
-1,6 ± 0,8 (-3,2; -0,5) |
F-test, р < 0,001*: W - критерий: р3-и = 0,01* р6-и = 0,001* р6-3 = 0,02* |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n=15 |
-2,0 ± 0,7 (-3,5; -0,6) |
-1,9 ± 0,7 (-3,4; -0,6) |
-1,8 ± 0,7 (-3,4; -0,6) |
F-test, р < 0,001*: W - критерий: р3-и = 0,33 р6-и = 0,01* р6-3 = 0,03* |
| 3 | Контроль, n = 15 Control, n=15 |
-1,9 ± 0,8 (-3,3; -0,5) |
-2,0 ± 0,8 (-3,3; -0,6) |
-2,1 ± 0,7 (-3,4; -0,8) |
F-test, р < 0,001*: W - критерий: р3-и = 0,42 р6-и = 0,002* р6-3 = 0,019* |
| Критерий, p p criteria |
Кр-Уол, р = 0,82 |
Кр-Уол, р = 0,044* M-U критерий: р1-3 = 0,015*; р2-3 < 0,06*; р1-2 < 0,04* |
— | ||
*р < 0,05 – различия значимы p < 0.05, the differences are significant
Наиболее выраженные и заметные различия динамики Т-критерия между исследуемыми группами пациентов были получены при сравнительном анализе изменений этого показателя относительно исходного уровня. Так, у пациентов 1 группы уже к 3 месяцу повышение показателя МПКТ более чем в 2 раза превысило рост МПКТ в группе 2. Эта тенденция сохранилась и к 6-му месяцу исследования. В группе же контроля уже к 3 месяцу отметили снижение показателя МПКТ относительно исходного уровня, а к 6 месяцу это снижение оказалось еще более выраженным (табл. 7 и рис. 3).
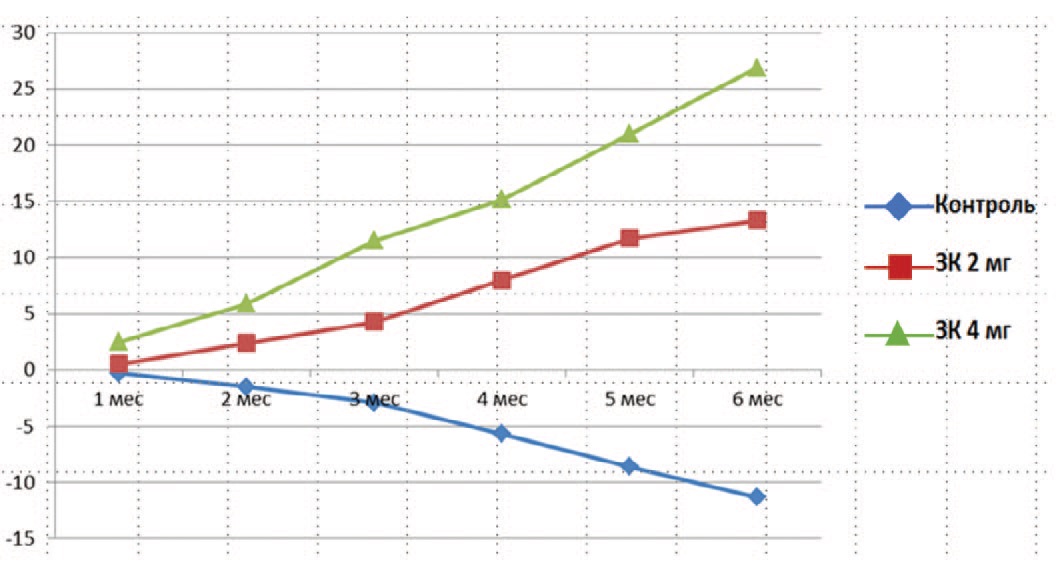
Рис. 3. Изменение МПКТ в процессе АРТ от исходного уровня (в %) Исследования МПК методом денситометрии выполнены в конце каждого месяца в течение 6 месяцев.
Fig. 3. Change in BMD during ART from baseline (in %). BMD studies by densitometry were performed at the end of each month for 6 months
Таблица 7. Динамика МПКТ по Т-критерию (в %) к 3 и 6 месяцам АРТ
Table 7. Dynamics of BMD by T-criterion (in %) by 3 and 6 months of ART
| № | Группы Groups |
Изменение Т-критерия в % от исходного уровня, нг/мл, М ± S (мин; макс) Change T-test in % of initial level, M ± S (min; max) |
Критерий p p criteria |
|
|---|---|---|---|---|
| 3 месяца 3 months |
6 месяцев 6 months |
|||
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n=15 |
11,5 ± 7,4 (27; 0) |
26,9 ± 6,0 (36; 15) |
W критерий, р = 0,01* |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n=15 |
4,3 ± 7,7 (27; -6) |
13,3 ± 10,5 (36; 0) |
W критерий, р = 0,03* |
| 3 | Контроль, n = 15 Control, n=15 |
-2,9 ± 7,8 (9; -20) |
-12,1 ± 7,8 (0; -25) |
W критерий, р = 0,01* |
| Критерий, р p criteria |
Кр-Уол: р < 0,001* M-U критерий: р1-2 = 0,006*; р1-3 = 0,004*; р2-3 < 0,001* |
Кр-Уол: р < 0,001* M-U критерий: р1-2 = 0,001*; р1-3 < 0,001*; р2-3 < 0,001* |
— | |
* различия значимы the differences are significant
В таблице 8 представлены число и процентное соотношение пациентов 1 и 2 групп, у которых повышение МПКТ к 6-му месяцу под влиянием АРТ препаратом ЗК позволило снять диагноз «остеопороз», а также число пациентов, у которых показатели МПКТ достигли уровня нормы. Как видно, в группе 1 (ЗК 4 мг) остался только 1 больной с остеопорозом, а показатель нормы отметили у 6 пациентов, тогда как в группе 2 (ЗК 2 мг) осталось 2 пациента с остеопорозом, а нормальные значения МПКТ подтвердили у 4-х мужчин. В противоположность этому, в группе контроля к концу 6-го месяца продолжающейся АДТ без АРТ, остеопороз выявили у 6, а показатель нормы только у 1 пациента.
Таблица 8. Число пациентов с различным состоянием МПКТ к 6 месяцам АРТ
Table 8. Number of patients with different BMD status after 6 months of ART
| № | Группы Groups |
Остеопороз Osteoporosis |
Остеопения Osteopenia |
Норма Normal |
Критерий p p criteria |
|---|---|---|---|---|---|
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n=15 |
1 (7%) | 8 (53%) | 6 (40%) | χ2 Пирсона, р1-3 = 0,028*; р2-3 < 0,14*; р1-2 < 0,67* |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n=15 |
2 (13%) | 9 (60%) | 4 (27%) | |
| 3 | Контроль, n = 15 Control, n=15 |
6 (40%) | 8 (53%) | 1 (7%) |
*различия значимы the differences are significant
Основные биохимические показатели больных РПЖ в процессе АРТ
У пациентов, получающих АДТ аналогами ГнРГ отмечали кастрационный уровень тестостерона и максимально сниженные значения ПСА. Как видно из таблицы 9, показатели ПСА у пациентов 3-х групп оставались на низком уровне, соответствующем действию АДТ, в течение всех 6-и месяцев наблюдения. При этом, различий между группами выявлено не было.
Таблица 9. Динамика ПСА (нг/мл) в процессе АРТ
Table 9. Dynamics of PSA (ng/ml) during ART
| № | Группы Groups |
ПСА, нг/мл, М ± S (мин; макс) PSA, ng/ml, M ± S (min; max) |
Критерий p p criteria |
||
|---|---|---|---|---|---|
| Исходно Initial level |
3 месяца 3 months |
6 месяцев 6 months |
|||
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n=15 |
1,19 ± 1,03 (0,16; 3,96) |
1,48 ± 0,87 (0,12; 3,54) |
1,34 ± 1,07 (0,1; 3,88) |
ANOVA-П, р = 0,45 |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n=15 |
1,03 ± 0,65 (0,08; 2,57) |
1,11 ± 0,87 (0,1; 2,5) |
1,14 ± 0,84 (0,09; 2,45) |
ANOVA-П, р = 0,43 |
| 3 | Контроль, n = 15 Control, n=15 |
1,29 ± 0,78 (0,13; 3,01) |
1,27 ± 0,82 (0,11; 3,13) |
1,32 ± 0,91 (0,12; 3,27) |
ANOVA-П, р = 0,68 |
| Критерий, р p criteria |
ANOVA-П, р = 0,64 |
ANOVA-П, р = 0,87 |
— | ||
р < 0,05 – различия значимы p < 0.05, the differences are significant
Аналогичные результаты были получены и при анализе показателей тестостерона сыворотки крови (табл. 10). Кастрационный уровень тестостерона, соответствующий действию АДТ, сохранялся у пациентов всех групп на протяжении 6-и месячного периода наблюдения. Статистических различий между группами также выявлено не было.
Таблица 10. Динамика уровня тестостерона в процессе АРТ
Table 10. Dynamics of blood testosterone levels during ART
| № | Группы Groups |
Тестостерон, нг/мл, М ± S (мин; макс) Testosterone, ng/ml, M ± S (min; max) |
Критерий p p criteria |
||
|---|---|---|---|---|---|
| Исходно Initial level | 3 месяца 3 months | 6 месяцев 6 months | |||
| 1 | ЗК (4 мг) n = 15 ZA (4 mg) n=15 |
0,27 ± 0,15 (0,10; 0,78) |
0,35 ± 0,23 (0,10; 0,87) |
0,36 ± 0,20 (0,12; 0,79) |
ANOVA-П, р = 0,49 |
| 2 | ЗК (2 мг) n = 15 ZA (2 mg) n=15 |
0,33 ± 0,12 (0,14; 0,59) |
0,38 ± 0,18 (0,10; 0,79) |
0,37 ± 0,17 (0,11; 0,72) |
ANOVA-П, р = 0,73 |
| 3 | Контроль, n = 15 Control, n=15 |
0,31 ± 0,15 (0,11; 0,64) |
0,29 ± 0,20 (0,12; 0,68) |
0,36 ± 0,18 (0,11; 0,75) |
ANOVA-П, р = 0,63 |
| Критерий, р p criteria |
ANOVA-П, р = 0,66 |
ANOVA-П, р = 0,89 |
— | ||
*р < 0,05 – различия значимы p < 0.05, the differences are significant
Анализ безопасности АРТ с использованием ЗК
Из 30 пациентов, получавших АРТ, у 2-х (у одного после первой инфузии 4 мг ЗК и у второго после первой инфузии 2 мг ЗК) отметили нежелательные явления, в виде реакции острой фазы с гриппоподобными симптомами: лихорадка, озноб, артралгия. Эти симптомы разрешились в течение трех дней на фоне противовоспалительной терапии парацетамолом. Других побочных эффектов, связанных с терапией препаратом ЗК, выявлено не было. В частности, креатинин крови у 30 пациентов, получивших АРТ препаратом ЗК, оставался на уровне 100 кмоль/л в течение всех 6-и месяцев наблюдения. Экскреция креатинина также находилась в пределах (7,1 – 18,5 ммоль/сут). Уровень общего кальция в плазме крови был в диапазоне возрастной нормы: от 2,1 до 2,5 ммоль/сут, а экскреция кальция – колебалась от 1,4 до 5,5 ммоль/сут. В ходе исследования костных переломов у пациентов зарегистрировано не было.
ОБСУЖДЕНИЕ
Исследования свидетельствуют о развитии остеопении и остеопороза у больных РПЖ на фоне АДТ, снижении общей прочности костей за счет уменьшения МПКТ [39-40]. Так, через 12 месяцев АДТ наблюдали значительное снижение МПКТ: бедренной кости на 2,4 – 2,5% и позво-ночника на 3,3 – 4,0% [7]. В настоящем исследовании у пациентов, получавших АДТ не менее 6 месяцев, показатель МПКТ (Т-критерий), полученный методом DXL денситометрии, до начала АРТ был снижен у 93% пациентов. При этом остеопороз отметили у 24% и остеопению у 69% больных. О динамике процесса нарушений в костях судить было невозможно, так как измерения МПКТ до начала АДТ не проводили. Такая распространенность костных нарушений, в нашем исследовании оказалась несколько выше, чем работах со сходным дизайном. Так в исследовании Campbell S.C. и соавт., доля пациентов с остеопорозом и остеопенией составила 68% [41].
В ряде руководств по профилактике и лечению потери костной массы в результате АДТ, не указан препарат первой линии для лечения остеопороза, имеются только ссылки на хорошие результаты применения ЗК и деносумаба [20, 42]. Также, нами не найдено работ, описывающих в сравнении эффективность и безопасность 4 мг и 2 мг доз ЗК при лечении остеопороза, вызванного АДТ.
Ранее было показано, что однократное введение ЗК не обеспечивает долговременного антирезорбтивного эффекта [43]. Поэтому мы использовали кратное введение ЗК с интервалом в 3 месяца, что до этого применяли и в других работах [41].
Проведенное исследование показало, что АРТ с использованием препарата ЗК эффективно подавляет резорбцию костной ткани, существенно повышенную у больных гормонально-чувствительным РПЖ, перенесших хирургическую кастрацию или получающих АДТ агонистами ГнРГ. При АРТ в группах, получивших препарат ЗК дважды через каждые 3 месяца в дозах 4 мг и 2 мг, показатель МПКТ увеличился к 6-ому месяцу на 27% и 13% соответственно. В группе контроля он снизился на 12%. При этом, под влиянием терапии препаратом ЗК в дозе 4 мг число пациентов с остеопорозом уменьшилось до 6%, а с нормальным уровнем МПКТ – достигло 40%.
В похожем по дизайну исследовании, после 12 месяцев лечения ЗК в дозе 4 мг раз в три месяца, МПКТ поясничного отдела позвоночника увеличилась на 4,17% (p < 0,0001), а МПКТ обеих бедренных костей и шейки правой бедренной кости также значимо выросла (p -2.0), свидетельствующие об отсутствии остеопороза, наблюдали у 25% больных [42]. То есть, продемонстрирован тренд, характерный и для нашего исследования. Имеющиеся различия, вероятно, связаны с разными методами измерения МПКТ и различием состояния в группах пациентов из-за малой выборки.
В данном исследовании в качестве скрининг-метода определения МПКТ успешно применили DXL денситометрию, которая характеризуется простотой, быстротой проведения, мобильностью и более низкой стоимостью, что важно при организации обследования больших потоков пациентов. Проведенные ранее исследования показали сравнимую эффективность методов DEXA и DXL [44, 45]. При этом, следует иметь в виду необходимость использования одного и того же метода при оценке МПКТ в динамике.
В настоящем исследовании, как и ряде работ ранее, в качестве основного биохимического маркера костной резорбции использовали CTX-1 [29, 32, 34]. Нами продемонстрировано снижение уровня СТХ-1, одного из наиболее информативных маркеров костной резорбции, в 4 раза к 3 месяцам наблюдения, после однократной инфузии 4 мг препарата ЗК. После повторного введения 4-х мг ЗК этот уровень СТХ-1 сохранился и к 6-и месяцам наблюдения. При инфузии в аналогичном режиме препарата ЗК в дозе 2 мг, также наблюдали снижение СТХ-1, но менее выраженное, чем в первом случае. Важно отметить, что у всех пациентов после двукратной инфузии 4 мг ЗК, показатели СТХ-1 снизились к 6-ому месяцу до уровня возрастной нормы (100%). При терапии препаратом ЗК в дозе 2 мг, такой результат наблюдали у 87% больных.
Ряд специалистов считают, что если у пациентов, которым планируется АДТ, уже есть остеопороз, то лечение остеомодифицирующими кость агентами следует проводить параллельно, так как эти больные подвергаются повышенному риску переломов [41]. Более того, показано, что проведение денситометрии и лечение мужчин с высоким риском перелома костей является экономически эффективным [46].
Японскими авторами из JSBMR (Japanese Society Bone and Mineral Research) в руководстве 2020 года по ведению пациентов с потерей костной массы, обусловленной лечением рака, предложен алгоритм, основанный на оценке Т-критерия и рекомендованной ВОЗ шкалы FRAX – Fracture Risk Assessment Tool, использующей антропометрические данные пациента, результаты специального опросника и показатели денситометрии (https://www.sheffield.ac.uk/FRAX/tool.aspx?country=13) [42]. Применение данного инструмента может быть полезным при отборе пациентов, получающих длительную терапию агонистами ГнРГ в ходе АДТ (рис. 4).
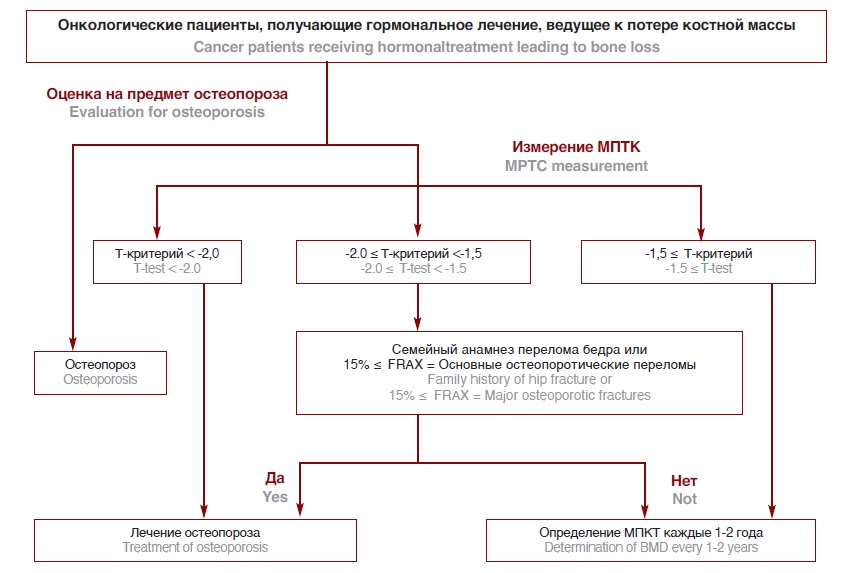
Рис. 4. Алгоритм оказания медицинской помощи пациентам с потерей костной массы, вызванной лечением рака [43]
Fig. 4. Algorithm for providing medical care to patients with bone loss caused by cancer treatment [43]
Применение ЗК у больных РПЖ может, помимо антирезорбтивного действия, оказывать и противоопухолевый эффект. В обзоре J. Zekri и соавт. описаны возможные прямые и косвенные механизмы противоопухолевого действия ЗК. Авторы указывают, что противоопухолевый эффект может быть опосредован ингибированием пролиферации опухолевых клеток, индукцией апоптоза, синергическим/аддитивным ингибирующим действием цитотоксических агентов, ингибированием ангиогенеза, снижением адгезии опухолевых клеток к кости, уменьшением инвазии и миграции опухолевых клеток, дезорганизацией клеточного цитоскелета и активацией специфического клеточного противоопухолевого иммунного ответа. Существуют также данные клинических испытаний, свидетельствующие о том, что применение ЗК улучшило результаты долгосрочной выживаемости у больных РПЖ с метастазами в кости и без них [47].
ЗАКЛЮЧЕНИЕ
Таким образом, проведенное исследование показало высокую эффективность и достаточную безопасность препарата ЗК (Резорба) в дозах 4 мг и 2 мг в/в 1 раз в 3 месяца в качестве средства антирезорбтивной терапии у пациентов, получающих длительную гормональную терапию агонистами ГнРГ.
Сокращения:
М – среднее;
S – стандартное отклонение;
мин – минимальное значение;
макс – максимальное значение;
АНОВА – дисперсионный параметрический критерий для множественных сравнений;
АНОВА-П – дисперсионный критерий для множественных повторных сравнений;
Кр-Уол – «Краскела-Уоллиса» непараметрический критерий для множественных сравнений;
χ2 Пирсона – критерий различий для частотных показателей;
F-test – критерий Фридмана оценки значимости различий для множественных повторных измерений;
Wil–Bon – критерий Вилкоксона с поправкой Бонферони для оценки различий между 3-мя и 6-ю месяцами терапии при повторных измерениях;
M-U – Bon – критерий Манна-Уитни с поправкой Бонферони для оценки межгрупповых различий;
p1-2, р1-3, р1-2 – уровни значимости межгрупповых различий;
р3-и, р6-и – уровни значимости различий между исходными показателями и показателями на 3-й и 6-й месяц терапии;
р6-3 – уровень значимости различий между показателями на 3 и 6 месяцев терапии;
t–пар – парный параметрический критерий Стьюдента для оценки различий повторных измерений.
ЛИТЕРАТУРА
1. Taitt HE. Global trends and prostate cancer: a review of incidence, detection, and mortality as influenced by race, ethnicity, and geographic location. Am J Mens Health 2018;12(6):1807–23. https://doi.org/10.1177/1557988318798279.
2. Состояние онкологической помощи населению России в 2019 г. [под ред. А.Д. Каприна, В.В. Старинского, А.О. Шахзадовой]. М., 2020; 239 c. URL: https://glavonco.ru/cancer_register/%D0%9F%D0%BE%D0%BC%D0 %BE%D1%89%D1%8C%202019.pdf [The state of oncological care for the population of Russia in 2019 [editors: A.D. Kaprin, V.V. Starinsky, A.O. Shakhzadova]. M., 2020. 239 p. URL: https://glavonco.ru/cancer_register/ %D0%9F%D0%BE%D0%BC%D0%BE%D1%89%D1%8C%202019.pdf. (In Russian)].
3. Wu CT, Yang YH, Chen PC, Chen MF, Chen WC. Androgen deprivation increases the risk of fracture in prostate cancer patients: a populationbased study in Chinese patients. Osteoporos Int 2015;26(9):2281–90. https://doi.org/10.1007/s00198-015-3135-9.
4. Wang A, Obertova Z, Brown C, Karunasinghe N, Bishop K, Ferguson L, et al. Risk of fracture in men with prostate cancer on androgen deprivation therapy: a population-based cohort study in New Zealand. BMC Cancer 2015(15):837. https://doi.org/10.1186/ s12885-015-1843-3.
5. Nguyen C, Lairson DR, Swartz MD, Du XL. Risks of Major Long-term side effects associated with androgen-deprivation therapy in men with prostate cancer. Pharmacotherapy 2018;38(10): 999–1009. https://doi.org/10.1002/phar.2168.
6. Smith MR, Boyce SP, Moyneur E, Duh MS, Raut MK, Brandman J. Risk of clinical fractures after gonadotropin-releasing hormone agonist therapy for prostate cancer. J Urol 2006;175(1):136–9. https://doi.org/10.1016/ S0022-5347(05)00033-9.
7. Greenspan SL, Coates P, Sereika SM, Nelson JB, Trump DL, Resnick NM. Bone loss after initiation of androgen deprivation therapy in patients with prostate cancer. J Clin Endocrinol Metab 2005;90(12):6410–7.https://doi.org/10.1210/jc.2005-0183.
8. Hussain SA, Weston R, Stephenson RN, George E, Parr NJ. Immediate dual energy X-ray absorptiometry reveals a high incidence of osteoporosis in patients with advanced prostate cancer before hormonal manipulation. BJU Int 2003;92(7):690–4. https://doi.org/10.1046/j.1464-410x.2003.04471.x
9. Kiratli BJ, Srinivas S, Perkash I, Terris MK. Progressive decrease in bone density over 10 years of androgen deprivation therapy in patients with prostate cancer. Urology 2001;57(1):127–32.
10. Shahinian VB, Kuo YF, Freeman JL, Goodwin JS. Risk of fracture after androgen deprivation for prostate cancer. N Engl J Med 2005; 352(2):154–64. https://doi.org/10.1056/NEJMoa041943.
11. Shao YH, Moore DF, Shih W, Lin Y, Jang TL, Lu-Yao GL. Fracture after androgen deprivation therapy among men with a high baseline risk of skeletal complications. BJU Int 2013;111(5):745–52. https://doi.org/10.1111/ j.1464-410X.2012.11758.x.
12. Johnell O, Kanis JA, Oden A, Johansson H, De Laet C, Delmas P, et al. Predictive value of BMD for hip and other fractures. J Bone Miner Res 2005;20(7):1185–94. https://doi.org/10.1359/JBMR. 050304.
13. Marshall D, Johnell O, Wedel H. Meta-analysis of how well measures of bone mineral density predict occurrence of osteoporotic fractures. BMJ 1996; 312(7041):1254–9. https://doi.org/10.1136/ bmj.312.7041.1254.
14. Oefelein MG, Ricchiuti V, Conrad W, Resnick MI. Skeletal fractures negatively correlate with overall survival in men with prostate cancer. J Urol 2002;168(3):1005–7. https://doi.org/10.1097/01.ju. 0000024395.86788.cc.
15. Hernlund E, Svedbom A, Ivergard M, Compston J, Cooper C, Stenmark J, et al. Osteoporosis in the European Union: medical management, epidemiology and economic burden. A report prepared in collaboration with the International Osteoporosis Foundation (IOF) and the European Federation of Pharmaceutical Industry Associations (EFPIA). Arch Osteoporos 2013;8(1):136. https://doi.org/10.1007/s11657-013-0136-1.
16. National Institute for Health and Care Excellence (NICE). Prostate cancer: diagnosis and man-agement NICE guideline [NG131]. URL: https://www.nice.org.uk/guidance/ng131. 14 August 2019.
17. Mottet N, Bellmunt J, Bolla M, Briers E, Cumberbatch MG, De Santis M, et al. EAU-ESTRO-SIOG Guidelines on prostate cancer. Part 1: screening, diagnosis, and local treatment with curative intent. Eur Urol 2017; 71(4):618–29. https://doi.org/10.1016/j. eururo.2016.08.003.
18. El Badri S., Salawu A., Brown J. Bone health in men with prostate cancer: review article. Current Osteoporosis Reports 2019;17(6):527–537. https://doi.org/10.1007/s11914-019-00536-8.
19. Русаков И.Г., Алексеев Б.Я., Быстров С.В. Профилактика остеопороза у больных раком предстательной железы при максимальной андрогенной блокаде при применении препарата деносумаб. Медицинский вестник Башкортостана 2011;6(2):277-282. [Rusakov I.G., Alekseyev B.Ya., Bystrov S.V. Osteoporosis prevention in prostate cancer patients with аndrogen-deprivation therapy using denosumab. Meditsinskiy vestnik Bashkortostana = Bashkortostan medical journal 2011;6(2):277-282. (In Russian)].
20. Манзюк Л.В., Багрова С. Г., Копп М.В., Кутукова С.И., Семиглазова Т.Ю. Использование остеомодифицирующих агентов для профилактики и лечения патологии костной ткани при злокачественных новообразованиях. Злокачественные опухоли: Практические рекомендации RUSSCO 2017;7(S2):477–485. https://doi.org/10.18027 / 2224–5057–2017– 7–3s2–477–485. [Manzyuk L.V., Bagrova S.G., Kopp M.V., Kutukova S.I., Semiglazova T.Yu. The use of osteomodifying agents for the prevention and treatment of bone tissue pathology in malignant neoplasms. Zlokachestvennyye opu-kholi: Prakticheskiye rekomendatsii RUSSCO = Malignant tumors: Practice guidelines RUSSCO 2017;7(S2):477–485. https://doi.org/10.18027/2224–5057–2017–7–3s2–477–485.
21. Datta M, Schwartz GG. Calcium and vitamin D supplementation during androgen deprivation therapy for prostate cancer: a critical review. Oncologist 2012;17(9):1171–9. https://doi.org/10.1634/theoncologist.2012-0051.
22. Smith MR, McGovern FJ, Zietman AL, Fallon MA, Hayden DL, Schoenfeld DA, et al. Pami-dronate to prevent bone loss during androgen-deprivation therapy for prostate cancer. N Engl J Med 2001;345(13):948–55. https://doi.org/10.1056/NEJMoa010845.
23. Michaelson MD, Kaufman DS, Lee H, McGovern FJ, Kantoff PW, Fallon MA, et al. Random-ized controlled trial of annual zoledronic acid to prevent gonadotropin-releasing hormone agonist-induced bone loss in men with prostate cancer. J Clin Oncol 2007;25(9):1038–42. https://doi.org/10.1200/ JCO.2006.07.3361.
24. Bhoopalam N, Campbell SC, Moritz T, Broderick WR, Iyer P, Arcenas AG, et al. Intravenous zoledronic acid to prevent osteoporosis in a veteran population with multiple risk factors for bone loss on androgen deprivation therapy. J Urol 2009;182(5):2257–64. https://doi.org/10.1016/ j.juro.2009.07.046.
25. Ryan CW, Huo D, Demers LM, Beer TM, Lacerna LV. Zoledronic acid initiated during the first year of androgen deprivation therapy increases bone mineral density in patients with prostate cancer. J Urol 2006;176(3):972–8; discussion 8. https://doi.org/10.1016/j.juro.2006.04.078.
26. Serpa Neto A, Tobias-Machado M, Esteves MA, Senra MD, Wroclawski ML, Fonseca FL, et al. Bisphosphonate therapy in patients under androgen deprivation therapy for prostate cancer: a systematic review and meta-analysis. Prostate Cancer Prostatic Dis 2012;15(1):36–44. https://doi.org/10.1038/ pcan.2011.4.
27. Smith MR, Egerdie B, Hernandez Toriz N, Feldman R, Tammela TL, Saad F, et al. Denosumab in men receiving androgendeprivation therapy for prostate cancer. N Engl J Med 2009;361(8):745–55. https://doi.org/10.1056/ NEJMoa0809003.
28. Denham JW, Nowitz M, Joseph D, Duchesne G, Spry NA, Lamb DS, et al. Impact of androgen suppression and zoledronic acid on bone mineral density and fractures in the Trans-Tasman Radiation Oncology Group (TROG) 03.04 Randomised Androgen Deprivation and Radiotherapy (RADAR) randomized controlled trial for locally advanced prostate cancer. BJU Int 2014;114(3):344–53. https://doi.org/10.1111/bju.12497.
29. Сивков А.В., Кешишев Н.Г., Рабинович Э.З., Трудов А.А. Остеопороз при гормональной терапии рака предстательной железы и маркеры ремоделирования костной ткани. Экспериментальная и клиническая урология 2015(4):46-53. [Sivkov A.V., Keshishev N.G., Rabinovich E.Z., Trudov A.A. Osteoporosis during the hormonal therapy of prostate cancer and markers of bone tissue remodeling. Eksperimentalnaya i Klinicheskaya urologiya= Experimental and Clinical Urology 2015(4):46-53. (In Russian)].
30. Vinholes J, Coleman R, Eastell R. Effects of bone metastases on bone metabolism: implications for diagnosis, imaging and assessment of response to cancer treatment. Cancer Treat Rev 1996;22(4):289–331. https://doi.org/10.1016/ s0305-7372(96)90021-3.
31. Christgau S, Bitsch-Jensen O, Hanover Bjarnason N, Gamwell Henriksen E, Qvist P, Alexan-dersen P, Bang Henriksen D. Serum CrossLaps for monitoring the response in individuals undergoing antiresorptive therapy. Bone 2000;26(5):505-511. https://doi.org/10.1016/S8756-3282(00)00248-9.
32. Bergmann P, Body JJ, Boonen S, Boutsen Y, Devogelaer JP, Goemaere S, et al. Evidence-based guidelines for the use of biochemical markers of bone turnover in the selection and monitoring of bisphosphonate treatment in osteoporosis: a consensus document of the Belgian bone club. Int J Clin Pract 2009;63(1):19–26. https://doi.org/10.1111/j.1742-1241.2008.01911.x
33. Bjarnason NH, Henriksen EEG, Alexandersen P, Christgau S, Henriksen DB, Christiansen C. Mechanism of circadian variation in bone resorption. Bone 2002;30(1):307–313. https://doi.org/ 10.1016/s8756-3282(01)00662-7.
34. Vasikaran S, Eastell R, Bruyère O, Foldes AJ, Garnero P, Griesmacher A, et al. Markers of bone turnover for the prediction of fracture risk and monitoring of osteoporosis treatment: a need for interna-tional reference standards. Osteoporos Int 2011;22(2):391–420. https://doi.org/10.1007/ s00198-010-1501-1
35. International Society for Clinical Densitometry (ISCD). Adult Official Positions of the ISCD as updated in 2019. URL: https://www.iscd.org/ officialpositions/2019-iscd-official-positions-adult/.
36. Kanis JA, Melton LJ 3rd, Christiansen C, Johnston CC, Khaltaev N. The diagnosis of osteoporosis. J Bone Miner Res 1994;9(8):1137–41. https://doi.org/10.1002/jbmr.5650090802.
37. Родионова С.С., Морозов А.К., Варецкая-Чивилихина Н.Б., Мунина Л.И., Лягинский А.В. Оценка диагностической значимости остеоденситометра DXL CALSCAN. Остеопороз и остеопатии 2005(3):24-28. [Rodionova S.S., Morozov A.K., Varetskaya-Civilikhina N.B., Munina L.I., Lyaginskii A.V. Evaluation of the diagnostic significance of the DXL CALSCAN osteodensitometer. Osteoporoz i osteopatii = Osteoporosis and osteopathy 2005(3):24-28. (In Russian)].
38. Thorpe JA, Steel SA. The DXL Calscan heel densitometer: evaluation and diagnostic thresholds. Br J Radiol 2006;79(940):336-41. https://doi.org/10.1259/ bjr/22191429.
39. Alibhai SM, Yun L, Cheung AM, Paszat L. Screening for osteoporosis in men receiving androgen deprivation therapy. JAMA 2012;307(3):255–6. https://doi.org/10.1001/jama.2011.2022.
40. Cheung AS, Hoermann R, Ghasem-Zadeh A, Tinson AJ, Ly V, Milevski SV, et al. Differing effects of Zoledronic acid on bone microarchitecture and bone mineral density in men receiving androgen deprivation therapy: a randomized controlled trial. J Bone Miner Res 2020;35(10):1871–80. https://doi.org/10.1002/jbmr.4106.
41. Campbell SC, Bhoopalam N, Moritz TE, Pandya M, Iyer P, Vanveldhuizen P, et al. The use of zoledronic acid in men receiving androgen deprivation therapy for prostate cancer with severe osteopenia or osteoporosis. Urology 2010;75(5):1138-43. https://doi.org/10.1016/j.urology.2009.11.083.
42. Fukumoto S, Soen S, Taguchi T, Ishikawa T, Matsushima H, Terauchi M, et al. Management manual for cancer treatment-induced bone loss (CTIBL): position statement of the JSBMR. J Bone Miner Metab 2020;38(2):141–144. https://doi.org/10.1007/s00774-020-01087-0.
43. Watanabe D, Kimura T, Watanabe R, Takano Y, Uehara Y, Minowa T, et al. Effects of once-yearly zoledronic acid on bone density and incident vertebral fractures in nonmetastatic castration sensitive prostate cancer patients with osteoporosis. BMC Cancer 2021;17;21(1):422 https://doi.org/10.1186/s12885-021-08177-w.
44. Salminen H, Sääf M, Ringertz H, Strender L-E. Bone mineral density measurement in the calcaneus with DXL: comparison with hip and spine measurements in a cross-sectional study of an elderly female population. Osteoporos Int 2005;16(5):541-51. https://doi.org/10.1007/s00198-004-1719-x.
45. Muschitz C, Dimai HP, Kocijan R, Kaider A, Zendeli A, Kühne F, et al. The discriminatory capacity of BMD measurements by DXA and dual X-ray and laser (DXL) at the calcaneus including clin-ical risk factors for detecting patients with vertebral fractures. Osteoporos Int 2013;24(8):2181-90. https://doi.org/10.1007/s00198-013-2266-0.
46. Ito K, Elkin E.B, Girotra M, Morris MJ. Cost-effectiveness of fracture prevention in men who receive androgen deprivation therapy for localized prostate cancer. Ann Intern Med 2010;152(10):621-629 https://doi.org/10.7326/0003-4819-152-10-201005180-00002.
47. Zekri J, Mansour M, Mustafa Karim S. The anti-tumour effects of zoledronic acid. J Bone Oncol 2014;3(1):25-35. https://doi.org/10.1016/j.jbo.2013.12.001.









Комментарии