Ю.Г. Аляев, Л.М. Рапопорт, Е.С. Сирота, Е.А. Безруков, А.В. Кондрашина
НИИ уронефрологии и репродуктивного здоровья человека ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» (Сеченовский университет) Минздрава России; Россия, 119991 Москва, ул. Большая Пироговская, 2, стр. 1 Контакты: Евгений Сергеевич Сирота essirota@mail.ru
Введение
Рак почки составляет 2–3 % от общего числа опухолей в организме человека. В мире ежегодно определяется прирост заболеваемости раком почки в 2 %, около 90 % случаев рака почки локализуется в ее паренхиме [1]. В Российской Федерации с 2010 по 2014 г. зарегистрировано около 100 тыс. новых случаев, ежегодный прирост заболеваемости составляет около 3–4 % [2]. На сегодняшний день в лечении локализованных форм рака почки все больше используются нефронсберегающие технологии. Резекция почки является рекомендованной операцией для хирургического лечения рака стадии Т1а и при наличии технической возможности при стадии Т1b – Т2 [1, 3].
Общемировой тенденцией последних десятилетий стало выполнение лапароскопических резекций почки (ЛРП) и робот-ассистированных вмешательств при наличии опухолевого поражения, как моно-, так и билатерального [4–6]. В результате чего опухоль удаляется полностью в отсутствие положительного хирургического края с максимально возможным сохранением почечной паренхимы. Выполнение ЛРП у пациентов со стадией Т1b и выше в некоторых случаях сопряжено с риском возникновения положительного хирургического края и возможным увеличением числа больных с местным рецидивом рака почки.
Как показало наше исследование, в настоящее время в России нет данных о работах по частоте и причинам развития местного рецидива после выполнения ЛРП при локализованном раке паренхимы почки.
Цель исследования – оценить частоту и причины развития местных рецидивов рака почки после выполнения ЛРП при локализованном раке паренхимы почки.
Материалы и методы
В исследовании были ретроспективно проанализированы данные историй болезни 459 пациентов с опухолью почки, которым с июня 2011 г. по май 2017 г. выполнили ЛРП в Клинике урологии им. Р.М. Фронштейна ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» (Сеченовский университет) Минздрава России. Возраст больных варьировал от 25 до 79 лет (средний – 55 ± 8 лет). Мужчин было 255 (55,5 %), женщин – 204 (44,5 %). По данным планового гистологического исследования у 399 (86,9 %) больных был верифицирован рак почки. Средний размер опухоли составлял 3,5 ± 1,8 см. Синхронный рак почки имел место у15 (3,75 %) больных. Остальные характеристики опухолей представлены в табл. 1. С опухолью единственной почки были прооперированы 6 (1,3 %) пациентов.
Таблица 1. Характеристики опухолей почки перед первичными оперативными вмешательствами
| Опухоль Tumor |
Число больных, абс. (%), n = 459 Number of patients, abs. (%), n = 459 |
|---|---|
| Первичная рТ: PrimaryрТ: |
|
| pTla | 243(61) |
| pTlb | 114 (28.7) |
| рТ2 | >4(3.5) |
| рТЗа | 28 (7.S) |
| Доброкачественная: Benign: |
60(13) |
| N0 | 399(100) |
| МО | 399(100) |
| Дифференцировка но Фурману: Fuhrman nuclear grade: |
|
| G1 | 80 (20) |
| G2 | 238 (59.8) |
| G3 | 81 (20.2) |
| G4 | 0(0) |
| Морфологический вид: Morphological type: |
|
| светлоклеточный clear cell |
281 (73) |
| папиллярный papillary |
85 (21.3) |
| хромофобный chromophobe |
33(6.7) |
| Локализация, сегмент почки: Localization, kidney's segment: |
|
| верхний upper |
118(25.7) |
| средний median |
199(43.3) |
| нижний lower |
72 (31) |
Кроме стандартных методов предоперационного обследования 297 (64,7 %) больным было выполнено 3D-моделирование патологического процесса с целью планирования и навигации операций. Для получения трехмерных объектов в нашей работе мы использовали программу Amira компании VSG версии 5.4.5 (лицензия ASTND. 44644), в которой обрабатывались данные мультиспиральной компьютерной томографии (МСКТ), полученные в формате DICOM (Digital Imagingand Communications inMedicine). Для проведения операций лапароскопический доступ был использован у 392 (85,4 %) больных, ретроперитонеоскопический – у 67 (14,6 %). Для лапароскопических операций применяли стандартный набор эндоскопического оборудования. Техника их выполнения была классической, с соблюдением всех этапов оперативного вмешательства. Операции выполняли 5 хирургов Клиники урологии им. Р.М. Фронштейна Сеченовского университета с большим опытом выполнения лапароскопических операций. Местный рецидив рака развился у 3 (0,75 %) из 399 больных.
Результаты
Рецидив после выполнения лапароскопической операции по поводу рака почки развился у 3 мужчин в возрасте 58 (1-й больной), 63 (2-й больной) и52 (3-й больной) лет. У1-го пациента опухоль размером 55 × 40 × 55 мм локализовалась в нижнем сегменте правой почки по передней поверхности. У 2-го пациента образование размером 44 × 45 × 46 мм располагалось на границе среднего и нижнего сегментов правой почки, также по передней поверхности. У 3-го больного опухоль размером 64 × 46 × 49 мм находилась в области верхнего сегмента левой почки. Пациентам в предоперационном периоде на основании данных МСКТ брюшной полости с контрастированием выполнены 3D-компьютерное моделирование патологического процесса и виртуальное планирование оперативного вмешательства. На основании проведенного моделирования опухоли были оценены по 3 шкалам нефрометрической оценки (табл. 2).
Таблица 2. Нефрометрическая оценка сложности планируемого оперативного вмешательства по шкалам RENAL, PADOVA и С-индекс
| Пациент | RENAL | PADOVA | С-индекс |
|---|---|---|---|
| 1-й 1* | 7а | 10 | 1,36 |
| 2-й 2«j | Юа | 11 | 1,66 |
| 3-й | 6а | S | 1,84 |
У 1-го больного образование размером до 17 × 18 × 19 мм локализовалось в нижнем сегменте правой почки, в зоне выполненной резекции, и активно накапливало контрастный препарат. У 2-го больного на границе среднего и нижнего сегментов правой почки визуализировалась зона измененной паренхимы без четких границ размером 45 × 25 мм, неравномерно накапливающая контрастный препарат. Также были выявлены образования в периренальной клетчатке, по переднему листку фасции Герота и в правом латеральном канале на уровне почки, по ходу правой почечной артерии, вокруг нижней полой вены на уровне ворот почек размером 4–12 мм, накапливающие контраст до 90 ед. Н в артериальную фазу. У 3-го больного при контрольном обследовании в области ложа удаленной почки определялось образование размером 12 × 12 × 14 мм с неровными контурами.
Первому больному с целью предотвращения прогрессирования опухолевого процесса выполнено оперативное вмешательство в объеме лапароскопической нефрэктомии с регионарной лимфаденэктомией. По данным гистологического исследования была подтверждена опухоль того же самого морфологического типа, что и при первичной резекции опухоли почки (рис. 1).
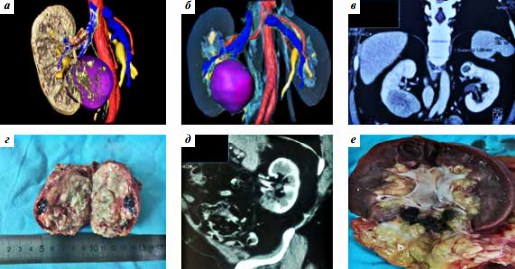
Рис. 1. Данные 1-го больного: а, б – 3D-моделирование патологического процесса и виртуальное планирование оперативного вмешательства перед резекцией почки, в – МСКТ больного перед резекцией, г – макропрепарат резецированной опухоли, д – МСКТ рецидива опухоли, е – удаленная почка с рецидивом в дне резекции. МСКТ – мультиспиральная компьютерная томография
Второй больной прооперирован из открытого доступа, выбор которого был обусловлен наличием не только местного рецидива в зоне выполненной резекции, но и метастатического поражения в паранефральной клетчатке и диссеминированного процесса по всему правому флангу. Операция выполнена в объеме нефрэктомии с регионарной лимфаденэктомией. Морфологически был выявлен светлоклеточный рак, но степень опухолевой дифференцировки стала низкой. Во всех удаленных подозрительных участках паранефральной клетчатки выявлены метастазы рака, также в 2 из 10 удаленных паракавальных лимфатических узлов установлено наличие метастатического поражения.
Третьему пациенту был удален местный рецидив опухоли из лапароскопического доступа. На дооперационном этапе на основании 3D-моделирования (рис. 2а) было проведено планирование оперативного пособия с определением анатомических ориентиров. Для улучшения интраоперационной навигации ввиду малого размера образования использовался интраоперационный лапароскопический ультразвуковой датчик. Применение в комплексе данных методик навигации позволило выявить и удалить рецидив опухоли (рис. 2б). При морфологическом исследовании установлено наличие светлоклеточного почечного рака со степенью дифференцировки 2 по Фурману, образование было ограничено хорошо выраженной капсулой и удалено с запасом окружающей клетчатки.
Обсуждение
Согласно данным мировой литературы, случаи рецидива рака почки после выполнения резекции почки колеблются от 0 до 10,6 % случаев [7–10]. В нашем исследовании местные рецидивы после проведенных ЛРП при сроке наблюдения от 3 до 71 мес (в среднем 8,6 мес) возникли в первые 12 мес после операции. В России данные по местному рецидиву после резекции почки по поводу рака представлены ФГБУ «Национальный медицинский исследовательский центр онкологии им. Н.Н. Блохина» Минздрава России, где в группе наблюдения из 203 больных с выполненной резекцией почки местный рецидив был выявлен у 5 (2,5 %) больных в среднем через 56,1 (3–120) мес после лечения [11].
Наибольшая выборка больных (806 пациентов) после резекции почки по поводу опухоли была оценена в работе J.-C. Bernhard и соавт., при этом рецидив опухоли развился у 26 больных (3,2 %), а временной диапазон выявления рецидивов опухоли составлял от 7 до 252 мес [12].
При ретроспективном анализе интраоперационных видеозаписей первичных резекций почки у больных причина местного рецидива рака почки была связана с неполностью удаленной первичной опухолью почки, так как опухоль глубоко проникала в синус почки и охватывала множество магистральных сосудов почки или имела многоузловое строение. Также нами отмечено, что опухоль имела плохо выраженную псевдокапсулу, поэтому при выполнении атипичной энуклеорезекции у пациентов возможно оставление участка опухолевой ткани в области дна резекции, который мог служить причиной развития местного рецидива опухоли. По данным мировых исследований, псевдокапсула имеется у 82 % опухолей паренхимы почки, толщина данной структуры опухоли в среднем составляет до 0,6 мм [13].
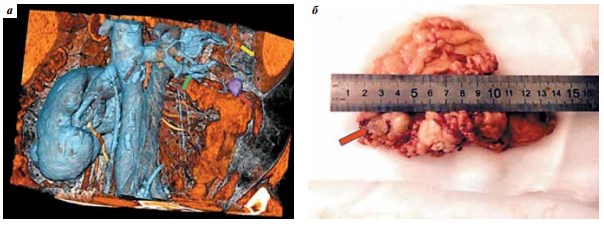
Рис. 2. Данные 3-го больного: а – 3D-моделирование рецидива в ложе удаленной почки (красной стрелкой показан рецидив опухоли в ложе почки, желтой – селезенка, зеленой – область пресечения почечной вены слева), б – макропрепарат: удаленная жировая клетчатка с местным рецидивом (красной стрелкой показан рецидив опухоли на разрезе)
Анализ данных клинических наблюдений показал, что развитие местного рецидива возникло у больных с размером опухолевых образований более 4 см. Ряд международных исследователей считают выполнение резекции почки при размерах опухоли более 4 см и стадии Т1b и выше одним из факторов риска возникновения местного рецидива рака почки [14], хотя имеются опубликованные данные о том, что размер опухоли более 4 см не имеет прогностического значения [15].
У всех пациентов с рецидивом рака почки верифицирован светлоклеточный почечноклеточный рак, который, помнению большинства мировых исследователей, относится к высокоагрессивным и быстропрогрессирующим опухолям [1, 16–17]. Низкодифференцированная форма рака (G3 по Фурману) также является фактором неблагоприятного прогноза [18–21].
При исследовании макропрепарата удаленной почки у 2-го больного было выявлено наличие рецидива опухоли не только в дне ранее выполненной резекции, но и на расстоянии от выполняемой операции – в ткани паренхимы почки (рис. 3).
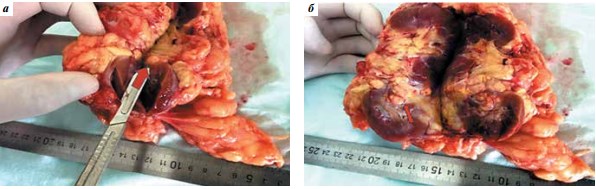
Рис. 3. Удаленная почка с рецидивом опухоли 2-го больного: а – участок опухоли за пределами дна резекции (показан стрелкой), б – область дна первично выполненной резекции (показана стрелкой)
Ряд авторов приводит данные исследований, которые подтверждают частоту выявления многоцентрового расположения опухоли в почке от 5,3 до 25 % [22–25]. При обследовании в предоперационном периоде применение методик диагностики в виде ультразвукового исследования и МСКТ не всегда эффективно для выявления мультицентровых образований в почке ввиду их малого размера [26].
До сих пор, по данным мировой литературы, не определена четкая взаимосвязь стадии Т с мультицентровым расположением опухоли. Имеются работы, по данным которых существует прямая связь мультицентрового расположения опухоли со стадией Т [27], в то время как часть исследователей такую связь отрицает [28–29].
Природа возникновения мультицентрового расположения опухоли в почке до сих пор не всегда понятна. Причиной может быть метастатическое распространение опухоли внутри паренхимы почки или образование новой опухоли, не связанной с основным образованием. У пациентов, согласно заключению патологических морфологов, после первичной ЛРП не был зафиксирован положительный хирургический край, при этом гистологически установлено наличие инвазии псевдокапсулы опухоли. Вероятнее всего, инвазию псевдокапсулы можно интерпретировать как положительный хирургический край опухоли, особенно в случае с энуклеорезекцией почки. Это предположение согласуется с исследованием X. Chen и соавт., в которое были включены больные с опухолями стадий Т1b (n = 87) и Т1а (n = 92). Пациентам выполнялась нефрэктомия с последующим морфологическим исследованием, при этом наличие инвазии опухоли за пределы псевдокапсулы было выявлено у 23 (25 %) больных со стадией Т1а и у 34 (39 %) больных со стадией опухоли Т1b, максимальная глубина инвазии в паренхиму почки составила 3 мм (в среднем 0,8–1,4 мм) [30].
Однако, по данным R.A. Azhar и соавт., на основании исследования данных 123 пациентов, подвергнутых резекции почки, инвазия псевдокапсулы была установлена в 28 % случаев у больных с опухолью почки со стадией Т1а, при этом у всех больных морфологически был подтвержден отрицательный хирургический край [13].
По мнению D.D. Laganosky и соавт., существует несколько прогностических факторов, приводящих к возникновению положительного хирургического края, одним из которых является глубокое расположение опухоли почки с проникновением в ее синус, что было выявлено у данных больных при виртуальном планировании вмешательства [31]. Также на вероятность и глубину инвазии псевдокапсулы опухоли влияет ядерная дифференцировка по шкале Фурмана [32]. В настоящее время наличие положительного хирургического края при выполнении органосохранных операций на почке у больных раком почки, по данным мировой литературы, встречается от 0 до 7 % при открытом доступе, от 0,7 до 4 % при лапароскопических операциях и от 3,9 до 5,7 % при роботических операциях [33].
У 2-го и 3-го больных возможной причиной диссеминации опухоли по паранефральной клетчатке стало повреждение псевдокапсулы опухоли при выполнении резекции, что могло послужить толчком к имплантационному метастазированию в паранефральную клетчатку. Однако при анализе мировой литературы было выявлено, что опухоли паренхимы почки в сравнении с другими опухолями мочеполовой системы имеют минимальный потенциал для имплантационного метастазирования при выполнении лапароскопических операций по поводу онкологических заболеваний [34–35].
Мировые данные о влиянии повреждения опухолевого узла на онкологические результаты и прогноз течения заболевания в ходе проведения лапароскопических пособий представлены исследованием H. Ito и соавт., в котором выявлено, что у 12 из 156 больных раком почки стадии Т1а в ходе выполнения ЛПР отмечено повреждение опухоли. При последующем динамическом наблюдении этих больных со средним периодом 30,0 (22,0–88,0) мес ни у одного из них не было выявлено метастатического поражения в брюшной полости [36]. Однако в ранее проведенных исследованиях о причинах метастазирования опухолей после выполнения лапароскопических операций отмечено, что факторы, способствующие развитию имплантационных метастазов, относятся к самой опухоли, а также связаны с самой раной и техническими аспектами проводимой операции [37]. В большинстве случаев к развитию имплантационного метастазирования приводит совокупность всех выше перечисленных факторов.
Заключение
По нашему мнению, для предотвращения развития местных рецидивов опухоли, особенно при выполнении ЛРП у больных со стадией процесса Т1b и выше, необходимо производить тщательный отбор пациентов для выполнения данного оперативного вмешательства. Выполнение технически сложных резекций приналичии глубокой инвазии опухоли в синус, а также широкого основания опухоли рекомендовано больным с абсолютными показаниями, такими как опухоль единственной почки, нарушение функции контралатеральной почки. При наличии относительных показаний к выполнению резекции предпочтительнее выполнять нефрэктомию.
В предоперационном периоде необходимы выявление наличия итолщины псевдокапсулы опухоли, исключение мультицентрового расположения опухоли.
Хорошая техническая оснащенность проводимой ЛРП, а также соблюдение онкологических принципов при выполнении пособий, таких как осторожное обращение с опухолью при резекции, соблюдение границ резекции опухоли, снижает риск развития рецидива рака почки.
При морфологической верификации опухолей паренхимы почки с высоким онкологическим потенциалом к прогрессированию, а также при наличии положительного хирургического края и инвазии псевдокапсулы опухоли необходимо проведение контрольной МСКТ органов брюшной полости с внутривенным контрастированием не позднее 3 мес после операции.
Авторы заявляют об отсутствии конфликта интересов
Литература
1. Ljungberg B., Bensalah K., Canfield S. et al. EAU Guidelines on Renal Cell Carcinoma: 2014 Update. Eur Urol 2015;67(5):913–24. DOI: 10.1016/j.eururo.2015.01.005.
2. Каприн А.Д., Аполихин О.И., Сивков А.В. Анализ уронефрологической заболеваемости и смертности в Российской Федерации за 2003–2013 гг. Экспериментальная и клиническая урология 2015;2:4–12. [Kaprin A.D., Apolikhin O.I., Sivkov A.V. Analysis of uronephrological morbidity and mortality in Russian Federation for 2003–2013. Eksperimentalnaya i klinicheskaya urologiya = Experimental and Clinical Urology 2015;2:4–12. (In Russ.)].
3. Campbell S., Uzzo R.G., Allaf M.E. et al. Renal mass and localized renal cancer: AUA Guideline 2017. J Urol 2017;198(3):520–9. DOI: 10.1016/j.juro.2017.04.100.
4. Patel S.G., Penson D.F., Pabla B. et al. National trends in the use of partial nephrectomy: a rising tide that has not lifted all boats. J Urol 2012;187:816–21. DOI: 10.1016/j.juro.2011.10.173. PMID: 22248514.
5. Smit Z.L. Current status of minimally invasive surgery for renal cell carcinoma. Curr Urol Rep 2016;17(6):43. DOI: 10.1007/s11934-016-0599-x. PMID: 27021911.
6. Zhao P.T., Richstone L., Kavoussi L.R. Laparoscopic partial nephrectomy. Int J Surg 2016;36(Pt C):548–53. DOI: 10.1016/j.ijsu.2016.04.028.
7. Novick A.C., Streem S., Montie J.E. et al. Conservative surgery for renal cell carcinoma: a single-center experience with 100 patients. J Urol 1989;141(4):835–9. PMID: 2926874.
8. Lapini A., Serni S., Minervini А. et al. Progression and long-term survival after simple enucleation for the elective treatmentof renal cell carcinoma: experience in 107 patients. J Urol 2005;174(1):57–60. DOI: 10.1097/01.ju.0000162019.45820.53. PMID: 15947577.
9. Serni S., Vittori G., Frizzi J. et al. Simple enucleation for the treatment of highly complex renal tumors: Perioperative, functional and oncological results. Eur J Surg Oncol 2015l;41(7):934–40. DOI: 10.1016/j.ejso.2015.02.019. PMID: 25957967.
10. Wood E.L., Adibi M., Qiao W. et al. Local tumor bed recurrence following partial nephrectomy in patients with small renal masses. J Urol 2017 Sep 20. PII: S0022–5347(17)77555–6. DOI: 10.1016/j.juro.2017.09.072. PMID: 28941919.
11. Матвеев В.Б., Матвеев Б.П., Волкова М.И. и др. Роль органосохраняющего хирургического лечения рака почки на современном этапе. Онкоурология 2007;2:5–11.
12. Bernhard J.-C., Pantuck A.J., Wallerand H. et al Predictive factors for ipsilateral recurrence after nephronsparing surgery in renal cell carcinoma. Eur Urol 2010;57(6):1080–6. DOI: 10.1016/ j.eururo.2010.02.019. PMID: 20188458.
13. Azhar R.A., de Castro Abreu A.L., Broxham E. et al. Histological analysis of the kidney tumor-parenchyma interface. J Urol 2015;193(2):415–22. DOI: 10.1016/j.juro.2014.08.010. PMID: 25111913.
14. Patard J.J., Shvarts O., Lam J.S. et al. Safety and efficacy of partial nephrectomy for all T1 tumours based on an international multicenter experience. J Urol 2004;171(6 Pt 1):2181–5, quiz 2435. PMID: 15126781.
15. Bensalah K., Crépel M., Patard J.J. Tumor size and nephron-sparing surgery: does it still matter? Eur Urol 2008;53(4):691–3. DOI: 10.1016/j.eururo.2007.11.023. PMID: 18060683.
16. Jean A.M., Hopirtean V., Bazin J.P. et al. Prognostic factors for the survival of patients with papillary renal cell carcinoma: meaning of histological typing and multifocality. J Urol 2003;170(3):764–7. DOI: 10.1097/01.ju.0000081122.57148.ec. PMID: 12913693.
17. Young J.R., Coy H., Douek M. et al. Type 1 papillary renal cell carcinoma: differentiation from Type 2 papillary RCC on multiphasic MDCT. Abdom Radiol (NY) 2017;42(7):1911–8. DOI: 10.1007/s00261-017-1091-x. PMID: 28265706.
18. Fuhrman S., Lasky L.C., Limas L. Prognostic significance of morphologic parameters in renal cell carcinoma. Am J Surg Pathol 1982;6(7):655–63. PMID: 7180965.
19. Medeiros L.J., Jones E.C., Aizawa S.A. et al. Grading of renal cell carcinoma: Workgroup No. 2. Union Internationale Contre le Cancer and the American Joint Committee on Cancer (AJCC). Cancer 1997;80(5):990–1. PMID: 9307204.
20. Ficarra V., Martignoni G., Maffei N. et al. Original and reviewed nuclear grading according to the Fuhrman system a multivariate analysis of 388 patients with conventional renal cell carcinoma 2004 American Cancer Society. Cancer 2005; 103(1):68–75. DOI: 10.1002/cncr.20749. PMID: 15573369.
21. Shah P.H., Moreira D.M., Okhunov Z. et al. Positive surgical margins increase risk of recurrence after partial nephrectomy for high risk renal tumors. J Urol 2016;196(2):327–34.
22. Tsivian M., Moreira D.M., Caso J.R. et al. Predicting occult multifocality of renal cell carcinoma. Eur Urol 2010;58(1):118–26. DOI: 10.1016/j.eururo.2010.03.011. PMID: 20346577.
23. Richstone L., Scherr D.S., Reuter V.R. et al. Multifocal renal cortical tumors: frequency, associated clinicopathological features and impacton survival. J Urol 2004;171(2 Pt 1):615–20. DOI: 10.1097/01.ju.0000106955.19813.f6. PMID: 14713772.
24. Whang M., O’Toole K., Bixon R. et al. The incidence of multifocal renal cell carcinoma in patients who are candidates for partial nephrectomy. J Urol 1995;154(3):968–70. PMID: 7637103.
25. Cheng W.S., Farrow G.M., Zincke H. The incidence of multicentricity in renal cell carcinoma. J Urol 1991;146(5):1221–3. PMID: 1942266.
26. Melissourgos N., Doumas K., Messini I. et al. Multicentricity in renal cell carcinoma: can primary tumor location serve as a co-determinant of surgical treatment? Eur Urol 2002;41(3):262–6. PMID: 12180226.
27. Oya M., Nakamura K., Baba S. et al. Intrarenal satellites of renal cell carcinoma: histopatholocic manifestation and clinical implication. Urology 1995;46(21):161–4. PMID: 7624986.
28. Lang H., Lindner V., Martin M. et al. Prognostic value of multifocality on progression and survival in localized renal cell carcinoma. Eur Urol 2004;45(6):749–53. DOI: 10.1016/j.eururo.2004.02.006. PMID: 15149747.
29. Sargin S.Y., Ekmekcioglu O., Arpali E. et al. Multifocality incidence and accompanying clinicopathological factors in renal cell carcinoma. Urol Int 2009;82(3): 324–9. DOI: 10.1159/000209366. PMID: 19440022.
30. Chen X., Zhang Z., Du J. et al. Optimal surgical margin in nephron-sparing surgery for T1b renal cell carcinoma. Urology 2012;79(4):836–9. DOI: 10.1016/j.urology.2011.11.023.
31. Laganosky D.D., Filson C.P., Master V.A. Surgical Margins in Nephron-Sparing Surgery for Renal Cell Carcinoma. Curr Urol Rep 2017;18(1):8. DOI: 10.1007/s11934-017-0651-5. PMID: 28211006.
32. Minervini A., di Cristofano C., Lapini A. et al Histopathologic analysis of peritumoral pseudocapsule and surgical margin status after tumor enucleation for renal cell carcinoma. Eur Urol 2009:55(6):1410–8. DOI: 10.1016/j.eururo.2008.07.038. PMID: 18692300.
33. Marszalek M., Carini M., Chlosta P. et al. Positive surgical margins after nephronsparing surgery. Eur Urol 2012;61(4):757–63. DOI: 10.1016/j.eururo.2011.11.028. PMID: 22136987.
34. Micali S., Celia A., Bove P. et al Tumor seeding in urological laparoscopy: an international survey. J Urol 2004;171(6): 2151–4. DOI: 10.1097/01.ju.0000124929. 05706.6b. PMID: 15126775.
35. Tanaka K., Hara I., Takenaka A. et al. Incidence of local and port site recurrence of urologic cancer after laparoscopic surgery. Urology 2008:71(4):728–34. DOI: 10.1016/j.urology.2007.10.054. PMID: 18279936.
36. Ito H., Makiyama K., Kawahara T. et al. Impact of Accidental Tumor Incision During Laparoscopic Partial Nephrectomy on the Oncologic and Clinical Outcomes. Clinical Genitourinary Cancer Month 2015. DOI: 10.1016/j.clgc.2015.11.013.
37. Curet M.J. Port site metastases. Am J Surg 2004;187(6):705–12. DOI: 10.1016/j.amjsurg.2003.10.015. PMID: 15191862.
Статья опубликована в журнале "Андрология и генитальная хирургия" выпуск №4/2017, стр. 61-68










Комментарии