М.И. Коган1 , А.В. Хасигов1,3, Д.Г. Пасечник2 , И.И. Белоусов1
1 ГБОУ ВПО Ростовский государственный медицинский университет Минздрава России, кафедра урологии, г. Ростов-на-Дону, Россия (344022, г. Ростов-на-Дону, пер. Нахичеванский 29), e-mail:dept_kogan@mail.ru
2 ГБОУ ВПО Ростовский государственный медицинский университет Минздрава России, Центральная научно-исследовательская лаборатория, г. Ростов-на-Дону, Россия (344022, г. Ростов-на-Дону, пер. Нахичеванский 29).
3 ГБОУ ВПО Северо-Осетинская государственная медицинская академия Минздрава России, кафедра хирургических болезней №2, г. Владикавказ, Россия.
Введение. Одним из эффективных методов избавления больных от коралловидных камней почек является перкутанная нефролитотомия. Помимо хирургических способов, современное лечение коралловидного нефролитиаза (КН) должно быть сфокусировано также на оптимизации функций почек, предотвращении трансформации почечного поражения в хроническую болезнь почек (ХБП) и минимизации степени хронической почечной недостаточности (ХПН) [1, 6, 9, 12]. Одним из способов оценки риска развития ХБП является морфологическое исследование ткани почки. Однако, большинство работ, посвященные патоморфологическим изменениям в почке при мочекаменной болезни (МКБ), основаны на изучении удаленных органов при запущенных и осложненных формах заболевания. Тем не менее, известно, что раннее выявление повреждения и перестройки различных структур нефрона могут быть предикторами риска развития ХБП и могут быть основанием для проведения нефропротективной терапии. В связи с этим изучение нефробиоптатов для оценки рисков развития почечной недостаточности у больных КН может иметь важный клинический интерес. [2, 3, 4, 5, 7, 8, 10, 11].
Цель исследования. Изучить особенности морфологических изменений почек на момент оперативного лечения коралловидного нефролитиаза.
Материал и методы исследования. Объектами морфологического исследования послужили ткани пораженной почки, полученные путем интраоперационной (во время выполнения перкутанной нефролитотомии) чрескожной пункционной тонкоигольчатой биопсии. Забор материала осуществляли у 12 пациентов в стандартных инраоперационных условиях: пациентам после проведения регионарной анестезии, обработки операционного поля и инструментария выполняли чрескожную биопсию патологической почки под УЗИнаведением в положении пациента на животе. Забирали два биоптата из почечной ткани с последующим выполнением основного этапа операции, не меняя положение больного на столе. Биоптаты фиксировали 10% забуференным нейтральным формалином c последующей заливкой в парафиновые блоки по классической методике, Срезы окрашивали гематоксилином-эозином, ШИК реакцией по Хочкиссу и трихромовой окраской по Массону для оценки фиброза интерстиция с последующим изучением и фотографированием под микроскопом.
Морфологические изменения в биоптатах анализировали в зависимости от поражения различных сегментов нефрона, интерстиция почки и сосудов. Степень фиброза интерстиция оценивали полуколичественно: Т0 – отсутствие фиброза, Т1 до 25% площади биоптата, Т2 от 26 до 50% площади биоптата, Т3 свыше 51% площади биоптата. Степень выраженности гломерулосклероза характеризовали как процент тотально гиалинизированных клубочков к их общему количеству в биоптате. Под ремоделированием сосудов понимали перестройку стенки сосудов с изменением параметров сосудистой морфологии (просвет, толщина стенки (медии, интимы), соотношение просвет/стенка). Были выделены три формы ремоделирования гипертрофическую, эутрофическую, гипотрофическую, в каждом случае учитывали уменьшение или увеличение просвета сосуда.
Результаты и обсуждение. В 6 наблюдениях отмечены изменения, характерные для начальной стадии фокального сегментарного гломерулосклероза (Рис.1). Стенки капилляров клубочка имели неравномерное утолщение, преимущественно в зоне его рукоятки. Отмечалась адгезия отдельных капиллярных петель между собой. Мезангиум незначительно расширен. В 4 наблюдениях отдельные клубочки были на стадии тотального гиалиноза. В 3 наблюдениях определялся перигломерулярный фиброз. В одном биоптате имелся выраженный отек мочевого пространства капсулы Боумена с коллабированием капиллярной сети. Возможно, эти изменения связаны с образованием «атубулярных» клубочков с последующим коллапсом и гиалинозом их, а также атрофией нефронов (Рис. 2).
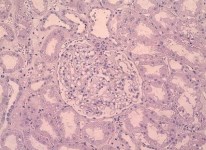
Рисунок 1. Начальные признаки ФСГС: неравномерное утолщение стенок капилляров клубочка, преимущественно в зоне его рукоятки. Слабо выраженное расширение мезангиума. Адгезия отдельных капиллярных петель между собой. Окраска гематоксилином-эозином. Ув.х200.
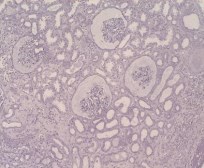
Рисунок 2. Клубочки сближены. Выраженный отек мочевого пространства капсулы Боумена с коллабированием капиллярной сети. Умеренная эктазия просвета дистальных извитых канальцев. В отдельных канальцах признаки повреждения и атрофии эпителия. Умеренный фиброз интерстиция со слабо выраженной лимфо-гистиоцитарной инфльтрацией. Окраска гематоксилином-эозином. Ув. х 100.
Во всех наблюдениях в извитых канальцах и корковых собирательных протоках выявлялись дистрофические изменения эпителия различной степени выраженности, в отдельных структурах – апоптоз групп клеток (Рис. 3). В 6 случаях отмечена эктазия просвета преимущественно дистальных извитых канальцев и собирательных протоков, как в корковом, так и мозговом веществе, причем в 4 наблюдениях встречалась микрокистозная трансформация отдельных канальцев и протоков. В 2 наблюдениях в просветах прямых канальцев и собирательных протоков мозгового вещества имелись глобулярного вида микрокальцинаты (Рис. 4,5).
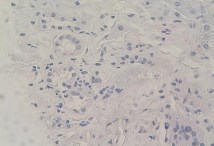
Рисунок 3. Дистрофические изменения эпителия дистальных извитых канальцев и собирательных протоков коркового вещества. Апоптоз групп клеток. Окраска гематоксилином-эозином. Ув.х400.
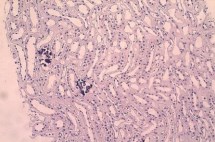
Рисунок 4. Кальцинаты в просвете собирательных протоков. Очаговая атрофия эпителия прямых канальцев. Умеренная эктазия просветов канальцев и протоков. Окраска гематоксилином-эозином. Ув.х100.
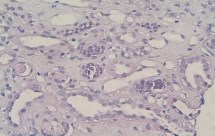
Рисунок 5. В просвете прямых канальцев – микролиты (глобулярные белковые массы с включениями кальция). Окраска гематоксилином-эозином. Ув.х400.
В 7 наблюдениях в мозговом веществе пирамид отмечались признаки бесклеточного фиброза и гиалиноза интерстиция, степень фиброза соответствовала Т1-Т2 (Рис. 6), и только в одном наблюдении достигала уровня Т3. Гиалиноз и фиброз интерстиция сопровождался атрофией эпителия прямых канальцев, собирательных и выводных протоков, в двух наблюдениях достигавшей уровня «тиреоидизации». Фиброз интерстиция коркового вещества почки встретился в 5 биоптатах, в 4 он соответствовал Т2 степени, в одном Т1. Кроме того, в 4 наблюдениях встречались субкапсулярно расположенные мелкие рубцы, представляющие собой фокусы выраженного фиброза интерстиция с умеренно выраженной лимфо-гистиоцитарной инфильтрацией, атрофией эпителия канальцев вплоть до их исчезновения и замещения рубцовой тканью (Рис. 7). В 3 наблюдениях фиброз интерстиция сочетался с дезорганизацией структуры канальцев и протоков. В этой зоне базальная мембрана и просвет канальцев и протоков отсутствовали, клетки приобретали вытянутую форму, с крупными гиперхромными ядрами (Рис. 8). Данные изменения оказались фенотипически сходными с описываемым в литературе эпителиально-мезенхимальным переходом, являющимся одной из причин прогрессии почечного фиброза.
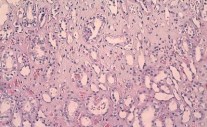
Рисунок 6. Бесклеточный фиброз и гиалиноз стромы пирамиды, умеренная эктазия собирательных протоков, атрофия прямых канальцев (петля Генле) и собирательных протоков. Окраска гематоксилином-эозином. Ув. х200.
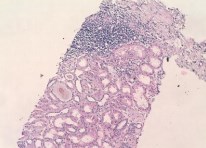
Рисунок 7. Под фиброзной капсулой почки фокус выраженной лимфогистиоцитарной инфильтрации интерстиция. Вокруг – дистрофические изменения эпителия извитых канальцев. Атрофия эпителия собирательных протоков, единичная микрокиста из собирательного протока. Окраска гематоксилиномэозином. Ув. х100.
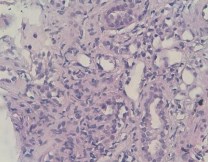
Рисунок 8. Фокус атрофии и дезорганизации структуры канальцев и протоков. В этой зоне базальная мембрана и просвет канальцев и протоков отсутствует, клетки приобретают вытянутую форму, с крупными гиперхромными ядрами. Количество внеклеточного матрикса (интерстиция) увеличено. Окраска гематоксилином-эозином. Ув. х 400.
Гипертрофический тип ремоделирования аркадной и междольковых артерий встретился в 4 наблюдениях, он сопровождался фиброэластозом интимы, очаговым фиброзом медии, просвет сосудов был сужен незначительно (Рис. 9). Гиалиноз приносящих и перитубулярных артериол выявлен в 4 биоптатах. В одном наблюдении в биоптат попала ткань почки в зоне, прилежащей к конкременту. В этом участке наблюдалось перифокальное смешанное экссудативно-продуктивное воспаление, единичные гигантские клетки типа инородных тел, грубоволокнистая фиброзная ткань, участок плоскоклеточной метаплазии уротелия (Рис. 10,11). В верхушке пирамиды – фокусы кальцинатов, окруженные рубцовой тканью. Перифокально некроз ткани пирамиды.
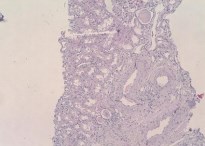
Рисунок 9. Аркадная и междольковые артерии – гипертрофия медии, утолщении и фиброэластоз интимы. Микрокистозная трансформация отдельных протоков и канальцев. Окраска гематоксилином-эозином. Ув. х100.
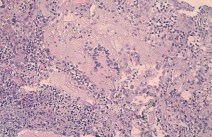
Рисунок 10. Ложе камня – выраженная полиморфноклеточная инфильтрация (нейтрофильные лейкоциты, лимфоциты, макрофаги). Гигантская клетка типа «инородных» тел. Окраска гематоксилином-эозином. Ув. х400.
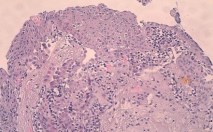
Рисунок 11. Ложе камня. Фокус плоскоклеточной метаплазии уротелия лоханки. Окраска гематоксилиномэозином. Ув. х400.
Заключение. Таким образом, в биоптатах почек у пациентов с КН преобладают изменения, связанные с различной степенью выраженности фиброза интерстиция преимущественно мозгового вещества и пирамид почки, сочетающиеся с повреждением и атрофией эпителия канальцев и протоков. В сосудах наблюдаются признаки гипертрофического типа ремоделирования артерий резистивного типа, гиалиноз артериол, что может быть связано с развитием у пациентов артериальной гипертензии. В клубочках начальные признаки фокального сегментарного гломерулосклероза вторичного сосудистого генеза.
Выше приведенные морфологические признаки почечного поражения могут быть предикторами развития ХПН у больных с КН, что позволяет рекомендовать проведение биопсии почек при ПНЛ у больных КН. Однако при проведении биопсии важно понимать, что изменения в почке при КН носят очаговый характер, и степень выраженности склеротических и воспалительных процессов в разных участках почек может существенно различаться. Поэтому при проведении процедуры биопсии важно избегать пункции явных зон рубцевания, чтобы исключить ошибочную трактовку процесса как конечную стадию ХБП. С
Список литературы.
1. Асфандияров, Ф.Р., Абдулхакимов Э. Р. Микроциркуляторное русло почек при мочекаменной болезни по данным лазерной допплеровской интраоперационной флоуметрии и морфологического исследования // Вестник Волгоградского государственного медицинского университета. 2008. № 1. С. 26-28.
2. Глыбочко П. В., Россоловский А. Н., Гражданов Р. А. и др. Клеточно-молекулярные механизмы повреждения мочевыводящих путей при обострении хронического калькулезного пиелонефрита // Медицинский вестник Башкортостана. 2011.T. 6, №2. С. 55 59.
3. Bosch J.P., Saccaggi A., Lauer A. Renal functional reserve in humans // Amer J. Med. – 1983. 75. – Р. 943-950.
4. Brian R. Lane, Poggio Emilio D., Herts Brian R.. Renal Function Assessment in the Era of Chronic Kidney Disease: Renewed Emphasison Renal Function Centered Patient Care // J.Urol. (Baltimore). – 2009. – №8. – Р. 435-443.
5. Brenner B.M., Levin S. A. Approaches to remission and regression of chronic renal diseases // J. Nephrol. – 1999. – №3. – Р. 81-83.
6. Canes D., Hegarty N. J., Kamoi K. Functional outcomes following percutaneous surgery in the solitary kidney // J. Urol. – 2009. –181(1). – P. 154-60.
7. Gambaro G. A., Favaro S., D'Angelo. Risk for renal failure in nephrolithiasis // Am. J. Kidney Dis. – 2001. – Vol. 37, suppl. 2. – P. 233-243.
8. Lane B.R., Poggio E.D., Herts B.R., Novick A.C. Renal function assessment in the era of chronic kidney disease: renewed emphasis on renal function centered patient care // J. Urol. – 2009. – Vol. 182 N 2. – P. – 435-43.
9. Leiske J. C., Toback F. G. Renal cellurinary crystal interaction // Curr Opin Nephrol Hypertens.-2000. 9. – Р. 349.
10. Moskovitz В., Halachmi S., Sopov V. Effect of percutaneous nephrolithotripsy on renal function: assessment with quantitative SPECT of (99m)Tc-DMSA renal scintigraphy // J. Endourol. – 2006. 20 (2). – Р. 102-106.
11. Shen P. The influence of percutaneous nephrolithotomy on human systemic stress response, SIRS and renal function // Urol. Res. –2010. – 38(5). – P. 403-408.
12. Wynn T. Cellular and molecular mechanisms of fibrosis // J. Pathol. – 2008. – Vol. 214. – P. 199-210.
Статья опубликована в журнале "Вестник урологии". Номер №1/2015 стр. 44-51














Комментарии