Яровой С.Ю.1 , Максимов В.А.2 , Медведев Е.В.2 , Ачба З.О.3 , Шоуа А.Б.4 , Маркарян С.В.3
1 Университетская хирургическая клиника, Россия, Москва
2 ФГБЛПУ «ЛОЦ МИД России» ‒ Больница, Россия, Москва
3 Центральный военный госпиталь Министерства обороны Республики Абхазии, г. Сухум
4 ГУ МЗ РА «Республиканская больница», Республика Абхазия, г. Сухум 127562, г. Москва, шоссе Алтуфьевское, 28, 1, тел: (916)1528149 Эл.почта: yarovoi.sergei@mail.ru, yarov_1968@mail.ru
Введение. Сложной проблемой в урологии остается лечение обструкции верхних мочевых путей вследствие стриктур мочеточников различного происхождения, локализации и протяженности.
Стриктуры мочеточника могут быть следствием различных причин, в том числе мочекаменной болезни, эндоскопических урологических процедур, лучевой терапии, открытой или лапароскопической хирургии, а также проникающих травматических повреждений. Частота стриктур мочеточника возросла в последние годы во многом в результате внедрения и широкого использования эндоскопии верхних мочевых путей. Так, возникновение стриктур мочеточника после уретероскопии встречается у больных от 3% до 11%. Это может возникать вследствие вклинения камня, относительной ишемии, часто из-за использования больших инструментов, чрезмерной продолжительности операции, травмы мочеточника с экстравазацией мочи, и прямой механической или термической травмы. Стриктура мочеточника может возникнуть вследствие травмы после различных оперативных вмешательств с формированием свища или непроходимости, в том числе абдоминальной и влагалищной гистерэктомии, восстановления сосудистого поражения, операций на органах малого таза, толстой кишки, прямой кишки и их злокачественных новообразований [1].
Одной из самых частых локализаций стриктур является проксимальный отдел мочеточника, которые встречаются в 70% случаев, на остальные локализации приходится оставшиеся 30% [2].
Золотым стандартом лечения таких больных остаются открытые и лапароскопические, робот-ассистированные реконструктивные операции (уретероуретероанастомоз, пластика ЛМС, уретероцистоанастомоз, заместительная кишечная пластика мочеточника) [3].
Стремительный рост минимально инвазивных технологий в медицине в течение последних лет привело к тому, что в современной хирургии очень сложно представить без установки дренажа. Спектр заболеваний, где стенты могут применяться, расширяется. Тем не менее, нерешенные проблемы связаны со стентированием, которые служат основой для развития и модернизации стентов, для поиска новых методов стентирования и новых материалов, которые могли бы оптимизировать их использование [4]. Применение стентов с наноструктурным покрытием успешно решает проблему бактериурии в послеоперационном периоде и значительно снижает риск воспалительных осложнений [5], однако это является методом кратковременного дренирования и не решает проблему качества жизни пациентов, которое является наиболее важным аспектом проблемы длительного дренирования мочеточника при помощи различных стентов [6-9].
С развитием технологий появились минимально инвазивные методики дренирования мочевых путей с использованием матричного стента Mematerm, который демонстрирует свойства саморасправляющейся гибкой конструкции. Он изготавливается из мононити никелида титана и обладает свойством «термопамяти», т.е. после установки в необходимую зону под влиянием определенной температуры начинает расправляться и принимать нужные по диаметру и форме размеры [10]. За последние 10 лет в мире появляется все больше сообщений о возможности коррекции сужений или облитераций мочеточника с помощью само удерживающихся металлических эндо протезов с оценкой эффективности их использования. [11-15].
Большое количество исследований было посвящено реакции ткани и изменениям стенки мочеточника вследствие воздействия металлических стентов, эффективности использования различных металлических и нитиноловых стентов. [16-19]. В то же время не так много публикаций об отдаленных результатах использования стентов из никелида титана при стриктурах мочеточников [20]. Однако минимально инвазивная операция по установке сетчатых эндопротезов в урологии стала практически рутинной в Европе. [21]
Представляем собственный опыт применения само удерживающихся стентов из никелида титана с термопамятью в различных клинических ситуациях. Целю исследования, явился анализ отдаленных результатов лечения больных со стриктурами различных отделов мочеточников с помощью установки стента из никелида титана Российского производства ООО МИТ.
Материалы и методы. Клинический материал был собран на базе ГКУБ 47, урологического отделения больницы МИД РФ Москва, Центрального Клинического Военного Госпиталя Министерства Обороны Республики Абхазия. За основу сообщения взяты отдаленные результаты лечения больных с 2009 по 2011 годы, с длительностью наблюдения 5-6 лет.
Нами выполнена установка 20 стентов из никелида титана 15 больным. Из них 6 женщин, 9 мужчин от 28 до 80 лет, средний возраст составил 54 года. Использованы стенты в комплекте с устройством доставки производства ООО МИТ Россия. Установка проводилась в условиях рентген-операционной с предварительной диагностической уретероскопией и ретроградной уретеропиелографией. В 4-х случаях использованы стенты с полипропиленовым покрытием, остальные стенты без покрытия.
5 пациентам стенты устанавливали в область пузырно-мочеточникового соустья после ТУР мочевого пузыря по поводу мышечно-неинвазивного уротелиального рака с вовлечением устья мочеточника и последующим рубцовым сужением области резекции (Рис. 1, 2).
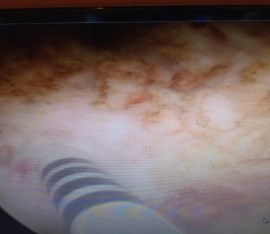
Рис. 1. Правый мочеточник дренирован стентом после трануретральной резекции мочевого пузыря по поводу уротелиального рака с вовлечением устья
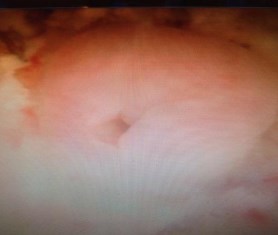
Рис. 2. Формирование рубцового стеноза правого мочеточника после удаления стента при контрольной цистоскопии через 3 месяца после ТУР
Все эти больные до установки сетчатого эндо протеза проходили диспансерное наблюдение в связи с мышечно-неинвазивным раком мочевого пузыря по стандартной методике в течение 2-х лет без рецидива заболевания, пассаж мочи из почек поддерживался путем установки внутренних стентов из полиуретана, которые меняли 1 раз в три месяца во время контрольной цистоскопии. Попытки восстановить пассаж мочи без стента у всех больных не увенчались успехом.
3 стента было установлено больной с обструкцией средней и нижней трети обоих мочеточников, обусловленных сдавлением извне увеличенными лимфоузлами вследствие их метастатического поражения при раке шейки матки и развитием уретерогидронефроза с 2-х сторон и обструктивной ОПН. Предварительно данной пациентке была выполнена двусторонняя ЧПНС, купирована ОПН, проведено 3 курса полихимиотерапии. 3 стента установлено пациенту с двусторонним гидронефрозом вследствие ретроперитонеального фиброза (Болезнь Ормонда).
5 стентов установлено 5 больным со стриктурой верхней трети мочеточника после перенесенных ранее открытых операций на почке (Рис. 3а, 3б).
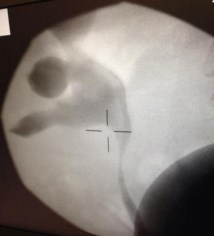
Рис. 3а. На ретроградной уретеропиелограмме перед установкой стента определяется стриктура верхней трети правого мочеточника, гидронефротическая трансформация, образовавшаяся у пациентки К. через 1 год после пиелолитотомии и сопровождавшаяся частыми атаками пиелонефрита, которые купировались только после дренирования правой почки
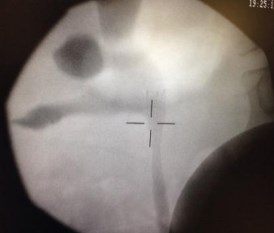
Рис. 3б. Восстановленный просвет верхней трети правого мочеточника у пациентки К. после установки стента из никелида титана производства ООО МИТ, Россия
3 стента установлено 3-м больным со стриктурой нижней трети мочеточника.
Всем больным проводили УЗ и рентгенологический мониторинг каждые 3 месяца в течение первого года наблюдения, каждые 6 месяцев в течение 2-го года наблюдения, далее 1 раз в год по настоящее время.
Результаты. Из 15 оперированных больных четырем (27%) стент был удален, одна пациентка с мигрировавшим в лоханку стентом, установленным из-за фиксированной девиации верхней трети мочеточника после пластики ЛМС (Culp-DeWeerd) готовится к операции лапароскопическому удалению стента, коррекции фиксированной девиации верхней трети левого мочеточника (Рис. 4, 5).
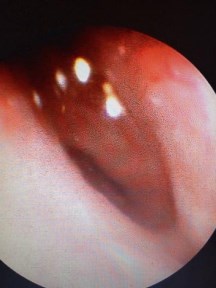
Рис. 4. Вид фиксированной девиации верхней трети левого мочеточника с образованием щелевидного сужения у пациентки С. после пластики лоханочно-мочеточникового сегмента во время диагностической уретеропиелоскопии
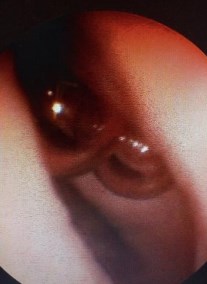
Рис. 5. Вид фиксированной девиации и губовидного сужения в области лоханочномочеточникового сегмента у той же пациентки С. во время уретеропиелоскопии
10 пациентов (66%) наблюдаются по настоящее время, длительность наблюдения составила от 5 до 6 лет, из них одной пациентке со стентом нижней трети правого мочеточника, установленном по поводу рецидивирующей стриктуры на 5-7 см от устья мочеточника и образовавшейся вследствие длительного стояния камня с образованием пролежня стенки мочеточника. Был установлен стент с полиуретановым покрытием. Через 2 года наблюдения при контрольном обследовании выявлен уретерогидронефроз вследствие обструкции на уровне стента. При диагностической уретероскопии визуализирована отслойка полиуретанового покрытия с заполнением просвета стента, больной выполнена реканализация путем коагуляции и удаления полиуретановой пленки, после чего отток мочи восстановился, больная наблюдается по настоящее время. Одному больному по поводу аналогичной стриктуры нижней трети правого мочеточника на 3-м году наблюдения выполнена установка дополнительного стента в связи с образованием сужения ниже дистального конца, ранее установленного стента. При диагностической уретероскопии и эндоуретеротомии перед установкой дополнительного стента признаков врастания, ранее установленного стента не выявлено, больной наблюдается по настоящее время (Рис. 6а, 6б, 6в).
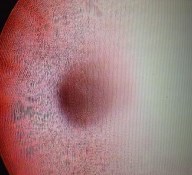
Рис. 6а. Вид стриктуры нижней трети правого мочеточника, образовавшейся у больного А. на 3-м году наблюдения и расположенной дистальнее ранее установленного стента на 0,5 см

Рис. 6б. Состояние проксимальной части стента и слизистой нижней трети правого мочеточника у того же больного А. после оптической эндоуретеротомии

Рис. 6в. Наложения фибрина в области дистальной части стента в нижней трети правого мочеточника у того же больного А. после оптической эндоуретеротомии
Четырем пациентам, которым удалены стенты, были в группе с мышечнонеинвазивным раком мочевого пузыря. Из них у одной пациентки при контрольной цистоскопии через 1 год наблюдения после установки стента выявлено врастание последнего с развитием уретерогидронефроза, что потребовало удаления эндопротеза с установкой обычного стента. При гистологическом исследовании выявлен рецидив рака мочевого пузыря с инвазией в мышечный слой, после чего было проведено 8 курсов химиотерапии Гемзар+Цисплатин с положительным эффектом в течение года. По данным контрольного обследования через 2 года после удаления стента, и через год на фоне полихимиотерапии, выявлена прогрессия заболевания в виде отдаленных метастазов в легкие и кости скелета. Пациентка умерла от нарастающей раковой интоксикации, вызванной метастазами рака мочевого пузыря на третьем году наблюдения после удаления стента (через 5 лет на фоне лечения рака мочевого пузыря).
У двоих пациентов этой группы стенты удалены через 2 года наблюдения вследствие выраженной ирритативной симптоматики и наличия пузырно-лоханочного рефлюкса. После удаления стента осложнений не было, пациенты наблюдаются по настоящее время, признаков нарушения пассажа мочи не выявлено. Один пациент 80 лет из этой группы не обращался в течение пятого года наблюдения после установки стента. При контрольном обследовании на пятом году наблюдения выявлен уретерогидронефроз с облитерацией в области стояния стента без покрытия. При цистоскопии обнаружена полная облитерация устья мочеточника с прорастанием стента. Выполнена биопсия мочевого пузыря, гистологическое заключение ‒ хроническое воспаление, опухолевой ткани не выявлено (Рис. 7а, 7б).
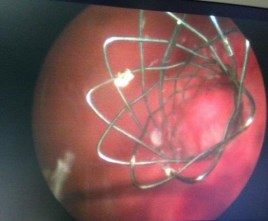
Рис. 7а. Цистоскопическая картина облитерации устья левого мочеточника с признаками полного врастания стента в стенку мочевого пузыря у больного 84 лет на 5-м году наблюдения после его установки
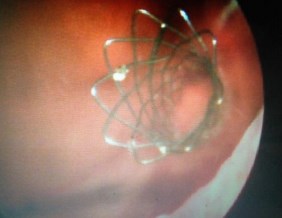
Рис. 7б. Цистоскопическая картина у того же больного 84 лет – топографическое расположение вросшего стента по отношению к шейке мочевого пузыря
Учитывая полученные данные об отсутствии прогрессии рака мочевого пузыря, длительное безрецидивное течение, больному выполнено удаление стента с резекцией мочевого пузыря, наложением неоуретероцистоанастомоза слева. Гистологическое заключение исследованного материала после резекции хроническое воспаление мочевого пузыря, ткань стенки мочеточника с выраженными склеротическими изменениями, опухолевой ткани не обнаружено. Больной наблюдается по настоящее время. Признаков нарушения пассажа мочи из верхних мочевых путей нет.
Выводы.
1. Исследование отдаленных результатов лечения больных со стриктурами мочеточника путем установки стента из никелида титана показало положительный результат в 66% случаев, что свидетельствует об эффективности данного минимально инвазивного метода лечения.
2. Установка стентов из никелида титана в области пузырномочеточникового соустья после ТУР может являться методикой выбора для временного длительного дренирования, которое требует тщательного диспансерного наблюдения.
3. Установка стента с целью устранения обструкции вызванной девиацией мочеточника может привести к миграции стента и требует дальнейших исследований в этом направлении.
4. При стриктурах мочеточника любой локализации установка стента из никелида титана показана у соматически осложненных пациентов.
Литература
1. Mang, C. Ureteral Strictures GU Reconstruction December 2011; 29.
2. Richard, B. Strategies for Open Reconstruction of Upper Ureteral Strictures Knight/ Steven J. Hudak, М. Allen F. Morey – Urol Clin North Am 2013 Aug 18;40(3):351-61.
3. Mufarrij, PW. Robotic dismembered pyeloplasty: a 6-year multi-institutional experience/ M. Woods, O.D. ShahJ Urol. 2008;180:1391.
4. Kogan, M.I. Directions and perspectives of the urological stent development (literature review)/ S.V. Shkodkin, A.V. Lyubushkin, O.V. MiroshnichenkoG. Endourologi №4, 64-69.
5. Коган, М.И. Эффективность использования стентов с наноструктурным покрытием при трансплантации почки (предварительные результаты) /М.И. Коган, Я.Г. Мойсюк, С.В. Шкодкин и др. Урология. – 2015. –№ 1. – С. 58-61.
6. Коган, М.И. Качество жизни пациентов с внутренними мочеточниковыми стентами / С.В. Шкодкин, Ю.Б. Идашкин и др. Медицинский вестник Башкортостана. – 2013. – № 2. – С. 98-100.
7. Дорончук, Д.Н. Оценка качества жизни больных мочекаменной болезнью в зависимости от метода дренирования верхних мочевыводящих путей/ М.Ф. Трапезникова, В.В. ДутовУрология. 2010. N 2. С. 14.
8. Мартов, А.Г. Улучшение качества жизни пациентов с внутренними стентами путем изменения их формы. / Ергаков Д.В., Корниенко С.И., Абоян И.А., и др.-Урология. 2011. N 2. С. 7-13.
9. Al-Kandari, A.M. Effects of proximal and distal ends of double J ureteral stent position on postprocedural symptoms and quality of life: a randomized clinical trial/ T.F Al-Shaiji, H. Shaaban, H.M. Ibrahim, and otherJ Endourol. 2007. Vol. 21, N 7. P. 698-702.
10. KOMIAKOV, B.K. Ureter replacement/ B.G. GULIEV, A.M. ZAGAZEJEVEndosk Hir 2010; 6: 50
11. Pauer, W. Metallic Wallstents: a new therapy for extrinsic ureteral obstruction/ H.Lugmayr-J Urol 1992; 148: 281—84.
12. Комяков, Б.К. Внутреннее дренирование верхних мочевыводящих путей при опухолевых обструкциях мочеточников/ Б.Г. ГулиевОнкоурология. 2010. N 2. С. 78-84.
13. Chung, H.H. Multicenter experience of the newly designed covered metallic ureteral stent for malignant ureteral occlusion: comparison with double J stent insertion/ Kim MD, Won JY, Won JH, and otherCardiovasc Intervent Radiol. 2014. Vol. 37, N 2. P. 463-470.
14. Ernesto, M. Novel Type of Ureteral Stents in the Treatment of a Bilateral Iatrogenic Transaction of the Ureters, Case Reports/F. Mondaini, D. Abdulcadir, C. Raspanti, and otherUrology 4, Volume 2013 (2013), Article ID 302351, 5 pages.
15. Bonniol, R. The thermoformable spiral metallic stents in the treatment of localized ureteral stenosis: an alternative to JJ stent? Prospective multicenter study/ P. Meria, A. Safsaf, B. Albouy, L. SibertProg Urol. 2011. Vol. 21, N 6. P. 397-404.
16. Шкодкин, С.В. Сравнительный анализ эффективности использования полиуретанового и наноструктурного стентов при дренировании верхних мочевых путей в эксперименте/ Коган М.И., Идашкин Ю.Б., Кобякова Ю. Н., и др.Вестник трансплантологии и искусственных органов. 2012. Т. 14, N 4. С. 65-73.
17. Глыбочко, П.В. Стенты мемокат (MEMOKATH) в лечении обструктивных заболеваний мочевых путей/ Аляев Ю.Г., Газимиев М.А., Григорьев Н.А., и др.Медицинский вестник Башкортостана. 2011. Т. 6, N 2.С. 227-231.
18. Borin, J.F. Initial experience with full-length metal stent to relieve malignant ureteral obstruction/ O. Melamud, R.V. ClaymanJ Endourol. 2006. Vol. 20, N 5. P. 300-304.
19. Шкуратов, С.И. Временные и постоянные никелид-титановые стенты при перкутанных операциях по поводу стриктур лоханочно-мочеточникового сегмента / И.В. Феофилов, В.Э. Гюнтер, В.И. Исаенко -Урология. 2007. N 4. С. 31-34.
20. Liatsikos, E.N. Ureteral metal stents: 10-year experience with malignant ureteral obstruction treatment/ Karnabatidis D, Katsanos K, Kallidonis P, and otherJ Urol. 2009. Vol. 182, N 6. P. 2613-2617
21. Daskalopoulos, G. Intraureteral metallic endoprosthesis in the treatment of ureteral strictures/ A. Hatzidakis, T. TriantafyllouEuropean Journal of Radiology, vol. 39, no. 3, pp. 194–200, 2001.
Статья опубликована в журнале "Вестник урологии" №1 2016, стр. 12-23










Комментарии