С.В. Котов
ГБУ ГКБ № 1 им. Н.И. Пирогова Департамента здравоохранения города Москвы
Стриктура уретры является заболеванием, проявляющимся симптомами нижних мочевых путей, рецидивирующей инфекцией мочевых путей, острой или хронической задержкой мочеиспускания, недержанием мочи, а иногда и почечной недостаточностью. Одной из самых сложных групп пациентов для реконструктивных операций в урологии являются пациенты со стриктурой или облитерацией уретры, требующие выполнения многоэтапной (заместительной) уретропластики. Целью данной работы явилась оценка эффективности многоэтапной уретропластики у пациентов с протяженными стриктурами уретры.
МАТЕРИАЛЫ И МЕТОДЫ
Проспективному анализу были подвергнуты результаты лечения 18 пациентов, перенесших заместительную уретропластику («двухили многоэтапная уретропластика») в период с 2010 по январь 2015 гг., которым было выполнено 40 операций.
В таблице 1 представлена клиническая характеристика пациентов, включенных в анализ. Подавляющее большинство больных (94,4%) было моложе 65 лет, при этом из них 14 (77,8%) пациентов – моложе 45 лет. Более чем в половине случаев (55,6%) причиной стриктуры уретры служили предшествующие медицинские вмешательства. Каждый третий пациент перенес в детском возрасте операции по поводу гипоспадии. В 7 случаях выявлено травматическое поражение уретры, причем 4 пациента перенесли многократные неудачные уретропластики. В одном случае поражение гениталий пациента облитерирующим ксеротическим баланитом (BXO) привело к распространению заболевания с крайней плоти на наружное отверстие уретры, ладьевидную ямку и дистальную треть пенильного отдела мочеиспускательного канала.
Таблица № 1. Клиническая характеристика пациентов, перенесших многоэтапную уретропластику
| Показатель | Значение |
|---|---|
| Количество пациентов, чел | 18 |
| Количество операций | 40 |
| Средний возраст, лет | 38,48+ 2,3 |
| Этиология стриктуры, кол-во пациентов (%) Ятрогенная: химический ожег уретры длительная катетеризация операция по поводу гипоспадии Посттравматическая Облитерирующий ксеротический баланит |
10 (55,6) 1 (5,6) 1 (5,6) 6 (33,3) 7 (38,9) 1 (5,6) |
| Локализация стриктуры, кол-во пациентов (%) мембранозный отдел бульбозный отдел пенильный отдел пануретральная стриктура |
1 (5,6) 3 (16,7) 9 (50) 5 (27,8) |
| Медиана протяжённости стриктуры (25 и 75 перцентиль) Min-max, см |
6,0 (5,4 ; 12,0) 4-18 |
| Наличие цистостомического дренажа, кол-во пациентов (%) | 6 (33,3) |
| Среднее значение максимальной скорости мочеиспускания, мл/с | 7,5 + 1,8 |
| Предшествующее лечение, кол-во пациентов (%) Нет Бужирование Внутренняя оптическая уретротомия (ВОУТ) > 2 ВОУТ + бужирование уретропластика |
9 (50) 3 (33,3) 1 (1,1) 1(1,1) 4 (44,4) |
Наиболее частыми локализациями поражения мочеиспускательного канала были: пенильный отдел независимо от вовлечения ладьевидной ямки (50%) и сочетание пенильного и бульбозного отделов, т.е. пан уретральная стриктура (27,8%). Это объясняется преобладанием ятрогенных причин образования стриктуры уретры.
Медиана протяженности поражения мочеиспускательного канала составила 6 см. Минимальная протяженность стриктуры уретры равнялось 4 см, а максимальная – 17 см.
Каждый второй пациент ранее подвергался лечению стриктуры уретры. Так, у 4-х (22,2%) больных были в анамнезе выявлены неудачные уретропластики. Последние, возможно, привели к дефициту кровообращения в зоне поражения уретры, а следовательно, и к полной потере уретральной площадки, здоровой спонгиозной ткани. Результатом этого стала необходимость выполнения заместительной уретропластики, как единственного варианта реконструктивной операции, позволяющей восстановить у пациента самостоятельное мочеиспускание. У 16,7% пациентов в анамнезе были неоднократные бужирования с прогрессивно уменьшающимся сроком между операциями вплоть до 1 недели. 11,2% пациентов подвергались неоднократным внутренним оптическим уретротомиям (ВОУТ).
Показаниями к многоэтапной уретропластике явились:
- поражение уретры рубцовым процессом с тотальным спонгиофиброзом в этой зоне, исключающим возможность одноэтапного оперативного вмешательства;
- облитерация уретры в пенильном отделе;
- стриктура уретры вследствие ранее перенесенных оперативных вмешательств на мочеиспускательном канале (преимущественно по поводу гипоспадии), приведших к выраженному рубцовому поражению окружающих тканей;
- отсутствие части уретры как результат предшествующих операций;
- поражение уретры вследствие облитерирующего ксеротического баланита (Balanitis xerotica obliterans – BXO).
Оперативное лечение пациентов состояло из нескольких этапов. На первом этапе всем пациентам было выполнено формирование уретральной площадки из слизистой ротовой полости по следующей методике (рис. 1, 2):
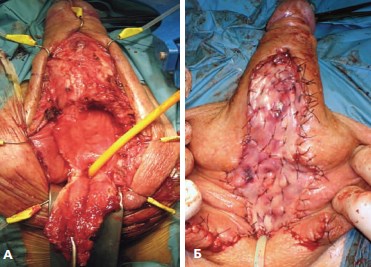
Рис. 1 А, Б. Первый этап уретропластики пациента Л., 62 года. А – выполнен доступ к пораженному участку уретры, вскрыт псевдодивернтикул уретры (полость в парауретральных тканях, выстланная эпителием). Б окончательный вид первого этапа уретропластики пациента два буккальных графта, фиксированных к белочной оболочке кавернозных тел
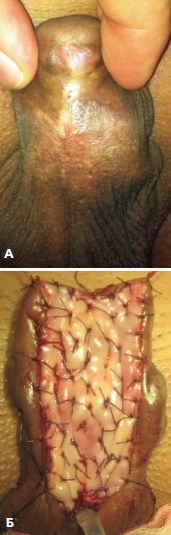
Рис. 2 А, Б. Первый этап уретропластики у пациента С., 21 года, Ds: стволовая гипоспадия: А – вид полового члена до операции; Б – вид полового члена по окончании первого этапа (формирование уретральной площадки буккальным графтом)
- положение пациента (на спине или литотомическое) выбиралось, учитывая локализацию поражения мочеиспускательного;
- при поражении бульбозного отдела уретры или при пануретральной стриктуре для формирования перинеостомы выкраивался трапецивидный кожный лоскут промежности;
- послойно выполнялся доступ к пораженному отделу уретры;
- производилась вентральная уретротомия в пределах здоровых тканей;
- измененный отдел уретры вместе со спонгиозным телом и окружающими рубцовыми тканями полностью иссекался;
- выполнялся забор буккального графта(-ов) по стандартной методике;
- трансплантат ротовой полости фиксировался на подготовленную белочную оболочку кавернозных тел;
- формировалась уретрокутанеостома;
- края буккального графта фиксировались в центре к белочной оболочке кавернозных тел, по краям к коже;
- накладывалась давящая повязка на новую уретральную площадку.
В случае сморщивания трансплантата слизистой щеки после первого этапа многоэтапной уретропластики, приведшее к сужению трансплантата и невозможности проведения тубуляризации неоуретры, выполнялась коррекция уретральной площадки.
Коррекция уретральной площадки – операция индивидуальная и точно описать ее стандартный протокол не представляется возможным. Операция может протекать по одному из трех сценариев:
- удаление уретральной площадки (полное или большей части) с формированием новой из графта;
- иссечение рубцово измененного участка вновь сформированной уретральной площадки в поперечном направлении с вставкой на место образовавшегося дефекта нового графта;
- продольное рассечение новой уретральной площадки по средней линии с фиксацией нового графта в образовавшийся дефект с одномоментной или отсроченной тубуляризацией уретральной площадки.
В случае сужения сформированной для самостоятельного мочеиспускания уретрокутанеостомы выполнялось ее продольное рассечение по вентральной полуокружности до нормального просвета. Удалялось рубцовое кольцо вокруг наружного отверстия уретры вместе с окружающими его рубцовоизмененными тканями. Фрагмент графта слизистой ротовой полости укладывался между краями здоровой уретры и окружающей кожи и фиксировался к подлежащим здоровым тканям для восстановления кровоснабжения в нем.
Заключительным этапом заместительной уретропластики является тубуляризация уретральной площадки (рис. 3, 4), которая выполнялась следующим образом:
- «U»-образным разрезом мобилизовались края уретральной площадки, которые отделялись от кавернозных тел по направлению к центру;
- после достаточной мобилизации краев уретральной площадки выполнялось их сшивание вокруг уретрального катетера № 24 Ch с формированием трубчатой неоуретры;
- производили замену уретрального катетера № 24 на силиконовый № 14 Ch;
- послойно ушивали фасции Бака (при ее сохранении по краям), мясистой оболочки над линией швов (для профилактики образования уретрокожных свищей) кожи.
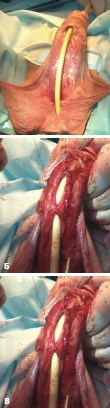
Рис. 3 А, Б, В. Пациент Л., 62 года. Заключительная операция многоэтапной уретропластики (тубуляризация уретральной площадки): А –вид уретральной площадки перед операцией; Б – тубуляризация; В – окончательный вид полового члена после операции
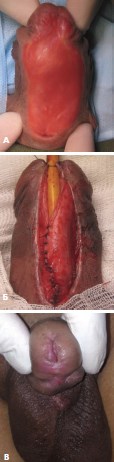
Рис.4 А, Б, В. Пациент С., 21 год, Ds: стволовая гипоспадия. Заключительная операция многоэтапной уретропластики (тубуляризация уретральной площадки): А – уретральная площадка перед операцией; Б – тубуляризация уретральной площадки; В – окончательный вид полового члена через 3 месяца после операции
РЕЗУЛЬТАТЫ
Общее количество операций в группе обследованных больных составило 40.
Первый этап оперативного лечения – формирование уретральной площадки из трансплантата слизистой ротовой полости – был выполнен всем 18 пациентам. В двух случаях он сочетался с реконструкцией суженного отверстия ранее сформированной перинеостомы. В 10 случаях потребовалось использование двух графтов слизистой щеки, забранных по одному с каждой стороны. У остальных 8 пациентов для первого этапа было достаточно использование одного буккального графта. В каждом случае при заборе трансплантата слизистой из ротовой полости старались получить его максимальный размер. Длина буккального графта обычно составляла 5 – 9 см, а ширина 2,5-4 см. В каждом случае форма последнего была прямоугольной. Именно такие параметры являются наиболее оптимальными. Окончательные максимальные размеры трансплантата слизистой щеки, которые можно получить, зависели от конституции больного и размеров его ротовой полости. Именно забор графта максимального размера из ротовой полости с последующей его пересадкой на хорошо подготовленную белочную оболочку полового члена обеспечивают максимальную вероятность выполнения тубуляризации уретральной площадки без необходимости выполнения коррекции новой уретральной площадки.
Коррекция уретральной площадки новым графтом слизистой ротовой полости потребовалась 6 пациентам. Двум пациента из 6 коррекция площадки неоуретры сочеталась с реконструкций наружного отверстия уретрокутанеостомы. Одному пациенту коррекционную операцию пришлось производить дважды. В двух случаях в связи с дефицитом слизистой внутренней поверхности щек графт для операции был получен с нижней поверхности языка.
У одного пациента с поражением мембранозного отдела, первый этап операции у которого включал формирование уретральной площадки из двух графтов, фиксированных в проекции мембранозного и проксимальной части бульбозного отделов уретры произошел полный некроз проксимального лоскута с последующим рубцеванием в этой зоне и стеноз перинеостомы.
Таким образом, первичное приживление новой уретральной площадки произошло у 11 (61,1%) пациентов, коррекция уретральной площадки после первого этапа оперативного вмешательства потребовалась в 6 (33,3%) случаях, у одного пациента (5,6%) произошел некроз графта.
Суммируя данные первичного приживления и положительных результатов коррекции новой уретральной площадки, общая эффективность первого этапа, т.е. возможность последующей тубуляризации неоуретры, составила 94,4%.
Медиана времени между этапами составила 7,5 месяцев.
Финальный этап заместительной (многоэтапной) уретропластики был выполнен 16 пациентам. Один пациент отказался от выполнения операции в связи с удовлетворительным качеством жизни, имея сформированную во время первого этапа перинеостому. При этом новая уретральная площадка у него полностью прижилась и была готова к тубуляризации. У одного пациента, как было сказано ранее, произошел полный некроз дистального графта.
У 15 пациентов после тубуляризации новой уретральной площадки удалось полностью заместить изначально пораженный отдел уретры. У одного больного отмечено прорезывание и несостоятельность швов на головке полового члена, в связи с чем, наружное отверстие уретры сформировалось в дистальной части ствола полового члена.
Дренирование мочевого пузыря после операции продолжалось от двух до трех недель в зависимости от результатов перикатетерной уретрографии и заживления тканей в зоне операции.
У одного пациента на 18 сутки после операции сформировался уретрокожный свищ точечного размера. Пациенту была выполнена троакарная цистостомия. Уретральный катетер был удален, а дренирование мочевого пузыря продолжилось через надлобковый свищ в течение дополнительных 2,5 недель, после чего уретрокожный свищ самостоятельно зажил и цистостомический дренаж был удален. У пациента восстановилось самостоятельное мочеиспускание.
Таким образом, эффективность тубуляризации (финального этапа) составила 93,8%, а общая эффективность многоэтапной (заместительной) уретропластики – 88,2%.
Четыре пациента спустя 6 месяцев не явились на контрольное обследование. Медиана наблюдения оставшихся 11 больных составила 14 месяцев. Ни одному из пациентов за время наблюдения не потребовалось каких-либо инструментальных вмешательств на уретре.
Всем больным выполнялась урофлоуметрия сразу после удаления уретрального катетера, через 6 и 12 месяцев после операции.
Отмечена положительная динамика среднего значения показателя Qmax в течение года после операции (табл. 2).
Таблица 2. Динамика показателей максимальной скорости мочеиспускания после многоэтапной уретропластики
| Показатель | после удаления катетера |
6 месяцев после операции |
12 месяцев после операции |
|---|---|---|---|
| Q max, мл/с | 19,9 + 1,5 | 18,82 + 1,1 | 16,6 + 0,5 |
| p | = 0,84 | = 0,12 | |
| = 0,14 | |||
ОБСУЖДЕНИЕ
Сегодня для лечения подавляющего большинства стриктур уретры применяется одноэтапная уретропластика. Но каждый десятый пациент имеет хотя бы один осложняющий фактор, который исключает выполнение последней [1]. Прежде всего это наличие выраженных изменений местных тканей, таких как:
- массивный спонгиофиброз, как последствие BXO;
- рубцовое изменение окружающих тканей, как результат предшествующих неудачных операций, в том числе и по поводу гипоспадии в детстве;
- уретрокожные свищи;
- протяженные облитерации уретры;
- абсцесс и инфекция парауретральных тканей.
Эффективность многоэтапной операции по данным литературы составляет 73% – 100% (табл. 3) [3-9].
Таблица 3.Мировые результаты многоэтапной уретропластики
| Автор, год |
Количество пациентов |
Используемый графт |
Медиана наблюдения, мес. |
Эффективность |
|---|---|---|---|---|
| Mundy, 1998 [5] |
16 | Буккальный графт |
36 | 93,8% |
| Andrich, 2003 [3] |
58 | Буккальный графт или кожа |
6 | 98% |
| Dubey, 2005 [4] |
15 | Буккальный графт |
24.2 | 86,7% |
| Dubey, 2005 [6] |
14 | Буккальный графт |
32.5 | 78,6% |
| Levin, 2007 [7] |
5 | Буккальный графт |
36 | 80% |
| Meeks, 2008 [8] |
6 | Кожа |
17 | 100% |
| Kulkarni, 2009 [9] |
15 | Слизистая ротовой полости |
56 | 73% |
| Котов, 2015 Наст исслед. |
18 | Буккальный графт |
14 | 88,2% |
С. Chapple и соавт. [2] проанализировали 66 работ, отвечающим критериям для включения в метаанализ и сделали вывод, что эффективность многоэтапной уретропластики среди 129 суммированных пациентов составляет 90,5%. Полученный внашем исследовании положительный результат (88,2%) сопоставим с мировыми данными. К сожалению, в приведенном выше мета-анализе не указана частота коррекции уретральной площадки после первого этапа. В нашей работе она составила 35,3%. В одной из наиболее крупных работ, посвященных многоэтапной уретропластике, D.E. Andrich и соавт. показали, что после 103 операций по формированию новой уретральной площадки ревизия последней понадобилась в 39 (37,8%) случаях [3]. В работе D. Dubey и соавт. отмечено, что коррекция уретральной площадки пришлось выполнять 5 пациентам из 17, что составило 29,4% [4].
D.E. Andrich и соавт. выделяют сл. причины, которые могли повлиять на плохое приживление лоскута [3]:
- эрекции в раннем послеоперационном периоде, которые могут провоцировать кровотечение и растяжение трансплантата, приводящие к изменению натяжения краев графта с кожей и подлежащим основанием и, следовательно, нарушению процессов неоваскуляризации;
- прогрессирование BXO, особенно в зоне уретростомы, вызывая ее стеноз;
- сморщивание графта на головке полового члена (фиксация последнего происходит на растянутой головке полового члена, а после операции последняя сокращается, приводя к сморщиванию к развитию контрактуры свободного лоскута).
Исходя из собственного опыта, считаем, что ранее существующие выводы о причинах сморщивания и рубцевания графта после первого этапа не совсем точны.
По нашему мнению, основной причиной сморщивания графта после первого этапа уретропластики является нарушение неоваскуляризации, которое зависит от качества питающего ложа, на который пересаживается трансплантат. Следовательно, дефекты в хирургической технике подготовки белочной оболочки кавернозных тел перед пересадкой и будут определять риски сморщивания графта. Неполное удаление собственной измененной уретральной площадки, остатков пораженного рубцовым процессом спонгиозного тела, эпителизированных рубцовых псевдодивертикулов и тканей будут нарушать приживление свободного лоскута. Иссечение измененных тканей должно производиться до здоровых краев уретры, по краям хорошо кровоснабжаемой мясистой оболочки и чистой белочной оболочки кавернозных тел. Тщательный гемостаз и хорошая фиксация графта позволяют избежать гематом, смещение трансплантата в раннем послеоперационном периоде, даже при возникновении эрекции, что снижает риски контрактуры графта.
Учитывая возможность эрекции в раннем послеоперационном периоде, графт фиксировали к подлежащему ложу – белочной оболочки полового члена – большим количеством швов. В дополнение к этому давящая повязка с тампоном, которая накладывалась на буккальный трансплантат, сохранялась на протяжении 7 дней после операции. Все это предотвращало смещение графта относительно подлежащего питающего ложа.
Прогрессия BXO является возможной причиной стеноза уретростомы и контрактуры лоскута. В нашей группе был всего лишь один пациент с лихен склерозом, при этом коррекция уретральной площадки после первого этапа ему не понадобилась.
Во всех 6 случаях коррекции уретральной площадки сморщивание происходило в ее основной части, и лишь в одном случае в сморщивающий процесс была вовлечена головка полового члена.
Выполнение финального этапа – заместительной уретропластики – должно выполняться не ранее 6-9 месяцев после последней операции.
Выбор подлежащего питающего ложа является залогом успеха удачной тубуляризации новой уретральной площадки, т.е. заключительного этапа оперативного вмешательства. Для сохранения кровообращения по краям площадки и в окружающих тканях фиксация графта должна происходить как на белочную оболочку кавернозных тел, так и на мясистую оболочку полового члена. Мясистая оболочка полового члена должна быть питающим ложем для 1/3 – 1/4 части лоскута с каждой стороны (рис. 5). Это позволит мобилизовать края уретральной площадки, не повредив кавернозные тела и получив для тубуляризации свободные края неоуретры достаточного размера с сохраненным кровоснабжением (рис. 6).
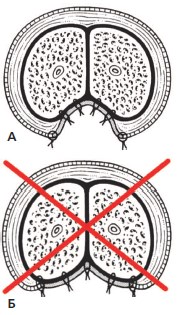
Рис. 5 А, Б. Фиксация графта на питающую основу по время первого этапа: А – правильная техника (края графта ложатся на мясистую оболочку полового члена); Б – неправильная техника (графт по всей ширине фиксирован к белочной оболочке кавернозных тел)
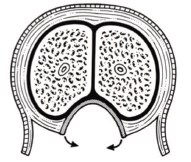
Рис.6. Правильная мобилизация краев новой уретральной площадки для ее тубуляризации при многоэтапной операции графт фиксирован к белочной оболочке кавернозных тел)
Ушивание послеоперационной раны над вновь сформированной неоуретрой должно происходить в несколько слоев для предотвращения формирования уретрокожного свища. Важными факторами профилактики фистулы является тщательный гемостаз и мероприятия, направленные на снижение рисков инфекционных осложнений: использование силиконового катетера маленького диаметра, антибактериальная профилактика и терапия, туалет послеоперационной раны и по возможности раннее удаление уретрального катетера.
Все эти хирургические приемы позволяют добиться высоких положительных результатов многоэтапной уретропластики, зачастую являющейся последним шансом пациента на восстановление самостоятельного мочеиспускания.
ВЫВОДЫ
Многоэтапная уретропластика является длительным, но эффективным методом лечения сложных стриктур уретры. В подавляющем большинстве случаев она применяется после неоднократных неудачных эндоскопических и открытых реконструктивных вмешательств на уретре. Только полное удаление измененных тканей и выполнение многоэтапного подхода позволяет в конечном итоге восстановить самостоятельное мочеиспускание. Многократные попытки выполнить уретропластику в один этап могут привести к значимому нарушению локального кровоснабжения уретры и тканей, а также дефициту пластического материала для формирования неоуретры. Важным моментом является тот факт, что после первого этапа операции может потребоваться коррекция вновь образованной уретральной площадки. Часто заместительная уретропластика является последним шансом пациента на восстановление самостоятельного мочеиспускания. В некоторых случаях восстановление необструктивного мочеиспускания через перинеостому, удовлетворяет пациентов и обеспечивает им высокое качество жизни.
ЛИТЕРАТУРА
- Carr LK, Webster GD. Urethral strictures. In: Krane RJ, Siroky MB, Fitzpatrick JM, editors.// Operative Urology: Surgical skills. Philadelphia: Churchill Livingstone. 2000. Р. 287.
- Chapple C, Andrich D, Atala A, Barbagli G, Cavalcanti A, Kulkarni S, Mangera A, Nakajima Y. SIU/ICUD Consultation on Urethral Strictures: The management of anterior urethral stricture disease using substitution urethroplasty. // Urology. 2014. Vol. 83 (3 Suppl). P. 31-47.
- Andrich DE, Greenwell TJ, Mundy AR. The problems of penile urethroplasty with particular reference to 2-stage reconstructions. // J Urol. 2003. Vol. 170. P. 87–89.
- Dubey D, Kumar A, Mandhani A, Srivastava A, Kapoor R, Bhandari M. Buccal mucosal urethroplasty: a versatile technique for all urethral segments. // BJU Int. 2005. Vol. 95. P. 625–629.
- Venn SN, Mundy AR. Urethroplasty for balanitis xerotica obliterans. // Br J Urol. 1998. Vol. 81. P. 735–737.
- Dubey D, Sehgal A, Srivastava A, Mandhani A, Kapoor R, Kumar A. Buccal mucosal urethroplasty for balanitis xerotica obliterans related urethral strictures: The outcome of 1 and 2-stage techniques. // J Urol. 2005. Vol. 173. P. 463–466.
- Levine LA, Strom KH, Lux MM. Buccal mucosa graft urethroplasty for anterior urethral stricture repair: evaluation of the impact of stricture location and lichen sclerosus on surgical outcome. // J Urol. 2007. Vol. 178. P. 2011–2015.
- Meeks JJ, Erickson BA, Gonzalez CM. Full-thickness abdominal skin graft for long-segment urethral stricture reconstruction. // Int Braz J Urol. 2008. Vol. 34. P. 602–607.
- Kulkarni S, Barbagli G, Kirpekar D, Mirri F, Lazzeri M. Lichen sclerosus of the male genitalia and urethra: surgical options and results in a multicenter international experience with 215 patients. // Eur Urol. 2009. Vol. 55. P. 945–956.
Статья опубликована в журнале"Экспериментальная и клиническая урология" №4 2015, стр.60-66











Комментарии