Синюхин В.Н., Стецюк Е.А., Арзуманов С.В.
Уремический синдром сопровождается накоплением в организме больного большого количества различного рода соединений, которые у здоровых людей экскретируются с мочой. Эти вещества принято называть уремическими токсинами. Считают, что они оказывают отрицательное влияние на биологические функции организма. Для удобства эти соединения принято делить на 3 группы:
1. Водорастворимые соединения с небольшим молекулярным весом, прототипом которых является мочевина;
2. Большие пептиды с молекулярным весом более 500 Da, которые принято называть средними молекулами, например, бета-2-микроглобулин;
3. Связанные с белком соединения, например, производные фенола или индола [1]. Каждое вещество, которое мы называем уремическим токсинам должно отвечать соответствующим критериям. Согласно классическому определению, данному Mastry S. и описанному Bergstrom J. [2] и совсем недавно одобренному группой EROTOX во главе с Vanholder R., к этим веществам относятся химически идентифицированные структуры, присутствующие в биологических жидкостях и поддающиеся количественному и качественному определению со следующими характеристиками:.
- их содержание в крови и тканях у уремических больных должно во много раз превышать такие же концентрации у здоровых людей;
- высокое содержание этих веществ в тканях должно коррелировать с развитием уремических симптомов;
- токсический эффект этих субстанций в диапазонах концентраций определяемых в тканях уремического больного должен быть подтвержден в опытах на лабораторных животных и в опытах in vitro;
- концентрации, используемые в экспериментах, должны соответствовать таковым у больных с хронической почечной недостаточностью [3, 4]
ТОКСИНЫ, СВЯЗАННЫЕ С БЕЛКОМ
Среди всех токсинов до последнего времени наименьшее внимание уделялось уремическим токсинам связанным с белком. Это было обусловлено тем, что они не выводятся во время стандартного диализа и связь с белком не позволяет реализовать их токсический эффект, так как он обусловлен только свободной фракцией. Работы последних лет показали наличие токсических свойств у этих веществ - уремических токсинов в связанном состоянии, и поэтому начались исследования по разработке методов их удаления из организма больного. В первой части этого обзора мы коснемся классификации этих веществ, а затем будем обсуждать возможности их выведения или уменьшения их содержания в крови больных.
Интенсивные исследования по идентификация связанных с белком соединений у больных с почечной недостаточностью начали проводится лишь в последние годы . Это связано с тем, что недавно было установлено, что эти вещества интенсивно вмешиваются в основные обменные процессы [5]. В таблице 1 представлены основные связанные с белком уремические вещества, обладающие выраженным токсическим эффектом.
Остановимся на двух веществах, которым уделяется наибольшее внимание при исследовании уремических токсинов - это пара-крезол (р-крезол) и индоксил-сульфат. Концентрация этих веществ в сыворотке крови увеличивается по мере ухудшения почечной функции и коррелирует с уровнем гломерулярной фильтрации [7, 8, 9, 10]. В опытах in vitro был продемонстрирован их токсический эффект [11]. Оказалось, что эти структуры являются факторами риска смертности при ХПН [8, 9, 10].
Установлено, что индоксил сульфат и р-крезол сульфат образуются в кишечнике. При воздействии кишечных бактерий на непереваренные белки синтезируется большое количество индолов и фенолов. Их накопление приводит к нарушению многих функций человеческого организма. Эти два соединения являются прототипами целого семейства связанных с белками уремических токсинов [12, 13].
В кишечнике триптофан метаболизируется кишечной флорой до индола, а после всасывания в печени образуется индоксил сульфат. Р-крезол возникает в результате метаболизма тирозина и фенилаланина, затем образуется 4-гидроксифенилуксусная кислота, при декарбоксилировании которой синтезируется р-крезол [14, 15]. После прохождения через слизистую кишечника под воздействием цитозолевой сульфотрансферазы образуется р-крезол сульфат. Р-крезол присутствует в кровотоке в виде этого конъюгата (рис. 1). В большинстве клинических исследованиях р-крезол определялся после кислотного гидролиза, в результате которого из одной молекулы р-крезол сульфата образуется одна молекула р-крезола, что и позволило судить о непосредственном содержании основного уремического токсина р-крезола [16, 17].
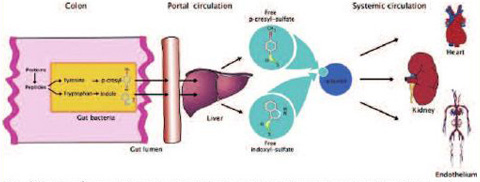
Рис. 1. Схема образования индоксил-сульфата и пара-крезола в организме человека [13].
Оба токсина экскретируются почками путем тубулярной канальцевой секреции, поэтому они накапливаются в крови больных с нарушенной функцией почек [18, 19]. Считают, что эти два вещества оказывают непосредственное повреждающее действие на почечную паренхиму путем индукции воспалительного процесса за счёт усиления экспрессии профибротических цитокинов таких, как трансформирующий фактор роста бета 1 (TFG 1) [20, 21].
Таблица 1. Уремические токсины и их биологические эффекты [6]
| Уремический токсин | Биологический эффект |
| AGE (advanced glycation end products) - конечные продукты гликозилирования |
Воспаление, сосудистые заболевания |
| CMPF (carboxy-methyl-propyl-furanpropionic acid)-фуранкарбоксиловая кислота |
Влияние на связывание с белком лекарственных соединений, влияние на детоксификацию, нейропатия, анемия |
| Цитокины | Воспаление, нарушение питания, анемия |
| Диметилгуанидины | Торможение активности кальций-АТФ-азы |
| Гиппуровая кислота | Влияние на связывание с белком лекарственных веществ, снижение толерантности к глюкозе |
| Гомоцистеин | Заболевания сосудов, влияние на детоксификацию |
| Индол-3-уксусная кислота | Влияние не связывание с белком лекарственных веществ, нейропатия, цитотоксичность |
| Индоксил-сульфат | Снижение почечной функции, функции щитовидной железы, влияние на связывание с белком лекарственных веществ, влияние на детоксификацию, нарушение функции эндотелия и репаративных процессов, индукция оксидативного стресса, стимуляция процесса кальцификации аорты, торможение пролиферации гладкомышечных волокон, стимуляция процесса резистентности остеокластов к паратгормону. |
| Кинуренин | Нейропатия |
| Лептин | Нарушение питания |
| Пара-крезол сульфат (p-крезол) | Воспаление, увеличение количества свободных радикалов, выделение эндотелиальных микрочастиц. |
| Фенолы | Нарушение функции иммунной системы, нейропатия |
| Фенилуксусная кислота | Торможение синтеза NO |
| Хинолиновая кислота | Нейропатия |
Показано, что введение индоксил сульфата крысам вызывало развитие фиброза почек [22], а его введение крысам с повышенным артериальным давлением приводило к экспрессии трансмембранного белка клеток, провоцировало старение клеток, сопровождавшееся фиброзом почечной паренхимы [23].
Существует огромное количество токсинов, имеющих прямое отношение к развитию сердечно-сосудистых нарушений на фоне уремии. Уже давно было показано, что р-крезол in vivo оказывает прямое воздействие на функцию эндотелиального барьера, пролиферацию эндотелиальных клеток и репаративные процессы в ране, но до сих пор не доказано повреждающее действие р-крезол сульфат на клетки сосудов in vitro [24, 25].
С другой стороны известно, что р-крезол сульфат, а не р-крезол оказывает провоспалительный эффект на нестимулированные лейкоциты in vitro, что позволяет предположить наличие прямого повреждающего действия р-крезол сульфата на сосуды больных с заболеваниями почек [26].
Кроме выраженного профибротического эффекта, индоксил сульфат способствует хроническим заболеваниям сосудов путем торможения репаративных процессов в эндотелии и стимуляции пролиферации гладкомышечных клеток [27]. Индоксил сульфат может вызывать дисфункцию эндотелия, так как способен провоцировать оксидативный стресс и индукцию процесса сенесценции эндотелия [28]. В последних исследованиях были получены парадоксальные результаты, которые показали, что в отличие от хронического заболевания почек, на фоне которых индоксил сульфат оказывал прооксидантный эффект, при нормальных физиологических условиях он обладал антиоксидантными свойствами [29].
До последнего времени выведение из организма соединений связанных с белком считалось безнадежной задачей. Высокопоточный диализ не показывал преимущества перед стандартным гемодиализом, то есть практически не был способен удалять эти вещества. Напротив, ежедневный, проводившийся в течение длительного времени гемодиализ приводил к снижению содержания этих соединений в крови [30]. Только недавно было показано, что оптимальная конвективная стратегия гемодиализа позволяет выводить значительно большее количество связанных с белком уремических токсинов по сравнению со стандартным диализом на фоне гемодиафильтрации [31]. В остром эксперименте было продемонстрировано преимущество этой тактики по сравнению с гемодиализом на высокопроницаемых мембранах, причем постдилюционная гемодиафильтрация имела большие преимущества по сравнению с преддилюционной гемодиафильтрацией [32, 33].
Было установлено, что постдилюционная гемодиафильтрация в большей степени уменьшала преддиализные концентрации связанных с белком уремических токсинов по сравнению с гемодиализом на высокопроницаемых мембранах. Однако если результаты острого эксперимента продемонстрировали выраженное уменьшение содержания этих веществ, длительное применение этой технологии диализа показало неоднозначные результаты [34].
В последние годы начались разработки методов по удалению уремических токсинов через кишечник. Известно, что индолы и р-крезол вырабатываются в кишечнике из аминокислот кишечной флорой. Причем при уменьшении фильтрационной функции почек синтез этих соединений усиливается [35, 36]. Известно, что содержание уремических токсинов тесно связанных с белком у больных ХПН можно уменьшить соблюдением безбелковой диеты, применением пробиотиков и сорбентов [37, 3, 39]. Все эти методики уменьшают количество уремических токсинов, но до сих пор не было показано, что они улучшают состояние больного.
В настоящее время наибольшего внимания заслуживает сорбент AST- 120, который уменьшает не только концентрацию индоксил-сульфата [40] и других уремических токсинов связанных с белком [41], но и позволяет отложить время начала программного гемодиализа у больного с ХПН [42], замедлить процесс снижения гломерулярной фильтрации [43], и приводит к увеличению продолжительности жизни больного после начала диализной терапии [44].
Следует отметить, что методы экстракорпоральной адсорбции в этом плане являются определяющими. Интересны исследования по фракционной сепарации плазмы больных ХПН с последующей адсорбцией на аппарате, напоминающим по функции искусственную печень. На группе уремических больных была продемонстрирована выраженная абсорбция на специальных сорбентах связанных с белком уремических токсинов [45]. Однако сорбционная терапия осложнилась возникновением тромбозов из-за одновременного выведения из организма антитромботических факторов [46]. Перитонеальный диализ по клиренсовым характеристикам не продемонстрировал преимущества перед высокопоточным гемодиализом [47]. Однако при перитонеальном диализе в крови наблюдаются невысокие концентрации связанных с белком уремических токсинов на фоне их низких клиренсов [48]. Считают, что при этом виде диализа должна быть более низкая способность кишечной флоры вырабатывать токсины [49]. Трансплантация почки приводит к снижению концентрации в крови р-крезола и индоксил сульфата, что коррелируют с уровнем гломерулярной фильтрации пересаженной почки [50].
ЗАКЛЮЧЕНИЕ
Накапливается все большее количество информации о повреждающем эффекте на сердечно-сосудистую систему и другие органы больного ХПН связанных с белком уремических токсинов. Лабораторные и клинические данные показывают, что имеется взаимосвязь между концентрацией этих веществ, клиническим течением и исходом заболевания. Удаление этих соединений из организма больного сильно ограничено при применении стандартного гемодиализа, но может быть оптимизировано при применении конвекционных методов их выведения. Добавляет оптимизм и разработка методов воздействия на метаболизм кишечных бактерий и интерстенальных адсорбентов, удаляющих продукты их жизнедеятельности. Трансплантация почки приводит и к снижению концентрации уремических токсинов. Не вызывает сомнения тот факт, что концентрация в организме больного ХПН связанных с белком уремических токсинов увеличивается при снижении скорости гломерулярной фильтрации.
ЛИТЕРАТУРА
1. Vanholder R, De Smet R, Glorieux G, Argilés A, Baurmeister U, Brunet P, Clark W, Cohen G, De Deyn PP, Deppisch R, Descamps-Latscha B, Henle T, Jörres A, Lemke HD, Massy ZA, Passlick-Deetjen J, Rodriguez M, Stegmayr B, tenvinkel P, Tetta C, Wanner C, Zidek W. Review on uremic toxins: classification, concentration, and interindividual variability. // Kidney Int. 2003. Vol. 63, N 5. P.1934-1943.
2. Bergstrom J, Furst P. Uremic toxins. // Kidney Int Suppl. 1978. Vol. 8. P. 9-12
3. Rutkowski P. Kliniczne i metaboliczne nastêpstwa zatrucia mocznicowego. // Przegl Lek. 2006. Vol. 63, N 4. P. 209-217.
4. Vanholder R, De Smet R, Lameire NH. Redesigning the map of uremic toxins. // Contrib Nephrol. 2001. Vol. 133. P. 42-70.
5. Jourde-Chiche N, Dou L, Cerini C, Dignat-George F, Vanholder R, Brunet P. Proteinbound toxins—update 2009. // Semin Dial. 2009. Vol. 22, N 4. P. 334-339.
6. Vanholder R, Schepers E, Pletinck A, Neirynck N, Glorieux G. An Update on Protein- Bound Uremic Retention Solutes . // J Ren Nutr. 2012. Vol 22, N 1. P. 90-94.
7. De Smet R, David F, Sandra P, Van Kaer J, Lesaffer G, Dhondt A, Lameire N, Vanholder R. A sensitive HPLC method for the quantification of free and total p-cresol in patients with chronic renal failure. // Clin Chim Acta. 1998. Vol. 278, N 1. P. 1-21.
8. Liabeuf S, Barreto DV, Barreto FC, Meert N, Glorieux G, Schepers E, Temmar M, Choukroun G, Vanholder R, Massy ZA. Free p-cresylsulphate is a predictor of mortality in patients at different stages of chronic kidney disease. // Nephrol Dial Transplant. 2010. Vol. 25, N 4. P. 1183–1191.
9. Barreto FC, Barreto DV, Liabeuf S, Meert N, Glorieux G, Temmar M, Choukroun G, Vanholder R, Massy ZA. Serum indoxyl sulfate is associated with vascular disease and mortality in chronic kidney disease patients. // Clin J Am Soc Nephrol. 2009. Vol. 4, N 10. P. 1551–1558.
10. Meijers BK, Claes K, Bammens B, de Loor H, Viaene L, Verbeke K, Kuypers D, Vanrenterghem Y, Evenepoel P. p-Cresol and cardiovascular risk in mild-to-moderate kidney disease. // Clin J Am Soc Nephrol. 2010. Vol. 5, N 7. P. 1182–1189.
11. Vanholder R, Massy Z, Argiles A, Spasovski G, Verbeke F, Lameire N. Chronic kidney disease as cause of cardiovascular morbidity and mortality. // Nephrol Dial Transplant. 2005. Vol. 20, N 6. P. 1048–1056.
12. Vanholder R, van Laecke S, Glorieux G. What is new in uremic toxicity? // Pediatr Nephrol. 2008. Vol. 23, N 8. P. 1211–1221.
13. Meijers BK, Evenepoel P. The gut–kidney axis: indoxyl sulfate, p-cresyl sulfate and CKD progression. // Nephrol Dial Transplant. 2011. Vol. 26, N 3. P. 759-761.
14. De Smet R, van Kaer J, van Vlem B, de Cubber A, Brunet P, Lameire N, Vanholder R. Toxicity of free p-cresol: A prospective and cross-sectional analysis. // Clin Chem. 2003. Vol. 49, N 3. P. 470–478.
15. Curtius HC, Mettler M, Ettlinger L. Study of the intestinal tyrosine metabolism using stable isotopes and gas chromatography-mass spectrometry. // J Chromatogr. 1976. Vol. 126. P. 569–580.
16. Burchell B, Coughtrie MW. Genetic and environmental factors associated with variation of human xenobiotic glucuronidation and sulfation. // Environ Health Perspect. 1997. Vol. 105, Suppl. 4. P. 739–747.
17. Vanholder R, Bammens B, de Loor H, Glorieux G, Meijers B, Schepers E, Massy Z, Evenepoel P. Warning: The unfortunate end of p-cresol as a uraemic toxin.// Nephrol Dial Transplant. 2011. Vol. 26, N 5. P. 1464–1467.
18. Niwa T. Phenol and p-cresol accumulated in uremic serum measured by HPLC with fluorescence detection. // Clin Chem. 1993. Vol. 39, N 1. P. 108–111. 19. De Smet R, David F, Sandra P, van Kaer J, Lesaffer G, Dhondt A, Lameire N, Vanholder R. A sensitive HPLC method for the quantification of free and total p-cresol in patients with chronic renal failure. // Clin Chim Acta. 1998. Vol. 278, N 1. P. 1–21.
20. Niwa T, Ise M. Indoxyl sulfate, a circulating uremic toxin, stimulates the progression of glomerular sclerosis. // J Lab Clin Med. 1994. Vol. 124, N 1. P. 96–104.
21. Miyazaki T, Ise M, Hirata M, Endo K, Ito Y, Seo H, Niwa T. Indoxyl sulfate stimulates renal synthesis of transforming growth factor-beta 1 and progression of renal failure. // Kidney Int Suppl. 1997. Vol. 63. P. 211–214.
22. Enomoto A, Takeda M, Tojo A, Sekine T, Cha SH, Khamdang S, Takayama F, Aoyama I, Nakamura S, Endou H. Role of organic anion transporters in the tubular transport of indoxyl sulfate and the induction of its nephrotoxicity.// J Am Soc Nephrol. 2002. Vol. 13, N 7. P. 1711–1720.
23. Adijiang A, Shimizu H, Higuchi Y, Nishijima F, Niwa T. Indoxyl sulfate reduces klotho expression and promotes senescence in the kidneys of hypertensive rats. // J Ren Nutr. 2011. Vol. 21, N 1. P. 105–109.
24. Dou L, Bertrand E, Cerini C, Faure V, Sampol J, Vanholder R, Berland Y, Brunet P. The uremic solutes p-cresol and indoxyl sulfate inhibit endothelial proliferation and wound repair. // Kidney Int. 2004. Vol. 65, N 2. P. 442–451.
25 Cerini C, Dou L, Anfosso F, Sabatier F, Moal V, Glorieux G, de Smet R, Vanholder R, Dignat-George F, Sampol J. P-cresol, a uremic retention solute, alters the endothelial barrier function in vitro. // Thromb Haemost. 2004. Vol. 92, N 1. P. 140–150.
26. Schepers E, Meert N, Glorieux G, Goeman J, van der Eycken J, Vanholder R. P-cresylsulphate, the main in vivo metabolite of p-cresol, activates leucocyte free radical production. // Nephrol Dial Transplant. 2007. Vol. 22, N 2. P. 592–596.
27. Dou L, Bertrand E, Cerini C, Faure V, Sampol J, Vanholder R, Berland Y, Brunet P. The uremic solutes p-cresol and indoxyl sulfate inhibit endothelial proliferation and wound repair. // Kidney Int. 2004. Vol. 65, N 2. P. 442–451.
28. Yu M, Kim YJ, Kang DH. Indoxyl sulfate-induced endothelial dysfunction in patients with chronic kidney disease via an induction of oxidative stress. // Clin J Am Soc Nephrol. 2011. Vol. 6, N 1. P. 30–39.
29. Miyamoto Y, Watanabe H, Otagiri M, Maruyama T. New insight into the redox properties of uremic solute indoxyl sulfate as a pro- and anti-oxidant. // Ther Apher Dial. 2011. Vol. 15, N 2. P. 129–131.
30. Fagugli RM, De Smet R, Buoncristiani U, Lameire N, Vanholder R. Behavior of nonprotein- bound and proteinbound uremic solutes during daily hemodialysis. //Am J Kidney Dis. 2002. Vol. 40, N 2. P. 339-347.
31. Meert N, Beerenhout C, Schepers E, Glorieux G, Kooman J,Vanholder R. Evolution of protein-bound uraemic solutes during predilution haemofiltration. // J Nephrol. 2009. Vol.22, N 3. P. 352-357.
32. Meert N, Eloot S, Schepers E, Lemke HD, Dhondt A, Glorieux G, Van Landschoot M, Waterloos MA, Vanholder R. Comparison of removal capacity of two consecutive generations of high flux dialysers during different treatment modalities. // Nephrol Dial Transplant. 2011. Vol. 26, N 8. P. 2624-2630.
33. Meert N, Eloot S, Waterloos MA, Van Landschoot M, Dhondt A, Glorieux G, Ledebo I, Vanholder R. Effective removal of protein-bound uraemic solutes by different convective strategies: a prospective trial. // Nephrol Dial Transplant. 2009. Vol. 24, N 2. P. 562-570.
34. Meert N, Waterloos MA, Van Landschoot M, Dhondt A, Ledebo I, Glorieux G, Goeman J, Van der Eycken J, Vanholder R. Prospective evaluation of the change of predialysis protein- bound uremic solute concentration with postdilution online hemodiafiltration. // Artif Organs. 2010. Vol. 34, N 7. P. 580-58.
35. Schepers E, Glorieux G, Vanholder R. The gut: the forgotten organ in uremia? // Blood Purif. 2010. Vol. 29, N 2. P. 130-136.
36. Bammens B, Verbeke K, Vanrenterghem Y, Evenepoel P. Evidence for impaired assimilation of protein in chronic renal failure.// Kidney Int. 2003. Vol. 64, N 6. P. 2196-2203.
37. Ling WH, Hanninen O. Shiing from a conventional diet to an uncooked vegan diet reversibly alters fecal hydrolytic activities in humans.// J Nutr. 1992. Vol. 122, N 4. P. 924- 930.
38. Birkett A, Muir J, Phillips J, Jones G, O’Dea K. Resistant starch lowers fecal concentrations of ammonia and phenols in humans. // Am J Clin Nutr. 1996. Vol. 63, N 5. P. 766-772.
39. Meijers BK, De Preter V, Verbeke K, Vanrenterghem Y, Evenepoel P. p-Cresyl sulfate serum concentrations in haemodialysis patients are reduced by the prebiotic oligofructoseenriched inulin. // Nephrol Dial Transplant. 2010. Vol. 25, N 1. P. 219-224.
40. Schulman G, Agarwal R, Acharya M, Berl T, Blumenthal S, Kopyt N. A multicenter, randomized, doubleblind, placebo-controlled, dose-ranging study of AST-120 (Kremezin) in patients with moderate to severe CKD. // Am J Kidney Dis. 2006. Vol. 47, N 4. P. 565-577.
41. Kikuchi K, Itoh Y, Tateoka R, Ezawa A, Murakami K, Niwa T. Metabolomic search for uremic toxins as indicators of the effect of an oral sorbent AST-120 by liquid chromatography/ tandem mass spectrometry. // J Chromatogr B Analyt Technol Biomed Life Sci. 2010. Vol. 878, N 20. P. 2997-3002.
42. Ueda H, ShibaharaN, Takagi S, Inoue T, Katsuoka Y. AST- 120, an oral adsorbent, delays the initiation of dialysis in patients with chronic kidney diseases. // Ther Apher Dial. 2007. Vol. 11, N 3. P. 189-195.
43. Akizawa T, Asano Y, Morita S, Wakita T, Onishi Y, Fukuhara S, Gejyo F, Matsuo S, Yorioka N, Kurokawa K. Effect of a carbonaceous oral adsorbent on the progression of CKD: a multicenter, randomized, controlled trial. // Am J Kidney Dis. 2009. Vol. 54, N 3. :P. 459- 467.
44. Ueda H, Shibahara N, Takagi S, Inoue T, Katsuoka Y. AST-120 treatment in pre-dialysis period affects the prognosis in patients on hemodialysis. // Ren Fail. 2008. Vol. 30, N 9. P. 856-860. 45. Meijers BK, Weber V, Bammens B, Dehaen W, Verbeke K, Falkenhagen D, Evenepoel P. Removal of the uremic retention solute p-cresol using fractionated plasma separation and adsorption. // Artif Organs. 2008. Vol. 32, N 3. P. 214-219.
46. Meijers BK, Verhamme P, Nevens F, , Hoylaerts MF, Bammens B, Wilmer A, Arnout J, Vanrenterghem Y, Evenepoel P. Major coagulation disturbances during fractionated plasma separation and adsorption. //Am J Transplant. 2007. Vol. 7, N 9. P. 2195-2199.
47. Evenepoel P, Bammens B, Verbeke K, Vanrenterghem Y. Superior dialytic clearance of beta(2)-microglobulin and p-cresol by high-flux hemodialysis as compared to peritoneal dialysis. // Kidney Int. 2006. Vol. 70, N 4. P. 794-799.
48. Pham NM, Recht NS, Hostetter TH, Meyer TW. Removal of the protein-bound solutes indican and p-cresol sulfate by peritoneal dialysis. // Clin J Am Soc Nephrol. 2008. Vol. 3, N 1. P. 85-90.
49. Vanholder R, Meert N, Van Biesen W, Meyer T, Hostetter T, Dhondt A, Eloot S. Why do patients on peritoneal dialysis have low blood levels of proteinbound solutes? // Nat Clin Pract Nephrol. 2009. Vol. 5, N 3. P. 130-131.
50.Huang ST, Shu KH, Cheng CH, Wu MJ, Yu TM, Chuang YW, Chen CH. Serum total pcresol and indoxyl sulfate correlated with stage of chronic kidney disease in renal transplant recipients.// Transplant Proc. 2012. Vol. 44, N 3. P. 621-624.
Статья опубликована в журнале "Экспериментальная и клиническая урология". Номер №1/2013 стр. 30-34










Комментарии