Волкова Е.В., Хоменков В.Г., Ахматова Э.А., Чалая Е.Л., Сорокина Е.В., Ахматова Н.К., Перепанова Т.С.
Ведение пациенток с рецидивирующей инфекцией нижних мочевых путей (ИМП) представляет большую проблему. Несмотря на различные методы лечения обострений ИМП и их профилактики, цистит продолжает рецидивировать. Основным возбудителем неосложненной ИМП является уропатогенная E. coli (от 75 до 90% случаев); в 5–20% случаев этиологически значимыми возбудителями являются Klebsiella pneumoniaе, Staphylococcus saprophyticus, Proteus spp. [1]. На сегодняшний день стандартизированного подхода к лечению рецидивирующей ИМП не выработано. Для профилактики рецидивирующей ИМП предлагается длительный прием антибактериальных лекарственных средств в низких (субингибирующих) дозах [2, 3], в тоже время длительный прием противомикробных препаратов приводит к селекции резистентных штаммов микроорганизмов, развитию аллергических реакций и, более того, после прекращения такого поддерживающего лечения, примерно у 60% женщин в течение 3-4 месяцев отмечается рецидив ИМП. Альтернативным методом ведения этих пациенток служит посткоитальная антимикробная профилактика при наличии четкой взаимосвязи между обострением ИМП и половым актом или лечение обострений ИМП полными курсовыми дозами антимикробных лекарственных средств [2]. Учитывая невысокую эффективность антибактериального лечения рецидивирующей ИМП, большое значение приобретают альтернативные методики, в частности – иммунопрофилактика рецидивов заболевания.
Чувствительность пациента к ИМП определяются генетическими механизмами, которые контролируют врожденный иммунный ответ слизистых оболочек. Ответная воспалительная реакция запускается уропатогенной E. сoli через факторы вирулентности, включая фимбрии Р и фимбрии 1-го типа, которые служат посредниками адгезии к уротелию. Хемокиновые рецепторы на уротелии вовлекаются для распознавания бактериальных факторов вирулентности, а активация тол-подобных рецепторов (TLR) слизистой оболочки мочевого пузыря стимулирует внутриклеточные сигнальные пути. Нейтрофилы для борьбы с возбудителем E. coli привлекаются и активизируются хемокинами и их рецепторами [4-6]. Дисфункция этих рецепторов оказывает большое влияние на индивидуальную чувствительность к ИМП. В ответ на сигналы TLR активизируется провоспалительный ответ, контролирующий местную активацию клеток в месте инфицирования. Клетки воспаления привлекаются к инфицированным тканям также посредством секреции цитокинов, интерферонов и хемокинов. Таким образом, TLRрецепторы контролируют выраженность и активность воспалительной реакции. Дисфункция TLR4 может иметь защитное действие вследствие подавления воспаления и симптомов заболевания [7].
Макрофаги, дендритные и эпителиальные клетки также имеют разные образ-распознающие рецепторы (PRR), например, такие как TLRрецепторы, которые играют ключевую роль в активизации врожденного иммунитета. Эти рецепторы распознают вирулентные компоненты патогенных микроорганизмов, включая компоненты, содержащиеся в препарате Уро-Ваксом, и инициируют иммунный ответ, направленный на их разрушение.
Доказано, что у больных с рецидивирующими инфекциями нижних мочевых путей имеются изменения местного иммунного ответа в виде нарушения отдельных функций нейтрофилов (хемотаксис, фагоцитоз, бактерицидная функция), снижения активности IL-2 и уровня IL-8 в моче, способствующих миграции нейтрофилов в просвет мочевого пузыря, а также секреторного IgA, который блокирует прикрепление бактерий к эпителиальным клеткам [8].
Исследования in vitro показали, что Уро-Ваксом стимулирует активность макрофагов и нейтрофилов, активизирует созревание дендритных клеток и увеличивает экспрессию адгезивных молекул нейтрофилами [9, 10, 11]. Кроме того, исследования на мышах показали, что Уро-Ваксом повышает активность лейкоцитов в крови и секрецию фактора некроза опухоли альфа (ФНОальфа) перитонеальными клетками, а также иммуноглобулина G (IgG) в культуре клеток селезенки [12, 13]. Молекулярный механизм, посредством которого Уро-Ваксом стимулирует клетки врожденного иммунитета, вероятно, связан с его способностью активировать PRR, такие как TLR2 и TRL4 [12].
Т-хелперы, играя ключевую роль в воспалительных реакциях, являются индукторами развития адаптивного ответа. Дисбаланс Тхелперов 1-го и 2-го типов может способствовать развитию хронических воспалительных заболеваний, в том числе и заболеваний мочеполовой системы. Кроме того, баланс этих клеток в воспалительный период определяет последующую форму иммунного ответа c поляризацией его преимущественно по клеточному или гу-моральному типу [14]. Изменение спектра различных цитокинов в плазме крови позволяет оценить развитие системной воспалительной реакции и функционирование иммунной системы в целом. В то же время скрининг Th-цитокинов может выявить нарушения ключевых иммунных процессов и помочь подобрать оптимальную терапию, а также определить эффективность применяемых препаратов [15, 16].
Цель работы – изучение влияния препарата Уро-Ваксом на цитокиновый статус пациенток с рецидивирующим бактериальным циститом.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование осуществлялось на базе НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал «ФГБУ НМИРЦ» Минздрава России и ФГБНУ НИИ вакцин и сывороток им. И.И. Мечникова с 2011 по 2014 гг. Всего в исследование включено 66 женщин, из них 40 женщин с рецидивирующими инфекциями нижних мочевых путей в возрасте от 18 до 68 лет. Средняя продолжительность заболевания – 3,8 лет. В контрольную группу вошли 26 практически здоровых женщин.
В исследование не включали пациенток с циститом, имеющих сопутствующие хронические заболевания в фазе обострения, инфекции, передаваемые половым путем (хламидии, микоплазмы, гонорея, трихомонады, папилломовирусная инфекция), а также беременных женщин. Все исследования выполнены после получения информированного согласия пациентов и в соответствии с этическими нормами Хельсинской Декларации (2006). Оценка клинических и лабораторных данных, помимо клинических анализов мочи и крови включала бактериологический анализ мочи и показатели врожденного и адаптивного иммунного ответа в сыворотке крови и в слизистых мочевых путей до включения в исследование (исходный), через 1 мес. после начала лечения, через 3 мес. после начала лечения и через 6 мес. после начала лечения (по окончании исследования). Бактериологические исследования проводились в микробиологической лаборатории Национального агентства по клинической фармакологии.
Ранее все пациентки получали антимикробную терапию. В основном, в качестве монотерапии пациентки использовали фосфомицина трометамол, норфлоксацин, фуразидин и ципрофлоксацин. Мы проводили монотерапию препаратом Уро-Ваксом, который представляет собой лиофилизированный бактериальный лизат 18 штаммов Escherichia coli. Уро-Ваксом назначали утром натощак по одной капсуле в день (6 мг) в течение 90 дней (3 месяца), в соответствии со стандартной схемой приема, одобренной в Российской Федерации. Забор крови для иммунологических исследований осуществляли натощак в утренние часы. Полученную сыворотку крови хранили при температуре минус 700 С до проведения анализа. Цитокиновой профиль оценивали по содержанию прои противовоспалительных цитокинов: IL1b, IL-2, TNF-α, IFN-g, IL-12p70, IL-4, IL-5, IL-6, IL-10, IL-13, IL-9, Il-17a, IL-22.
Уровень цитокинов определяли методом проточной цитометрии (Сytomix FC-500, Beckman Coulter, USA) c помощью тест-системы Multiplex-13 (Bender MedSystems,Austria).Анализ результатов проводили с использованием программы Statistica 10 [17]. Статистическая значимость различий уровня цитокинов между группами оценивали непараметрическими методами исследования с помощью критерия Манна-Уитни. Статистически достоверными считали различия при значениях (p≤0,05).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Динамика Th1-цитокинов представлена на рисунке 1. Провоспалительный цитокин TNF-α в сыворотке крови больных c рецидивирующей инфекцией нижних мочевых путей до лечения (0 точка, 106,9 пг/мл) был повышен в 2,8 раза по сравнению с контрольной группой (условно здоровые, 51,1 пг/мл). Применение Уро-Ваксома способствовало снижению уровня TNF-a в 1,3-1,7 раз в течение 6 месяцев (62,9-82,5 пг/мл, p<0,05) по сравнению с пациентами до лечения. Однако, несмотря на динамику снижения этого показателя во все сроки наблюдения, уровень TNF-α оставался повышенным(p<0,05) по сравнению со здоровыми лицами.
IL-1b у больных до лечения составил 70,5 пг/мл (выше нормы в 2,5 раза). После применения препарата уровень его начал активно снижаться до нормы, достигнув своего минимума на 2-м месяце лечения – 35,1 пг/мл (ниже в 1,6 раза по сравнению с 0 точкой). Но по истечении этого периода происходило постепенное его увеличение до 53,5 пкг/мл на 6-м месяце (повышение в 1,8 раз по сравнению с нормой и снижение в 1,3 раза по сравнению с 0 точкой, p<0,05).
Изначально концентрация IL-2, обеспечивающего пролиферацию и дифференцировку 1-клеток, была снижена в 1,3 раза (317,7 пг/мл против 414 пкг/мл – у здоровых). Использование препарата Уро-Ваксом приводило к резкому повышению этого показателя у пациентов уже через месяц лечения (до 428 пг/мл) и содержание IL-2 в сыворотке на нормальном уровне сохранялось на протяжении всего периода наблюдения.
В начальные сроки наблюдения (1 мес.) уровень IFN-γ резко повышался под воздействием препарата Уро-Ваксома (с 26,4 до 75,6 пг/мл), превышая нормативные (55 пг/мл) показатели в 1,4 раза (p<0,05). После чего происходило его постепенное снижение в течение последующих двух месяцев до нормальных значений (56,9-55,2 пг/мл). Начиная с 4-го месяца наблюдения уровень IFN-γ еще сильнее снижался, хотя статистически значимо был выше его уровня в острый период заболевания до начала лечения.
Концентрации IL-12 у больных в остром периоде заболевания находились ниже (p<0,05) уровня нормы в 1,4 раза (64,3 против 82,7 пкг/мл). Лечение Уро-Ваксомом повышало этот показатель до нормы на протяжении всего периода наблюдения (6 мес.).
Таким образом, среди Th1 цитокинов уровень TNF-α и IL-1β у больных в острый период был резко повышен. Под влиянием препарата отмечалась тенденция к их снижению, но изменения показателей до нормальных значений не отмечалось (за исключением IL-1 через 1 мес. после применения препарата Уро-Ваксом). Противоположная картина отмечалась в отношении других Th1 цитокинов: IL-2, IFN-γ, IL-12p70. Изначально их уровни были существенно ниже нормальных значений. Под действием препарата происходила нормализация уровней IL-2, IFN-γ и IL-12 на протяжении всего периода, за исключением IFN-γ, показатели которого снова начинали снижаться ниже контрольных значений через 4 месяца после начала лечения.
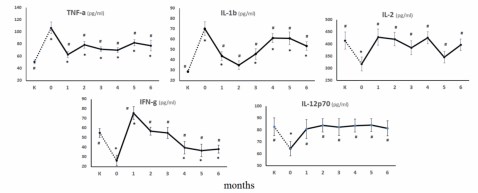
Рис. 1. Динамика Th1 цитокинов в сыворотках больных с рецидивирующей инфекцией нижних мочевых путей под воздействием препарата Уро-Ваксом®. Данные представленны как среднее значение ± стандартное отклонение. * – достоверность различий по сравнению с контролем; # – между группами до и после лечения, p<0,05. Тест МаннаУитни для независимых выборок.
Динамика Th2 цитокинов в процессе лечения Уро-Ваксомом представлена на рисунке 2. Уровни IL-4, IL-5 и IL-13 у больных до лечения значимо (соответственно в 4,4 3,1 и 1,6 раз) повышены по сравнению со здоровыми (соответственно 345 пг/мл, 133,8 пг/мл и 406 пг/мл против 78 пг/мл, 41,5 пг/мл и 252 пг/мл. Лечение с помощью препарата Уро-Ваксом приводит к кратковременному снижению уровня IL-4 в 1,5-1,12 раза (соответственно через 1 и 3 мес.) по сравнению с пациентами в фазе обострения заболевания. Аналогичная картина наблюдается и по отношению к IL-5, когда его уровень снижается приблизительно в 3,5 раз и сохраняет стабильность в течение 6 мес. Однако нормализации значений как IL-4, так и IL-5 не наблюдается. IL-13 через 1 мес. после применения Уро-Ваксом®а снижается в 1,6 раза (до 289,6 пг/мл) и сохраняется на уровне нормальных значений в течение 5 мес.
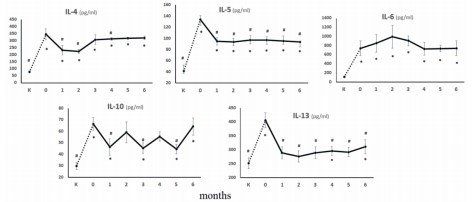
Рис. 2. Динамика Th2 цитокинов в сыворотках больных с рецидивирующей инфекцией нижних мочевых путей под воздействием препарата Уро-Ваксом®. К (контроль) – показатели в норме. Данные представленны как среднее значение ± стандартное отклонение. * – достоверность различий по сравнению с контролем; # – между группами до и после лечения, p<0,05. Тест МаннаУитни для независимых выборок.
У здоровых лиц уровни IL-6 находятся в пределах 116,4 пг/мл, что в 6,4 раза ниже показателей у пациентов в фазе обострения заболевания (742пг/мл, p<0,05). Существенного влияния на данный показатель при терапии женщин препаратом Уро-Ваксом не выявлено, так как значения IL-6 стабильно оставались высокими (730,6-997 пкг/мл).
Исходно у больных отмечался высокий уровень IL-10 (66,5 пг/мл), что превышало нормальные показатели в 2,2 раза (29,9 пг/мл). В процессе терапии отмечался волнообразный характер синтеза этого цитокина в крови: через 1 мес. он снижался до 46,3 пг/мл (в 1,4 раза), затем были отмечены периоды его повторного повышения с последующим снижением. Несмотря на то, что уменьшение уровней IL-10 на 1, 3 и 5 месяце наблюдения значимо отличались от исходных показателей в период обострения, они также превышали показатели контрольной группы (p<0,05).
Таким образом, в отношении Th2 цитокинов IL-4, IL-6 и IL-10 достоверного снижения их уровней по сравнению с начальными показателями не происходило, при этом концентрации IL-5 статистически значимо снижались, но не достигали уровня контрольных значений здоровых лиц. Значимое уменьшение концентраций наблюдалось только в отношении IL-13. То есть, в случае Th2 цитокинов наблюдалась относительная корреляция иммунного ответа.
У больных до начала лечения уровни IL-9 и IL-22 превышали нормальные значения соответственно в 1,25 и 4,3 раз, после проведения терапии данные показатели практически не менялись в течение второго (IL-9) и третьего (IL-22) месяцев, после чего происходило резкое снижение показателей до нормальных значений, которое стабильно держалось в последующие сроки наблюдения (рис. 3).
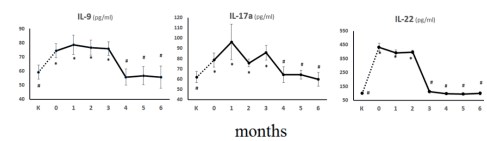
Рис. 3. Динамика Th9/Th17/Th22 цитокинов в сыворотках больных с рецидивирующей инфекцией нижних мочевых путей под воздействием препарата Уро-Ваксом® Данные представлены как среднее значение ± стандартное отклонение. * – достоверность различий по сравнению с контролем; # – между группами до и после лечения, p<0,05. Тест МаннаУитни для независимых выборок.
Был отмечен повышенный уровень IL-17 у больных в остром периоде (в 1,26 раз, 78,7 пг/мл против 62,2 пг/мл в контроле), который кратковременно (через 1 мес., 96,3 пг/мл) повышался после проведения терапии Уро-Ваксомом, затем происходило постепенное его снижение до уровня нормальных значений к четвертому месяцу наблюдения.
По полученным данным были рассчитаны коэффициенты баланса Коэффициенты рассчитывались как отношения концентраций Th1 и Th2, Th1 и Th9, Th1 и Th17, Th1 и Th22, а также Th2 и Th9, Th2 и Th17, Th2 и Th22 цитокинов, являющихся агонистами:IL-1b/IL-4,IL-1b/IL-5,IL-1b/IL-6, IL-1b/IL-10, IL-1b/IL-13, IL-1b/IL-17a, IL-1b/IL-22, IL-1b/L-9, IL-4/IL-17a, IL4/IL-22, IL-4/IL-9, IL-5/IL-17a, IL-5/IL22, IL-5/IL-9, IL-6/IL-17a, IL-6/IL-22, IL-6/IL-9, IL-10/IL-17a, IL-10/IL-22, IL10/IL-9, IL-13/IL-17a, IL-13/IL-22, IL13/IL-9 (табл. 1, 2)
Таблица 1. Коэффициенты баланса Th1/Th2, Th1/Th9, Th1/Th17 и Th1/Th22 у больных с рецидивирующей инфекцией нижних мочевых путей
| IL-1b/IL-4 | IL-1b/IL-5 | IL-1b/IL-6 | IL-1b/IL-10 | IL-1b/IL-13 | IL-1b/IL-17а | IL-1b/IL-22 | IL-1b/IL-9 | |
|---|---|---|---|---|---|---|---|---|
| Контроль | 0,37 | 0,7 | 0,25 | 0,96 | 0,11 | 0,46 | 0,28 | 0,38 |
| До лечения | 0,2 | 0,52 | 0,1 | 1,06 | 0,17 ↑ | 0,89 ↑ | 0,16 | 1,18 ↑ |
| 1 мес | 0,19 | 0,46 | 0,05 | 0,95 | 0,15 ↑ | 0,45 | 0,11 | 0,55↑ |
| 2 мес | 0,15 | 0,47 | 0,05 | 1,01 | 0,16 ↑ | 0,53 ↑ | 0,40↑ | 0,60↑ |
| 3 мес | 0,16 | 0,57 | 0,07 | 0,83 | 0,17 ↑ | 0,89 ↑ | 0,52↑ | 0,8 ↑ |
| IL-2/IL-4 | IL-2/IL-5 | IL-2/IL-6 | IL-2/IL-10 | IL-2/IL-13 | IL-2/IL-17а | IL-2/IL-22 | IL-2/IL-9 | |
| Контроль | 5,3 | 9,9 | 3,5 | 13,8 | 1,6 | 6,6 | 4,1 | 5,5 |
| До лечения | 0,9 | 2,3 | 0,4 | 4,7 | 0,8 | 4,0 | 0,7 | 5,3 |
| 1 мес | 1,8 | 4,5 | 0,5 | 9,2 | 1,5 | 4,4 | 1,1 | 5,4 |
| 2 мес | 1,2 | 3,9 | 0,4 | 8,5 | 1,3 | 4,5 | 3,4 | 5,1 |
| 3 мес | 1,2 | 4,2 | 0,5 | 6,2 | 1,3 | 6,6 | 3,9 | 5,9↑ |
| IL-4/TNF-a | IL-4/IL-5 | IL-4/IL-6 | IL-4/IL-10 | IL-4/IL-13 | IL-4/IL-17а | IL-4/IL-22 | IL-4/IL-9 | |
| Контроль | 0,6 | 1,2 | 0,4 | 1,7 | 0,2 | 0,8 | 0,5 | 0,6 |
| До лечения | 0,3 | 0,8 | 0,1 | 1,6 | 0,3 | 1,3 ↑ | 0,2 | 1,8↑ |
| 1 мес | 0,3 | 0,6 | 0,07 | 1,3 | 0,2 | 0,6 | 0,1 | 0,8↑ |
| 2 мес | 0,2 | 0,7 | 0,08 | 1,6 | 0,2 | 0,8 | 0,6 ↑ | 0,9↑ |
| 3 мес | 0,2 | 0,8 | 0,1 | 1,2 | 0,2 | 1,3 ↑ | 0,7 ↑ | 1,1 ↑ |
| IFN-g/IL-4 | IFN-g/IL-5 | IFN-g/IL-6 | IFN-g/IL-10 | IFN-g/IL-13 | IFN-g/IL-17а | IFN-g/IL-22 | IFN-g/IL-9 | |
| Контроль | 0,7 | 1,3 | 0,5 | 1,8 | 0,2 | 0,9 | 0,5 | 0,7 |
| До лечения | 0,07 | 0,2 | 0,03 | 0,4 | 0,06 | 0,3 | 0,06 | 0,4 |
| 1 мес | 0,3 | 0,8 | 0,09 | 1,6 | 0,3 | 0,8 | 0,2 | 0,9↑ |
| 2 мес | 0,2 | 0,6 | 0,07 | 1,2 | 0,2 | 0,6 | 0,5 | 0,7↑ |
| 3 мес | 0,1 | 0,4 | 0,05 | 0,6 | 0,1 | 0,6 | 0,4 | 0,6 |
| IL-12p70/IL-4 | IL-12p70/IL-5 | IL-12p70/IL-6 | IL-12p70/IL-10 | L-12p70/IL-13 | IL-12p70/IL-17а | IL-12p70/IL-22 | IL-12p70/IL-9 | |
| Контроль | 1,1 | 2,0 | 0,7 | 2,7 | 0,3 | 1,3 | 0,8 | 1,0 |
| До лечения | 0,2 | 0,5 | 0,1 | 0,9 | 0,1 | 0,8 | 0,1 | 1,1 |
| 1 мес | 0,3 | 0,8 | 0,1 | 1,7 | 0,3 | 0,8 | 0,2 | 1,0 |
| 2 мес | 0,2 | 0,8 | 0,1 | 1,8 | 0,3 | 0,9 | 0,7 | 1,1 ↑ |
| 3 мес | 0,2 | 0,9 | 0,1 | 1,3 | 0,3 | 1,3 | 0,8 | 1,2 ↑ |
Примечание. ↑ – повышение коэффициента баланса Th1/Th2/Th9/Th/17/Th22 цитокинов по сравнению с контролем
Таблица 2. Коэффициенты баланса Th2/Th9, Th2/Th17 и Th2/Th22 у больных с рецидивирующей инфекцией нижних мочевых путей
| IL-4/IL-17а | IL-4/IL-22 | IL-4/IL-9 | |
|---|---|---|---|
| Контроль | 1,2 | 0,8 | 1,03 |
| До лечения | 4,4 ↑ | 0,8 | 5,8 ↑ |
| 1 мес | 2,4 ↑ | 0,6 | 2,9 ↑ |
| 3 мес | 3,6 ↑ | 2,7 ↑ | 4,05 ↑ |
| 6 мес | 5,3 ↑ | 3,1 ↑ | 4,7 ↑ |
| IL-5/IL-17a | IL-5/IL-5 | IL-5/IL-9 | |
| Контроль | 0,7 | 0,4 | 0,5 |
| До лечения | 1,7 ↑ | 0,3 | 2,2 ↑ |
| 1 мес | 1,0 ↑ | 0,2 | 1,2 ↑ |
| 3 мес | 1,1 ↑ | 0,8 ↑ | 1,3 ↑ |
| 6 мес | 1,5 ↑ | 0,9 ↑ | 1,4 ↑ |
| IL-6/IL-17a | IL-6/IL-22 | IL-6/IL-9 | |
| Контроль | 1,9 | 1,1 | 1,5 |
| До лечения | 9,4 ↑ | 1,7 ↑ | 12,5 ↑ |
| 1 мес | 8,8 ↑ | 2,1 ↑ | 10,8 ↑ |
| 3 мес | 10,5 ↑ | 7,9 ↑ | 11,9 ↑ |
| 6 мес | 12,4 ↑ | 7,2 ↑ | 11,1 ↑ |
| IL-10/IL-17a | IL-13/IL-22 | IL-13/IL-9 | |
| Контроль | 0,5 | 0,3 | 0,4 |
| До лечения | 0,8 ↑ | 0,1 | 1,1 ↑ |
| 1 мес | 0,5 | 0,1 | 0,6 ↑ |
| 3 мес | 0,5 | 0,4 ↑ | 0,6 ↑ |
| 6 мес | 1,0 ↑ | 0,6 ↑ | 0,9 ↑ |
| IL-13/IL-17a | IL-13/IL-22 | IL-13/IL-9 | |
| Контроль | 4,0 | 2,5 | 3,3 |
| До лечения | 5,1 ↑ | 0,9 | 6,8 ↑ |
| 1 мес | 3,0 | 0,7 | 3,7 ↑ |
| 3 мес | 3,4 | 2,5 | 3,8 ↑ |
| 6 мес | 5,2 ↑ | 3,0 ↑ | 4,6 ↑ |
Примечание. ↑ – повышение коэффициента баланса Th2/Th9, Th2/Th17 и Th2/Th22 цитокинов по сравнению с контролем
Как видно из таблиц 1 и 2, был выявлен дисбаланс соотношения пяти типов Т-хелперных клеток. Из таблицы 1 видно, что значения коэффициентов баланса 1 и 2 типов цитокинов при рецидивирующей инфекции нижних мочевых путей у женщин снижаются (за исключением IL-1b/IL-13) в сравнении с контрольной группой, а соотношение Th1/Th9/ Th17/Th22 цитокинов меняются разнонаправленно. При этом соотношение Th2/Th9/Th17/Th22 преимущественно повышается. Этот факт может свидетельствовать о смещении баланса цитокиновой системы в сторону Th2 хелперных клеток. Применение препарата Уро-Ваксом® в некоторой степени корригирует данный показатель, снижая уровень коэффициентов, но перевешивание баланса Th2 типа все же сохраняется.
Полученные результаты свидетельствуют о смещении цитокинового баланса в сторону противовоспалительных цитокинов. Поддержание эффективного иммунного ответа в такой ситуации становится невозможным. Увеличение концентраций провоспалительных цитокинов в крови пациенток служит основой для развития воспалительной реакции при рецидивирующих инфекциях мочевых путей. Это может привести к расширению очага воспаления и повреждению тканей, усилению перекисного окисления липидов и белков, накоплению свободных радикалов, стимуляции апоптоза. Преобладание 2 цитокинов приводит к поляризации иммунного ответа преимущественно по гуморальному типу.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
CD4 T хелперы – важные медиаторы клеточного иммунного ответа. Предполагается, что эти популяции существуют как дихотомические линии так называемых Th1 и Th2 хелперных клеток. Тип-1 цитокинов включает IL-2, IFN-γ, IL-12 и TNF, в то время как тип 2 – IL-4, IL-5, IL-6, IL-10 и IL-13. В настоящее время обнаружены и охарактеризованы также и другие субпопуляции эффекторных Тклеток-хелперов:Th17,Th9 иTh22 [18].
Как показывают наши исследования, у больных с рецидивирующей инфекцией нижних мочевых путей наблюдается дисбаланс Th1, Th2, Th9 и Th17 и Th22 цитокиновой системы. До начала терапии в спектре Th1 цитокинов отмечались повышенные концентрации TNF-α и IL-1β, которые являются ключевыми провоспалительными составляющими иммунного ответа. TNF-α, синтезируемый преимущественно клетками миеломоноцитарного ряда и играющий важную роль при метаболическом синдроме, оказывает влияние на функционирование эндотелия, продукцию IL-1, IL-6, IL-8, IFN-ɣ и активацию лимфоцитов. IL-1β, обеспечивая резистентность к патогенам, также может усугублять повреждения тканей при хронических заболеваниях и острой травме [19].
Однако, уровни других провоспалительных цитокинов IL-2, IFN-γ, IL-12p70 у женщин, страдающих рецидивирующим бактериальным циститом, находились ниже нормальных значений, что может свидетельствовать о нарушении механизмов функционирования в системе Th1 медиаторов воспаления.
IL-2, оказывая непосредственное воздействие на лимфоциты, приводит к дифференциации некоторых незрелых Т-клеток в регуляторные Тклетки, которые подавляют аутореактивные клоны. Также под воздействием IL-2 Т-клетки дифференцируются в эффекторные и клетки памяти, тем самым обеспечивая быстрое реагирование иммунной системы на повторное вторжение патогенов [20]. При этом IFN-γ, являясь активатором макрофагов, может вызывать как защитные, так и патологические эффекты. Этот интерферон индуцирует дифференцировку миелоидных клеток костного мозга, в результате которой они приобретают высокоаффинные Fcg-рецепторы для связывания мономерной формы IgG. IFN-γ активирует и антителозависимую клеточную цитотоксичность (АЗКЦ) осуществляемую зрелыми гранулоцитами [21].
Очень важным цитокином врожденного иммунного ответа является IL-12p70, который участвует в дифференцировке наивных Т-клеток в Тh1-клетки и стимулирует рост и функцию Т-клеток. IL-12p70 индуцирует синтез IFN-γ и TNF-α Ти NK-клетками, а также снижает IL-4 опосредованную супрессию IFN-γ [22, 23].
Применение Уро-Ваксома приводило к незначительному снижению изначально повышенных концентраций TNF-α и IL-1β и повышению уровней других Th1 цитокинов: IL-2, IFN-γ и IL-12, что может свидетельствовать о частичной коррекции воспалительного ответа у больных в исследуемые сроки наблюдения.
У больных с рецидивирующей инфекцией нижних мочевых путей изначально уровни противовоспалительных цитокинов были повышены относительно нормальных значений, что, может оказывать супрессирующее влияние на эффекторы иммунитета не только на системном, но и локальном уровнях.
Важными медиаторами иммунного ответа являются цитокины Th2-типа, включающие IL-4, IL-5 и IL-13, которые ассоциируются с индукцией IgE и эозинофильных ответов при атопии, а также IL-10, который характеризуется большей способностью индуцировать противовоспалительный ответ [24]. IL-10, продуцируемый моноцитами/ макрофагами, активированными В-клетками и Th1 и Th2 клетками, подавляет синтез Th1 цитокинов, включая IFN-γ, IL-2, и TNF-α с Th1 клетками и IL-1, IL-6, IL-8, IL-12 и GM-CSF моноцитами/макрофагами. В избытке, Th2-ответ противодействует Th1-опосредованному бактерицидному действию [25]. Поэтому, для поддержания адекватного иммунного ответа важен баланс ответа Т хелперов Th1/Th2/Th9/Th17/Th22. Как видно из наших исследований, уровень Th2 цитокинов оставался достаточно высоким по сравнению с группой здоровых лиц, хотя имел тенденцию к снижению при использовании препарата Уро-Ваксом®. При этом на проводимую терапию лучше отвечал IL-13, так как он давал лучшие результаты снижения сывороточных концентраций у больных циститами.
В целом, в наших исследованиях в группе больных происходило корригирование изначально повышенных уровней Th9/Th17/Th22 цитокинов. Известно, что IL-17A продуцируется уникальной субпопуляцией Т-хелперных клеток независимо от Th1/Th2 клеточного развития. Th17-клетки играют роль в защите организма от внеклеточных патогенов посредством рекрутирования нейтрофилов и макрофагов в инфицированные ткани. Кроме того, становится очевидным, что аберрантная регуляция Th17клеток может играть значительную роль в патогенезе многочисленных воспалительных и аутоиммунный нарушений [13].
Th17-клетки продуцируют IL-17, IL-17F и IL-22, тем самым вызывая массовую реакцию тканей вследствие широкого распространения IL-17 и IL-22 рецепторов. Через секрецию IL-21 17 клетки могут взаимодействовать с клетками иммунной системы. Недавно были идентифицированы дифференцировочные факторы (TGF-β плюс IL-6 или IL-21), факторыроста и стабилизации (IL-23), а также транскрипционные факторы (STAT3, RORγt и RORα), участвующие в развитии 17 клеток. Участие TGF-β в дифференциации Th17 клеток проводит тесную параллель между Th17 и CD4+/CD25+/Foxp3+ регуляторными Т-клетками (T-reg) [26].
В наших исследованиях повышенный уровень IL-17 у больных в остром периоде после применения Уро-Ваксом®а еще больше стимулировал синтез данного цитокина через 1 мес. Вероятно, это связано с распознаванием патоген-ассоциированных молекулярных структур, входящих в состав вакцины, которые могут запускать каскад внутриклеточных сигналов, активирующих ядерный транскрипционный фактор NF-kB.
Недавно открыта субпопуляция Т хелперных клеток – Th9, TGF-β, который является критически важным в дифференцировке Th17-клеток, индуцирует реорганизацию Th2 клеток в Th9, которые характеризуются секрецией IL-9. Th9-клетки могут также быть дериватами наивных CD4+ Тклеток, продуцирующих TGF-β и IL4. IL-9 является членом общего цитокинового рецептора γ цепь-зависимого семейства цитокинов, которые также включают IL-2, IL-4, IL-7, IL-15 и IL-21. Благодаря плейотропным эффектам в отношении Th2-лимфоцитов, В-лимфоцитов, тучных клеток, эозинофилов, а также эпителиальных клеток кишечника и респираторного тракта Th9 вовлекаются в патогенез астмы и других аллергических заболеваний [27].
IL-22 – член IL-10 цитокинового семейства, которые преимущественно секретируются Th17-клетками. IL-23 и IL-6 могут непосредственно стимулировать наивные Т-клетки к продукции IL-22. Также IL-22 способен защитить от бактериальной инфекции в легких и кишечнике. Недавно была открыта собственная Т-клеточная популяция, называемая Th22. Эти клетки инфильтрируют эпидермис у индивидов с воспалительными нарушениями кожи и характеризуются секрецией IL-22 и TNF-α, но не IFN-γ, IL-4 или IL-17 [28].
На тканевом уровне Th-цитокины отвечают за развитие воспаления и за регенерацию тканей. При развитии системной воспалительной реакции цитокины влияют практически на все органы и системы организма, участвующие в регуляции гомеостаза. Попадание цитокинов в кровяное русло, безусловно, означает, что местная защита не справилась с патогеном и требуется включение системной воспалительной реакции для предотвращения распространения патогена и противодействия развитию сепсиса. Регуляция защитных реакций организма цитокинами происходит не только в рамках иммунной системы, но и на уровне целостного организма, где цитокины осуществляют связь между иммунной, нервной, эндокринной, кроветворной и другими системами и служат для их вовлечения в организацию и регуляцию единой защитной реакции [28].
ЗАКЛЮЧЕНИЕ
1. У женщин с рецидивирующими инфекциями нижних мочевых путей отмечаются низкие уровни сывороточных провоспалительных цитокинов IL-2, IFN-γ, IL-12p70 и повышенные концентрации TNF-α и IL-1β, что может свидетельствовать о нарушении механизмов функционирования в системе 1 медиаторов воспаления.
2. Повышенные концентрации противовоспалительных цитокинов в крови больных с рецидивирующими инфекциями нижних мочевых путей свидетельствуют об активации механизмов иммуносупрессирующего действия Th2 цитокинов (IL-4, IL-5, IL-6, IL-10 IL-13) в отношении эффекторов иммунитета на системном уровне.
3. У больных с рецидивирующей инфекцией нижних мочевых путей наблюдается дисбаланс Th1, Th2, Th9, Th17 и Th22 цитокиновой системы с поляризацией иммунного ответа преимущественно по гуморальному (Th2) типу
4. Использование препарата Уро-Ваксом оказывает слабое иммунокорригирующее влияние на Th1/Th2 тип цитокинов и существенно корригирует баланс в системе Th9, Th17 и Th22 типов цитокинов у больных с рецидивирующей инфекцией нижних мочевых путей.
ЛИТЕРАТУРА
1. Перепанова Т.С., Козлов Р.С., Дехнич А.В. Выбор антимикробных препаратов при инфекции мочевых путей. // Урология, 2012. № 2. С. 4-8.
2. Российские национальные рекомендации «Антимикробная терапия и профилактика инфекций почек, мочевыводящих путей и мужских половых органов» / под ред. Н.А. Лопаткина, О.И. Аполихина, Д.Ю. Пушкаря, А.А. Камалова, Т.С. Перепановой. М., 2014. С. 33.
3. Grabe M, Bartoletti R, Bjerklund Johansen TE, Cek M, Koves B, Naber KG, Pickard RS, Tenke P, Wagenlehner F, Wullt B. Guidelines on Urological Infections. // European Association of Urology,2015. P.19-20.
4. Cerutti A, Chen K, Chorny A. Immunoglobulin responses at the mucosa interface. // Ann. Rev. Immunol. 2011. Vol. 29. P. 273–293.
5. Nielubowicz GR, Mobley HL. Host-pathogen interactions in urinary tract infection. // Nat. Rev. Urol. 2010. Vol. 7. № 8. P. 430–441.
6. Song J, Abraham SN. TLR-mediated immune responses in the urinary tract. // Curr. Opin. Microbiol. 2008. Vol. 11. № 1. P. 66–73.
7. Перепанова Т.С., Хазан П.Л., Волкова Е.М., Эгамбердиев Д.К. Возможности вакцинации при рецидивирующей инфекции мочевых путей.// Журнал Эффективнаяфармакотерапия.Урология. 2012. № 4.С. 24-31.
8. Симбарская М.Л. Особенности местного иммунитета слизистой оболочки влагалища при хроническом рецидивирующем кандидозе гениталий и бактериальном вагинозе у женщин репродуктивного возраста. Дис., Санкт-Петербург, 2015. С. 23-31.
9. Bessler WG, vor dem Esche U, Zgaga-Griesz A, Ataullakhanov R. Immunostimulatory properties of the bacterial extract OM-89 in vitro and in vivo. // Arzneimittelforschung. 2010. Vol. 60. № 6. P. 324–329.
10. Schmidhammer S, Ramoner R, Holtl L. An Escherichia coli-based oral vaccine against urinary tract infections potently activates human dendritic cells. // Urology. 2002. Vol. 60. № 3. P. 521–526.
11. Marchant A, Duchow J, Goldman M. Adhesion molecules in antibacterial defenses: effects of bacterial extracts. // Respiration. 1992. Vol. 59. Suppl. 3. P. 24–27.
12. Bessler WG, Puce K, vor dem Esche U. Immunomodulating effectsof OM-89, a bacterial extract from Escherichia coli, in murine and human leukocytes // Arzneimittelforschung. 2009. Vol. 59. № 11. P. 571–577.
13. Hasan M, Neumann B, Haupeltshofer S, Stahlke S. Activation of TGF-β-induced non-Smad signaling pathways during Th17 differentiation. // Immunol Cell Biol. 2015. N. 3. P. 216-223.
14. Kidd PМ. Th1/Th2 balance: the hypothesis, its limitations, and implications for health and disease. // Alternative medicine review. 2003. Vol. 8, N 3. P. 223-246.
15. Национальное руководство «Аллергология и иммунология» под ред. Хаитова Р.М., «ГЭОТАР-Медиа», 2009. С. 47-48.
16. Черешнев В.А., Черешнева М.В. Иммунологические механизмы локального воспаленя. Медицинская иммунология 2011. Т. 13, № 6. С. 557-568 © 2011, СПб РО РААКИ.
17. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ STATISTICA. М.: МедиаСфера. 2002. С. 312.
18. Steinman L. A brief history of T(H)17, the first major revision in the T(H)1/T(H)2 hypothesis of T cell-mediated tissue damage. // Nat. Med. 2007. Vol. 13, N 2. P. 139–145.
19. Lopez-Castejon G, Brough D. Understanding the mechanism of IL-1β secretion. // Cytokine Growth Factor Rev. 2011. Vol. 22, N 4. P. 189-195.
20. Balkhi MY, Ma Q, Ahmad S, Junghans RP. T cell exhaustion and Interleukin 2 downregulation. // Cytokine. 2015. Vol. 71, N 2. P. 339-47.
21. Hoeksema MA, Scicluna BP, Boshuizen MC. IFN-γ Priming of Macrophages Represses a Part of the Inflammatory Program and Attenuates Neutrophil Recruitment. // J Immunol. 2015. Vol. 3, N. 2. P. 329-335.
22. Hsieh CS, Macatonia SE, Tripp CS, Pillars article: development of TH1 CD4+ T cells through IL-12 produced by Listeria-induced macrophages. // J Immunol. 2008. Vol. 181, N 7. P. 4437-4439.
23. Espinosa V, Rivera A. Cytokines and the regulation of fungus-specific CD4 T cell differentiation. // Cytokine. 2012. Vol. 58, N. 1. P. 100-106.
24. Redpath SA, Heieis G, Perona-Wright G. Spatialregulation of IL-4 signalling in vivo. // Cytokine. 2015. Vol. 4, N 1. P. 112-116.
25. Muraille E, Leo O, Moser M. TH1/TH2 paradigm extended: macrophage polarization as an unappreciated pathogen-driven escape mechanism? // Front Immunol. 2014. N. 5. P. 603.
26. Rodríguez-Reyna TS, Furuzawa-Carballeda J, Cabiedes J. Th17 peripheral cells are increased in diffuse cutaneous systemic sclerosis compared with limited illness: a cross-sectional study. // Rheumatol Int. 2012. Vol. 32, N 9. P. 2653-2660.
27. Hoppenot D, Malakauskas K, Lavinskienė S, Bajoriūnienė I. Peripheral blood Th9 cells and eosinophil apoptosis in asthma patients. // Medicina. 2015. Vol. 51, N. 1. P. 10-17. 28. Jia L, Wu C. The biology and functions of Th22 cells. // Adv Exp Med Biol. 2014. Vol. 841. P. 209-230.









Комментарии