Журнал "Экспериментальная и клиническая урология" Выпуск №1 за 2014 год
Рудин Ю.Э., Марухненко Д.В., Сайедов К.М.
Гипоспадия – один из наиболее распространенных пороков развития полового члена у мальчиков. Она часто сопровождается нарушением мочеиспускания и половой функции. Гипоспадия встречается в среднем у 1:200 новорожденных мальчиков [1,2,3,4]. Проксимальная гипоспадия относится к наиболее сложным формам гипоспадии и встречается значительно реже – 1: 1250 мальчиков [3, 4, 5, 6]. Данная патология характеризуется как сочетанная аномалия развития наружных половых органов и уретры в виде грубого искривления полового члена в сторону мошонки и дистопии наружного отверстия мочеиспускательного канала. Вентральная деформация полового члена обусловлена несоответствием длины уретры и кавернозных тел, вследствие недоразвития губчатой части мочеиспускательного канала и наличия соединительнотканной рубцовой хорды [1, 4]. Степень искривления кавернозных тел, как правило, соответствует уровню эктопии меатуса. Наружное отверстие уретры может располагаться по вентральной поверхности ствола полового члена, мошонки, вплоть до промежности. Крайняя плоть недоразвита, не полностью окружает головку, локализуется по дорзальной поверхности в виде мясистого лоскута.
Форма гипоспадии определяется комбинацией отклонений развития на этапах формирования полового члена [4]:
1. Типичная проксимальная стволовая гипоспадия характеризуется следующими нарушениями [4]:
а. Нарушение слияния срединной складки (medial fold) (зачатка уретральной трубки) в среднем отделе, что приводит к формированию наружного отверстия уретры на вентральной поверхности полового члена.
б. Нарушение слияния складки в латеральном отделе, что вызывает нарушение формирования крайней плоти по вентральной поверхности, укорочению и недоразвитию кожи в области уздечки, отклонению срединного шва (raphe) от центра.
в. Нарушение слияния зачатков головки, что приводит к отсутствию головчатой части уретры; головка при этом расщеплена по центру и имеет продолговатое углубление; отмечаются зачатки несостоявшегося слепо заканчивающегося наружного отверстия мочеиспускательного канала либо даже дополнительной уретры.
г. Недостаточное воздействие мезодермы при закладке и формировании полового члена приводит к дефициту или аномалиям фиброзных волокон белочной оболочки кавернозных тел, мясистой оболочки мошонки и глубокой фасции полового члена. В результате этих нарушений происходит образование деформирующей хорды.
В НИИ урологии применяют международную классификацию гипоспадии, основанную на степени искривления полового члена, а не на положении наружного отверстия уретры. Именно выраженность рубцовой деформации кавернозных тел определяет объем оперативного вмешательства и, соответственно, его сложность. Выделяются три формы гипоспадии: головчатая, дистальная и проксимальная.
Коррекция головчатой формы гипоспадия не представляет значительных трудностей и практически не имеет осложнений (0,5-1%).
К дистальным формам гипоспадии относят все те формы, которые не требуют тотального иссечения рубцовой хорды на вентральной поверхности полового члена. К этой группе относятся больные с венечной, субвенечной и стволовой формами гипоспадии, которые не сопровождаются деформацией кавернозных тел, либо имеющие минимальное искривление (до 15-20°), которое поддается коррекции за счет пликации белочной оболочки по дорсальной поверхности полового члена и рассечения белочной оболочки по вентральной поверхности. Протяженность формируемой уретры при дистальной гипоспадии незначительная, не требует выкраивания и сложного перемещения обширных кожных лоскутов, создания анастомозов уретры с кожной трубкой. Данные операции относительно просты в техническом исполнении и, по общепринятому мнению, выполняются исключительно одномоментно, в один этап [1, 4, 5, 6].
Наиболее сложную проксимальную форму гипоспадии составляют пациенты с грубой деформацией полового члена (30-90°), с эктопией наружного отверстия уретры на стволе полового члена, в стволо-мошоночном отделе, на мошонке или промежности. Проксимальной эту форму порока назвали потому, что после расправления кавернозных тел наружное отверстие уретры смещается ниже или проксимальнее середины ствола полового члена. Так, например, субвенечная форма гипоспадии с грубым искривлением кавернозных тел после иссечения хорды нередко становится низкой стволовой или стволо-мошоночной. Поэтому далеко не каждая субвенечная форма гипоспадии может считаться дистальной, а ориентировка только на положение меатуса может быть причиной ошибки в выборе лечебной тактики.
Коррекция порока у больных с проксимальной гипоспадией предусматривает не только расправление кавернозных тел полового члена, но и создание протяженного участка мочеиспускательного канала путем выкраивания обширных кожных лоскутов на стволе полового члена или крайней плоти. Сформированную трубку перемещают в зону дефекта уретры на значительное расстояние с сохранением кровоснабжения. Далее формируют анастомоз естественной и артифициальной уретры, выполняют пластику головки и укрывают дефекты кожи на стволе полового члена. Поэтому лечение проксимальной гипоспадии представляет собой сложное реконструктивное и пластическое хирургическое вмешательство. В зависимости от подготовки хирурга и опыта лечения гипоспадии, возможно проведение либо одномоментной операции, либо поэтапной коррекции.
Ошибки в выборе методики хирургического пособия и недостаточный опыт хирургов в коррекции данной патологии приводят к большому (25-60%) числу осложнений [7-12]. Существует несколько подходов к лечению проксимальной гипоспадии. Имеются приверженцы одномоментных методов коррекции порока [11-17] и специалисты, которые предпочитают проводить раздельно расправление кавернозных тел и пластику уретры [7-10, 18-23]. План лечения может предусматривать две, три и более операций.
Показания к применению каждого метода одномоментной коррекции и этапного лечения четко не определены и активно обсуждаются в научной литературе. Имеется очень мало информации об отдаленных результатах лечения этой сложной группы больных. Практически отсутствуют работы, посвященные оценке фертильности и половой функции взрослых пациентов, перенесших коррекцию гипоспадии. Все вышеперечисленные проблемы лечения проксимальной гипоспадии, несомненно, требуют разрешения. Улучшение результатов хирургического лечения проксимальной гипоспадии стало основной задачей нашей работы.
МАТЕРИАЛЫ И МЕТОДЫ
За период с 2008 по 2012 гг. в детском уроандрологическом отделении ФГБУ «НИИ урологии» Минздрава России было прооперировано 125 мальчиков с проксимальной гипоспадией в возрасте от 11 мес. до 17 лет. Средний возраст детей составил 2,2 года. Пациентов с проксимальной стволовой формой гипоспадии было 41 чел., с члено-мошоночной – 35, с мошоночной – 36 и промежностной – 13 чел. Первичных больных было 94, ранее оперированных в других клиниках – 31(24,8%). Общий вид проксимальной гипоспадии у детей представлен на рис. 1А, 2А.
Проксимальная гипоспадия может сочетаться с признаками ложного мужского гермафродитизма (ЛМГ). Характерными проявлениями ложного гермафродитизма можно считать: уменьшенные размеры полового члена, наличие двустороннего или одностороннего крипторхизма с не пальпируемыми яичками, гипоплазия мошонки. Поэтому всем больным с проксимальной гипоспадией и крипторхизмом, госпитализированным в детское уроандрологическое отделение НИИ урологии, проведено дополнительное обследование:
- Определение кариотипа ребенка (ХУ).
- Определение чувствительности к тестостерону (дегидротестостерону).
- УЗИ мочевого пузыря для исключения урогенитального синуса.
- Уретроскопия заднего отдела уретры для оценки области семенного бугорка и синусоскопия (синусография).
Больным с проксимальной гипоспадией в обязательном порядке проводили определение кариотипа (ХY) для подтверждения мужского пола ребенка и дифференциальной диагностики с адреногенитальным синдромом и другими генетически детерминированными заболеваниями. Оценка чувствительности ребенка к тестостерону и дегидротестостерону необходима для исключения пороков развития эндокринной системы (альфа-редуктазная недостаточность). Определение чувствительности к тестостерону мы проверяли путем применения хорионического гонадотропина или мазей, гелей с тестостероном (андрогель, омнадрен, андроктим). Увеличение размеров члена и яичек на фоне гормональной терапии свидетельствовало о положительной реакции и возможности проведения пластической операции. Отсутствие увеличения размеров полового члена при использовании тестостерона и дегидротестостерона свидетельствовало о тяжелой эндокринологической патологии. У таких детей невозможно достигнуть полноценного роста кавернозных тел полового члена в пубертатном периоде и родителям целесообразно максимально рано рассмотреть вопроса об изменении мужского пола на женский.
Кроме того, дети с признаками ложного мужского гермафродитизма (ЛМГ) имеющие двусторонний крипторхизм, гипоплазию яичка, уменьшенный по размеру половой член, могут иметь зачаток матки (урогенитальный синус). Данное образование встречается достаточно редко, у 7-10% детей с проксимальной гипоспадией. Причем в 1-2% случаев оно может достигать больших размеров – от 30 до 200 мл [4, 13]. Поэтому у детей с признаками ЛМГ перед проведением операции для предупреждения интраоперационных и послеоперационных осложнений необходимо исключить наличие урогенитального синуса с помощью выполнения УЗ исследования с наполненным мочевым пузырем и уретроскопии. Выявление объемного жидкостного образования за пузырем или наличие зияющего отверстия в области семенного бугорка указывало на существо-вание урогенитального синуса. Необходимо отметить, что во время операции при кате-теризации уретры у больных с ЛМГ и выраженными размерами урогенитального синуса, катетер постоянно попадает в расширенный урогенитальный синус и сворачивается там. При этом мочевой пузырь оказывается не дренированным. Данная ситуация опасна развитием острой задержки мочи в послеоперационном периоде (если пластика уретры выполняется без проведе-ния разгрузочной эпицистостомии).
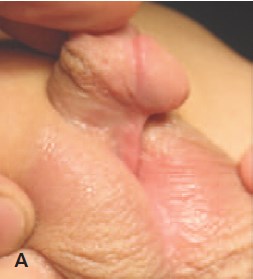
А . Общий вид мошоночной формы проксимальной гипоспадии с деформацией кавернозных тел у ребенка 1 года
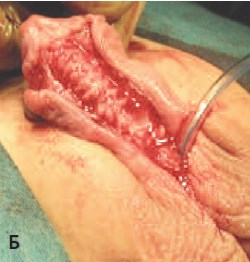
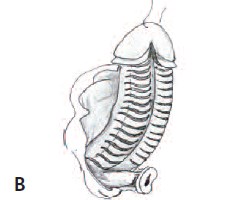
Б. В. Множественные поперечные послабляющие насечки белочной оболочки при коррекции деформации кавернозных тел.
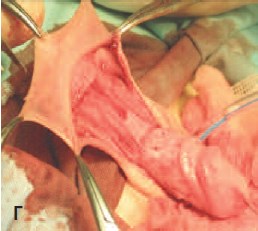
Г. Выкраивание поперечного лоскута крайней плоти на сосудистой ножке
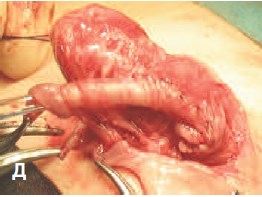
Д. Формирование лоскута крайней плоти в трубку непрерывным и последующим укрепляющим узловым швом
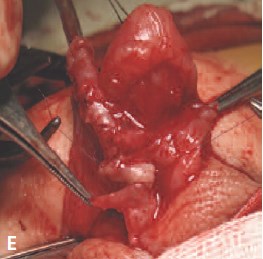
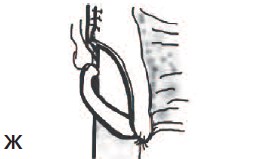
Е. Ж. Формирование анастомоза естественной и артифициальной уретры «бок в бок»
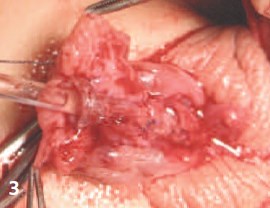
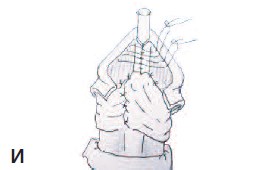
З. И. Мобилизация «крыльев» головки продольными
насечками и поверхностное сшивание крыльев
головки без натяжения
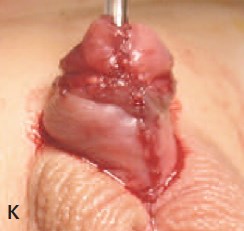
К. Внешний вид головки после мобилизации «крыльев» головки и сшивания вместе
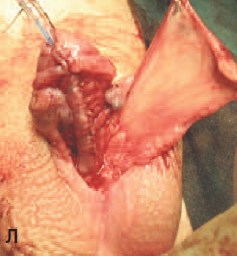
Л. Мобилизация мясистого лоскута мошонки
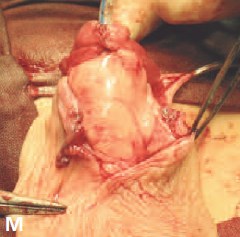
М. Неоуретра укрыта кровоснабжаемым лоскутом мясистой оболочки мошонки
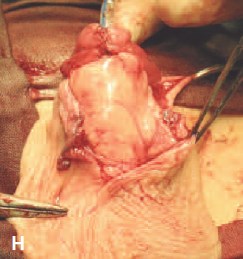
Н. Вид после операции. Мочевой пузырь дренирован пункционной эпицистостомой
Рис. 1. Одномоментная пластика уретры поперечным тубуляризированным лоскутом крайней плоти

А. Мальчик 1 года с пеноскротальной формой проксимальной гипоспадиии и деформацией ствола полового члена
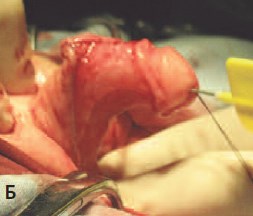
Б. Проба с искусственной эрекцией (деформация кавернозных тел на 650)
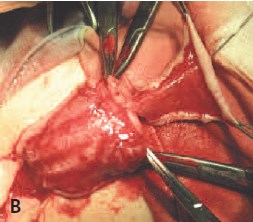
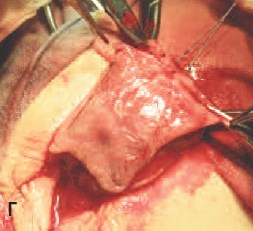
В. Г. Полное расправление кавернозных тел и мобилизация ткани головки (крыльев головки) полового члена, перемещение мясистой оболочки крайней плоти. Заготовка свободного лоскута крайней плоти
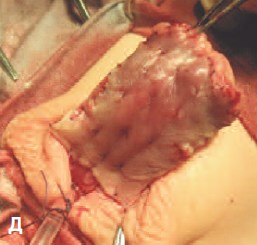
Д. Имплантация и фиксация свободного лоскута крайней плоти по вентральной поверхности полового члена
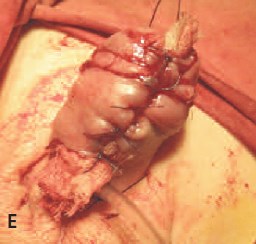
Е. Прижатие лоскута к турунде с левомиколем узловыми швами
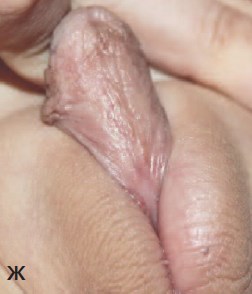
Ж. Результат первого этапа лечения проксимальной гипоспадии. Вид полового члена через 6 мес.
после расправления полового члена и имплантации свободного лоскута крайней плоти
Рис. 2. Методика двухэтапного лечения проксимальной гипоспадии. Первый этап – расправление кавернозных тел и имплантация свободного лоскута крайней плоти
Характеристика больных.
При лечении проксимальной гипоспадии у 125 больных мы использовали одномоментные и этапные методики коррекции порока.
Показанием к проведению одномоментной коррекции было наличие проксимально-стволовой и пеноскротальной гипоспадии с достаточным запасом кожи крайней плоти и с небольшими по длине кавернозными телами. Показанием для этапного метода лечения у первичных больных явилось недоразвитие крайней плоти, когда пластического материала было недостаточно для замещения отсутствующей части уретры.
Противопоказанием для одномоментной коррекции гипоспадии мы считали случаи, когда имелся дефицит пластического материала (недостаток крайней плоти или ее полное отсутсвие (обрезание), повторные операции в анамнезе с дефицитом или выраженными рубцовыми изменениями кожи на стволе полового члена и остаточной деформацией кавернозных тел). В этих случаях использовали этапный метод лечения.
Все больные были условно разделены на две группы.
В первую (группу сравнения) вошли 62 ребенка, оперированные в период с 2008 по 2010 гг. с применением стандартных одномоментной и этапной методик пластики уретры при проксимальной гипоспадии. Одномоментная операция: пластика уретры поперечным тубуляризированным лоскутом крайней плоти ПТЛКП (Duckett) и этапные операции: 1 этап – расправление полового члена; 2, 3 этапы – пластика уретры лоскутом ствола полового члена с укрытием неоуретры в члено-мошоночном анастомозе (Cecile I-II данная операция предусматривала два этапа).
Вторую (основную) группу составили больные (63 человека), оперированные в период с 2010 по 2012 гг. с использованием современных методов лечения проксимальной гипоспадии. Применялись следующие виды пластики: модификация одномоментной пластики уретры поперечным тубуляризированным лоскутом крайней плоти ПТЛКП (Duckett) и 2-х этапная операция (Bracka, Cukcow) коррекции проксимальной гипоспадии [18, 20, 23].
Для качественного улучшения результатов лечения мы внесли изменения в протокол подготовки больных к операции в виде предварительной гормональной терапии у больных с малыми размерами полового члена. Это позволило увеличить размеры полового члена на 20-30% и улучшить кровоснабжение кожи ствола полового члена и крайней плоти (по данным УЗ цветового доплеровского картирования сосудов члена и крайней плоти). Использовали хорионический гонадотропин 5000 МЕ в/м 1 раз в неделю (4 инъекции).
Суть модификации техники операции по Duckett одномоментной коррекции проксимальной гипоспадии поперечным тубуляризированным лоскутом крайней плоти состояла в следующем:
- Выполнение полного расправления кавернозных тел: – устранение сращений кожи ствола полового члена и белочной оболочки по вентральной поверхности; – иссечение соединительнотканной хорды (недоразвитой спонгиозной ткани уретры); – пликация белочной оболочки по дорсальной поверхности; – множественные поперечные послабляющие насечки при наличии дисплазии кавернозных тел по вентральной поверхности (рис.1 Б,В).
- Создание неоуретры из поперечного тубуляризированного лоскута внутреннего листка крайней плоти на сосудистой ножке. На рис. 1 (Г, Д) представлен двухрядный шов неоуретры (непрерывный вворачивающий шов (первый ряд швов) и поддерживающий узловой – второй ряд швов).
- Формирование анастомоза собственной (естественной) уретры с артифициальной в косом направлении (бок в бок), с целью создания более широкого просвета неоуретры (рис.1 Е, Ж).
- Модификация пластики головки полового члена: увеличение длины крыльев головки путем продольных насечек и сшивание крыльев головки поверхностно на глубине 2 мм на коротком протяжении (5-8 мм) верхней половины головки (рис.1 З, И, К).
- Дополнительное укрытие созданной уретры кровоснабжаемым лоскутом мясистой оболочки мошонки (рис.1 Л, М).
- Дополнительное дренирование мочевого пузыря пункционной эпицистостомой (помимо уретрального катетера) (рис. 1 Н).
Двухэтапная методика коррекции проксимальной гипоспадии (операция Bracka, Cukcow [18, 20, 23]) предусматривала на первом этапе устранение деформации кавернозных тел и заготовку лоскута для последующей пластики уретры.
Этот этап операции включал следующие процедуры:
- Пробу с искусственной эрекцией (рис. 2 Б); иссечение соединительнотканных тяжей кожи и кавернозных тел и удаление рубцовой хорды (диспластичной спонгиозной ткани порочной уретры).
- Мобилизацию ткани крыльев головки для увеличения площади головки, выделение мясистой оболочки крайней плоти и перемещение ее в область головки (рис. 2 В).
- Выкраивание свободного прямоугольного лоскута внутреннего листка крайней плоти, отделение его от мясистой оболочки яичка.
- Подшивание свободного лоскута крайней плоти на вентральную поверхность ствола полового члена множественными узловыми швами 7/0 PDS или Monocril (рис. 2 Г, Д).
- Прижатие имплантированного лоскута к кавернозным телам и головке путем сшивания краев раны вокруг турунды с левомиколем (рис. 2 Е).
Снаружи на половой член накладывали циркулярную бинтовую повязку, которую пропитывали глицерином. Через неделю швы снимали, удаляли турунду и начинали обрабатывать имплантированный лоскут сначала левомиколем на протяжении 1 недели, а затем противорубцовыми мазями (контрактубекс, ферменкол, медерма, мадекасол) в течение 2 месяцев.
В случае отсутствия крайней плоти в качестве пластического материала для будущей уретры использовали свободный лоскут слизистой щеки или губы.
Второй этап лечения проксимальной гипоспадии (методом Brackа, Cukcow) выполняли через 6-9 мес. после первого этапа, после стихания признаков рубцевания послеоперационной раны (рис. 2 Ж). Применялась пластика уретры по методу Duplay либо Snodgrass. Выделяли имплантированный лоскут по краю послеоперационного рубца. Формировали лоскут в трубку непрерывным швом PDS или Monocril 6/0. Двумя слоями ушивали послеоперационную рану на стволе полового члена и головке (рис.3 А, Б, В).
Послеоперационные осложнения представлены в таблице 1.
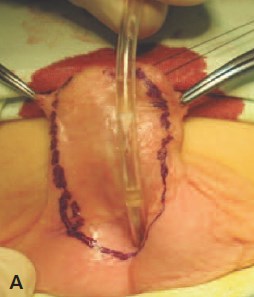
А. Выкраивание лоскута кожи по вентральной поверхности полового члена
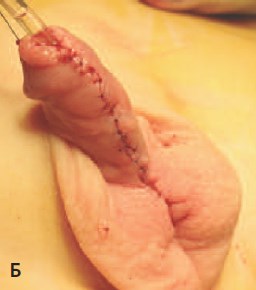
Б. Вид полового члена после операции
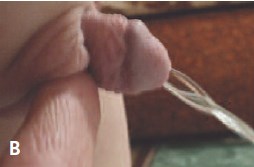
В. Тот же больной через 2 мес. после операции во время акта мочеиспускания
Рис. 3. Методика двухэтапного лечения проксимальной гипоспадии. Второй этап – пластика уретры по Дюплею
Таблица 1. Характер осложнений оперативного лечения проксимальной гипоспадии в зависимости от метода операции
| Метод операции и число больных |
Характер осложнений | ||||||
|---|---|---|---|---|---|---|---|
| Мочевой свищ |
Стеноз анастомоза уретры |
Стеноз наружного отвер. уретры |
Дивертикул неоуретры |
Вторичная деформация полового члена |
ВСЕГО: Число больных |
||
| 1группа сравнения Одномоментная пластика 43 больных. Поперечный тубуляризированный лоскут крайней плоти Duckett |
9 | 3 | 1 | 1 | 1 | 11* (25%) 15осл. (у11б-х) |
62 14* (22%) |
| Этапное лечение 19 б-х 1. Расправление члена 2. Пластика уретры членомошоночный анастомоз Cecile I 3. Разобщение членомошоночного анастомоза Cecile II |
– | – | – | – | – | 3(15%) | |
| 1 | – | – | 1 | 1 | |||
| – | – | – | – | – | |||
| 2группа основная Одномоментная пластика 43.б-х Поперечный тубуляризированный лоскут крайн |
5 | 1 | – | – | – | 6 (14 %) |
63 7 (11%) |
| Этапное лечение 20 б-х 1. Расправление члена и имплантация лоскута Bracka 2. Пластика уретры Duplay, Snodgrass |
– | – | – | – | – | 1 (5%) | |
| 1 | – | – | – | – | |||
| ИТОГО: 125 | 15 | 4 | – | 2 | 2 | 25 осл. у21*б-х (11,7%) |
125 |
*Один больной имел несколько осложнений (дивертикул уретры и стеноз уретры и др.)
Как видно из таблицы, большее число осложнений наблюдали при одномоментной коррекции гипоспадии, что вполне объяснимо сложной техникой операции при наличии дефицита пластического материала, а также нарушениями микроциркуляции перемещенного лоскута крайней плоти из которого формировалась уретра, и трудностями адекватного дренирования мочевого пузыря у детей младшего возраста.
Наиболее часто наблюдали осложнения в виде свища уретры (15 больных). Повторные операции, по коррекции данного осложнения, были успешны. Стеноз анастомоза выявлен у 4 больных. Сужение зоны анастомоза удалось устранить путем рассечения этой зоны и продленной катетеризации уретральными стентами (1мес.).
Для профилактики вторичной деформации полового члена в послеоперационном периоде на протяжении 2 мес. рубцы смазывали противорубцовыми кремами 2 раза в сутки утром и вечером (контрактубекс, ферменкол, медерма.) На ночной период времени половой член фиксировали к передней брюшной стенке пластырем. Данные мероприятия в сочетании с радикальным устранением деформации во время операции позволили сократить до минимума возникновение вторичного искривления кавернозных тел.
Отдаленные результаты прослежены в сроки от 6 мес до 5 лет у 105 больных. Хорошие результаты в виде нормальных показателей урофлоуметрии, отсутствия остаточной деформации кавернозных тел при хорошем косметическом результате наблюдали у 89 больных (84%): 39 детей первой группы (сравнительной) и 50 – второй (основной) группы. Удовлетворительные результаты в виде умеренного снижения потока мочи наблюдали у 16 больных (15%). Из них 9 детей было после одномоментной операции и 3 – после этапной операции – из первой (контрольной) группы. Во второй (основной) группе было 4 ребенка с удовлетворительным результатом после одномоментной операции. Неудовлетворительных отдаленных результатов в этой группе больных не было, поскольку все осложнения, возникающие в ближайшем послеоперационном периоде, устранялись повторными операциями.
ОБСУЖДЕНИЕ
В литературе, посвященной коррекции проксимальной гипоспадии, можно часто встретить противопоставление одномоментных и этапных методик лечения [1, 2, 5, 6, 12, 13, 16, 18, 23]. Известны преимущества одномоментных операций в виде уменьшения числа оперативных вмешательств и недостатки – в сложности методик и проблем обеспечения хорошего кровообращения перемещенных препуциальных лоскутов, из которых создается неоуретра. Этапные методики позволяют обеспечить более надежный косметический и функциональный результат за счет увеличения числа операций. Вполне понятно желание хирургов унифицировать и упростить операции при сложных формах гипоспадии, чтобы сократить до минимума число осложнений. Этапный метод лечения проксимальной гипоспадии целесообразно использовать начинающим специалистам, у которых нет достаточного опыта лечения больных со сложными формами гипоспадии. Однако можно встретить исследования, когда двухэтапные методики применяются при средне-стволовых и дистальных формах гипоспадии без искривления кавернозных тел [9,19]. По нашему мнению, применение двухэтапных операции при дистальной гипоспадии оправдано только при коррекции осложненных случаев гипоспадии и при отсутствии запаса пластического материала. При лечении первичных больных с дистальной гипоспадией целесообразно использовать одномоментные широко известные варианты пластики уретры (TIP (Snodgrass), Mathieu, GTIP и др.). По показаниям можно использовать одномоментные операции и при коррекции проксимальной гипоспадии. Минимум осложнений можно получить, если использовать одномоментную пластику уретры поперечным тубуляризированным лоскутом крайней плоти (ПТЛКП) у детей с проксимальной стволовой и мошоночной формой, и с хорошим запасом тканей крайней плоти при проведении первичных операций
Коррекция гипоспадии в настоящее время проводится в раннем возрасте. Большинство специалистов рекомендуют выполнять операцию в возрасте 1 года. Отдаленный послеоперационный период длительное время может протекать без особенностей. Однако, у ряда детей в пубертатном периоде (12-15лет) могут возникать изменения, которые требуют обследования, а иногда и коррекции. В период бурного полового развития и быстрого увеличения размеров кавернозных тел и уретры возможно появление вторичной деформации полового члена или умеренной стриктуры уретры в области анастомоза собственной уретры с искусственно созданной. Возможно образование камней на волосах в просвете неоуретры у детей, которым мочеиспускательный канал создавали из кожного лоскута мошонки. Поэтому мы считаем необходимым прохождение профилактического осмотра мальчиков с проксимальной гипоспадией, в переходном возрасте (12-15 лет). Постоянный контроль детскими урологами отдаленных результатов лечения больных с гипоспадией, особенно с проксимальными формами, спустя 10-15 лет после операции позволит предупредить возникновение осложнений в отдаленные сроки и устранить их, если таковые имеются, до перехода ребенка во взрослую поликлиническую сеть.
ВЫВОДЫ
1. Дифференцированный подход позволяет выбрать оптимальный метод лечения проксимальной гипоспадии в зависимости от сложности проявлений порока.
2.Одноэтапный метод лечения показан при более простых формах проксимальной гипоспадии (среднестволовой и пеноскротальной), а двухэтапный – при сложных ее формах (мошоночной и промежностной) в сочетании с грубой деформацией кавернозных тел.
3. Дети с признаками ложного мужского гермафродитизма (микрофаллосом и двусторонним крипторхизмом) помимо кариотипирования требуют определения чувствительности к тестостерону и дегидротестостерону, а также нуждаются в консультации эндокринолога и проведении дополнительных обследований (УЗИ, уретроскопии и уретрографии) для исключения урогенитального синуса.
4. Предложенные изменения в протоколе лечения больных с проксимальной гипоспадией в виде предоперационной гормональной подготовки и модификации одномоментной пластики уретры, позволили уменьшить число осложнений с 25% до 14%.
5. Двухэтапная методика пластики уретры по Bracka обеспечивает создание достаточного запаса тканей для более надежной коррекции сложных форм проксимальной гипоспадии с минимальным числом операций, хорошими косметическими и функциональными отдаленными результатами. Число осложнений этапных операций удалось снизить с 15 % до 5%.
ЛИТЕРАТУРА
1. Ашкрафт К.У., Холдер Т.М. Детская хирургия. Практическое руководство Лечение гипоспадии. С-Пб.,1999. С. 35-37.
2. Лопаткин Н.А., Пугачев А.Г. Детская урология. Руководство. М.: Медици-на, 1986. С. 217-235.
3. Урология. Национальное руководство. [Под ред. Н.А.Лопаткина]. М.: ГЭОТАР – Медиа, 2009. С. 307-340.
4. Ashcraft Keith W. Pediatric urology. Philadelphia: Saunders Company,1990. 552 p.
5. Smith ED. Hypospadias. // Ashcraft Keith W. Pediatric Urology. Philadelphia: Sunders Company 1990. Р. 353-395.
6. Hypospadias surgery. [eds. Hadidi AT, Azmy AF]. Springer, 2004. 335 p.
7. Савченко Н.Е. Гипоспадия и её лечение. Минск: 1962. С. 98-129.
8. Савченко Н.Е. Гипоспадия и гермафродитизм. Минск: 1974. С. 123 -191.
9. Русаков В.И. Лечение гипоспадии. Ростов на Дону: 1998. С. 108-112.
10. Продеус П.П., Староверов О.В. Гипоспадия. М.: 2003. С. 77-78.
11. Файзулин А.К. Современные аспекты хирургического лечения гипоспадии у детей: Дис. … д-ра мед. наук. М., 2002. 241 с.
12. Файзулин А.К. Одноэтапная коррекция гипоспадии у детей: Автореф. … дис. канд. мед. наук. М., 1995. 12 с.
13. Рудин Ю.Э. Реконструктивно-пластические операции при лечении гипоспадии в детском возрасте: Дис. … д-ра мед. наук. М., 2003. 328 с.
14. Рудин Ю.Э. Способ одномоментной коррекции проксимальной гипоспадии деэпителизированным лоскутом крайней плоти. // Урология. 2002. N 5. С. 58-63.
15. Hodgson NB. A one-stage hypospadias repair. // J Urol. 1970. Vol. 104, N2. Р. 281-283.
16. Djordjevic ML, Majstorovic M, Stanojevic D, Bizic M, Ducic S, Kojovic V, Vukadinovic V, Korac G, Perovic S. One-stage repair of severe hypospadias using combined buccal mucosa graft and longitudinal dorsal skin flap. // Eur J Pediatr Surg. 2008. Vol. 18б N 6. Р. 427-430.
17. Aoki K, Fujimoto K, Yoshida K, Hirao Y, Ueoka K. One-stage repair of severe hypospadias using modified tubularized transverse preputial island flap with V-incision suture. //J Pediatric Urol. 2008. N 12. Р. 439.
18. Bracka A. Hypospadias repair: the two stage alternative. // Br J Urol. 1995. Vol. 147. Р. 1057.
19. Суходольский А.А. Оценка эффективности двухэтапной коррекции гипоспадии у мальчиков с использованием свободного кожного лоскута крайней плоти: Автореф. … дис. канд. мед. наук. М., 2011. С. 36-39.
20. Bracka A. The role of two-stage repair in modern hypospadiology. // J Urol. 2008. N 4. Р. 210-218.
21. Altarac S, Papeš D, Bracka A. Two-stage hypospadias repair with inner preputial layer Wolfe graft (Aivar Bracka repair). // BJU Int. 2012. N 8. Р. 460-73.
22. Tan YW, Patel N, Scarlett A, Clibbon J, Kulkarni M, Mathur A. Bracka's staged repair of proximal hypospadias-revisiting a versatile technique. // J. Pediatr Urol. 2012. N 2. Р.108.
23. Nitkunan T, Johal N, O'Malley K, Cuckow P. Secondary hypospadias repair in two stages. // J. Pediatr Urol. 2006. N 12. Р.559-563.
24. Рудин Ю.Э., Марухненко Д.В., Гарманова Т.Н., Сайедов К.М. Новый метод пластики головки полового члена у пациентов с гипоспадией. // Экспериментальная и клиническая урология. 2013. N 1. С. 87-89.










Комментарии