О.А. Каплунова
ФГБОУ ВО «Ростовский государственный медицинский университет» МЗ РФ; Ростов-на-Дону, Россия
Диссертация приват-доцента оперативной хирургии и топографической анатомии Императорского Казанского Университета Василия Захаровича Голубева (1894) «О кровеносных сосудах в почках млекопитающих и человека» [1] была выполнена в гистологической лаборатории под руководством К.А. Арнштейна. Этот фундаментальный труд содержал наиболее полное и достоверное изложение закономерностей распределения тончайших кровеносных сосудов в корковом и мозговом веществе почки и их взаимосвязях. Исследование В.З. Голубева послужило дальнейшему развитию учения о микроангиоархитектонике почек и их потенциальных ресурсах
Прежде всего, В.З. Голубев расшифровал строение двух капиллярных сетей в корковом веществе почек: гломерулярной и перитубулярной. Гломерулярные сети образуют приносящие клубочковые артериолы, ответвляющиеся от междольковых артерий. От последних ответвляются и боковые веточки без сосудистых клубочков, формирующие перитубулярную капиллярную сеть коркового вещества. От дуговых или междольковых артерий начинаются внутренние перфорирующие артерии, которые имеют мало клубочков или их совсем их не имеют, и направляют кровь по кратчайшему пути от дуговых артерий к сосудистой сети фиброзной или жировой капсулы. Эти данные подтверждаются современными исследованиями с помощью микрокомпьютерной томографии [2].
Мозговое вещество почки кровоснабжается истинными и ложными прямыми артериолами. В.З. Голубев показал, что истинные прямые артериолы отходят непосредственно от дуговых артерий или от проксимальных частей междольковых артерий, а от выносящих артериол юкстамедуллярных клубочков начинаются ложные прямые артериолы. Проникнув в мозговое вещество, прямые артериолы образуют сосудистые пучки, которые спускаются к сосочку почки и разветвляются на капилляры, оплетающие мочевые канальцы. В составе прямых сосудов мозгового вещества В.З. Голубев выявил истинные прямые артериолы, ложные прямые артериолы и прямые венулы пирамид.
Особой новизной характеризуются данные В.З. Голубева о «новых чудесных сетях» – клубочковых капиллярных образованиях, расположенных по ходу дугообразных артерий в пограничном слое почки. В отличие от клубочков почечных телец, они не окружены капсулами, а их приносящие и выносящие артериолы расположены на противоположных полюсах. В.З. Голубев отнес эти образования к околососудистому руслу. В пограничной (юкстамедуллярной) зоне почки «новые чудесные сети» соединяют сосуды коркового и мозгового вещества, и регулируют почечный кровоток. В.З. Голубев писал: «Представляя запасный кровяной резервуар, чудесная сеть может игрой мышц, заложенных в стенках ее ветвей и приводящего и отводящего ствола, двинуть кровь вперед или задержать ее на месте, смотря по обстоятельствам, или же окольным боковым путем направить ее в ближайший район и тем до известной степени устранить вред нарушенного кровообращения».
Большое значение в механизме гемоциркуляции в почке В.З. Голубев отводил истинным прямым артериолам, которые «помимо своего физиологического значения, могут быть регуляторами кровообращения, будучи снабжены чудными сетями».
Данные В.З. Голубева о сосудистых анастомозах кортикомедуллярной (юкстамедуллярной) зоны почки, прямых артериолах мозгового вещества и его гениальное предположение об их физиологическом значении в регуляции внутрипочечного кровообращения были подтверждены экспериментальными работами J. Trueta et. al. [3]. Авторы установили, что юкстамедуллярные клубочки, прямые сосуды и связанные с ними сосудистые элементы составляют мозговой шунт, через который кровь, оттекая из коркового вещества, идет от почечных артерий к почечным венам. К юкстамедуллярному шунту, по мнению авторов, относятся: проксимальная часть междольковых артерий, первые ветви междольковых артерий, приносящие и выносящие сосуды юкстамедуллярных клубочков и сами клубочки, прямые артериолы в мозговом веществе, петли прямых артериол, межканальцевые капилляры, формирующие часть системы прямых артериол, прямые венулы, проксимальная часть междольковых вен.
В обычных условиях по юкстамедуллярному шунту проходит всего 20% почечной крови. При волнениях, тяжёлой физической нагрузке и особенно при патологических состояниях (кардиогенный или другой шок) большая часть крови (до 80%) сбрасывается по мозговым сосудам. Значительное усиление и продолжительность шунтирования приводят к тяжёлым нарушениям кровоснабжения поверхностных слоёв коркового вещества почки и острой почечной недостаточности [4].
В регуляции почечного кровообращения участвуют приспособительные образования в крупных артериях, которые выступают в просвет сосудов [5, 6, 7].
Особенность почечного кровообращения обусловлена способностью к ауторегуляции, в результате которой происходит внутрипочечное перераспределение кровотока: уменьшение его в поверхностных и увеличение в глубоких слоях почки [8]. Ауторегуляция почечного кровотока совершенна, многокомпонентна и основана на функционировании механизма «плотное пятно - скорость клубочковой фильтрации». В регуляции клубочкового кровотока принимают участие ренин-ангиотензин-альдостероновая и калликреин-кинин-простагландиновая системы, нервная система и предсердный натрийуретический фактор. В результате работы такой многофакторной системы, даже значительные колебания артериального давления не оказывают заметного влияния на почечный кровоток.
Почки принимают участие в регуляции системного артериального давления и как эндокринный орган [9, 10]. Одни почечные гормоны обладают сосудосуживающим (вазопрессорные системы), другие сосудорасширяющим действием (вазодепрессорные системы). Характерная особенность указанных систем состоит в том, что они действуют не только на отдельные органы-мишени, но и непосредственно на почку (местные или тканевые регуляторы). Юкстагломерулярный аппарат, секретирующий ренин, и интерстициальные клетки мозгового вещества, вырабатывающие простагландины, тесно взаимодействуют в регуляции почечного кровотока, распределяя его между корковым и мозговым веществом [10].
Наиболее универсальной реакцией сосудов коркового вещества почки является вазоконстрикция [4]. Она наблюдается при ортостазе, эмоциональном напряжении, физической нагрузке, гипоксии и т. д. Подвержены вазоконстрикции и приносящие сосуды клубочков. Кровоток в мозговом веществе почек при этом увеличивается [10]. Поскольку продукция депрессорных веществ (простагландинов) находится в прямой зависимости от уровнямедуллярного кровотока, то эту реакцию можно рассматривать как один из важных факторов, препятствующих чрезмерной вазоконстрикции сосуд, и стабилизации повышенного артериального давления [8]. Наблюдаемый при большинстве воздействий спазм сосудов коркового вещества почек имеет приспособительное адаптационное значение, которое заключается в ликвидации реально существующей или предупреждение ожидаемой гиповолемии и гипотонии. При этом в почках сброс основной массы крови происходит по шунту J. Trueta. Однако, эта реакция не всегда целесообразна, так как при ее многократном повторении развивается кортикальный некроз. Почки, как бы жертвуя собственным кровообращением, сохраняют условия для кровоснабжения других органов, нормализуя общее кровообращение [4].
При сердечно-сосудистых и почечных заболеваниях, как правило, возникает нефросклероз [11, 12]. На определенном этапе морфогенеза нефросклероза любой этиологии происходит формирование блока почечного кровотока, который может локализоваться на уровне разных структур почки: клубочков - при хроническом гломерулонефрите и амилоидозе, приносящих артериол – при артериальной гипертензии, перитубулярных капилляров - при хроническом нефрите. Блок кровотока вне зависимости от его локализации влечет за собой развитие гипоксического диффузного склероза стромы и атрофии структур нефрона.
Отсутствие эффективной регуляции в почках мозгового кровотока при артериальной гипертензии способствует транссудации и развитию гиалиноза стромы мозгового вещества [13]. При склерозе мозгового вещества почек наблюдается редукция и блок юкстамедуллярного шунта [14], что, в свою очередь, потенцирует повреждающее действие артериальной гипертензии на структуры коркового вещества в связи с усилением гемодинамической нагрузки [12].
Наши исследования [7] показали, что архитектоника сосудов микроциркуляторного русла почек при сердечно-сосудистых заболеваниях характеризуется уменьшением диаметров сосудистых клубочков, уменьшением клубочковой массы в корковом веществе и общего количества клубочков в почке. Наблюдаются также запустение и деформация перитубулярных капилляров, расширение и деформация прямых артериол мозгового вещества. Наиболее выражены указанные изменения при вазоренальной гипертензии, сочетании гипертонической болезни с хронической ишемической болезнью сердца и при гипертонической болезни по сравнению с ишемической болезнью сердца и атеросклерозом брюшной аорты.
Необходимо отметить, что при изученных сердечно-сосудистых заболеваниях адаптивные процессы в сосудах интраорганного артериального русла почек связаны с уменьшением относительного содержания артериальных сосудов в корковом и увеличением их в мозговом веществе почек, уменьшением диаметров сосудистых клубочков субкапсулярных и интракортикальных почечных телец и увеличением юкстамедуллярных клубочков. Увеличивается также диаметр прямых артериол мозгового вещества. Указанные изменения в интраорганных артериальных сосудах почек особенно выражены при острой ишемической болезни сердца и гипертонической болезни, и свидетельствует об усилении юкстамедуллярного шунтирования (рис.1-б, 2-б, 3). При хронических сердечно-сосудистых заболеваниях (хроническая ишемическая болезнь сердца, гипертонической болезнь в сочетании с хронической ишемической болезнью сердца), когда имеет место длительное воздействие изменившихся условий гемоциркуляции, были обнаружены изменения в микроциркуляторном русле почек по типу чрезмерного полнокровия, - проявление долговременной адаптации (рис. 4). При склеротических и деструктивных изменениях в интраорганном артериальном русле почек значительно уменьшается относительное содержание артериальных сосудов во всех зонах почек, что, очевидно, связано с отсутствием и юкстамедуллярного шунтирования и чрезмерного полнокровия и указывает на срыв процессов адаптации (рис. 1-в, 5.) [15].
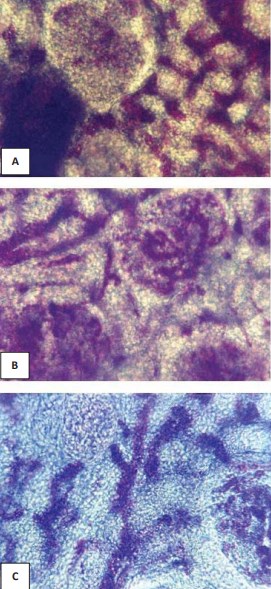
Рисунок 1. Артериальные сосуды в средней зоне коркового вещества: A – в почке мужчины 37 лет, контрольная группа; B – спавшиеся перитубулярные капилляры в почке мужчины 68 лет, хроническая ишемическая болезнь сердца; C – склерозированные и деформированные клубочки и сосуды в почке женщины 71 года, вазоренальная гипертензия (атеросклероз почечной артерии). Окраска эритрозином по Г.В.Ковалевскому. Об.15, ок. 7.
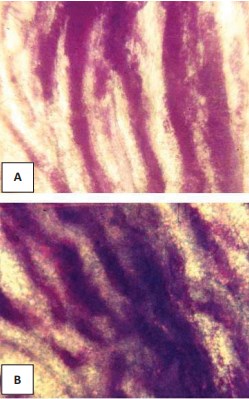
Рисунок 2. Артериальные сосуды мозгового вещества: A – в почке мужчины 23 лет, контрольная группа; B - расширение и переполнение кровью прямых артериол в почке мужчины 49 лет, острая ишемическая болезнь сердца. Окраска эритрозином по Г.В. Ковалевскому. Об.15, ок. 7.
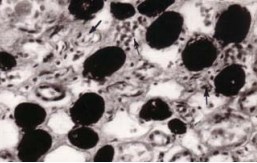
Рисунок 3. Расширенные прямые артериолы, просветы которых заполнены черной тушью, и венулы с форменными элементами крови (показаны стрелками) в мозговом веществе почки мужчины 58 лет. Хроническая ишемическая болезнь сердца. Инъекция сосудов черной тушью. Окраска по Вейгерту. Об. 40, ок. 10.
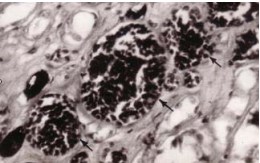
Рисунок 4. Прямые артериолы, просветы которых заполнены черной тушью, и расширенные венулы с форменными элементами крови (показаны стрелками) в мозговом веществе почки мужчины 41 года. Гипертоническая болезнь 2-й стадии. Инъекция сосудов черной тушью. Окраска по Вейгерту. Об. 40, ок. 10.
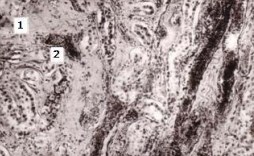
Рисунок 5. Участок мозгового вещества почки женщины 71 года с хронической ишемической болезнью сердца, вторичной гипертензией, атеросклерозом брюшной аорты. Очаги склероза мозгового вещества (1) и деформация прямых артериол (2). Окраска по ван Гизон. Об. 16, ок.10.
Итак, при острых сердечно-сосудистых заболеваниях возрастает значение юкстамедуллярного пути кровотока, наблюдается юкстамедуллярное шунтирование. При хронических сердечно-сосудистых заболеваниях вначале усиливается юкстамедуллярное шунтирование, а на поздних стадиях заболевания склероз мозгового вещества почек вызывает редукцию и блок юкстамедуллярного пути кровотока, ухудшается как юкстамедуллярный, так и кортикальный путь кровотока, что приводит к срыву адаптации интраорганного артериального русла почек.
На основании полученных данных, мы установили закономерность, связанную с процессом адаптации интраорганного артериального русла почек как к возрастным изменениям гемоциркуляции, так и при изученных сердечно-сосудистых заболеваниях. Необходимо отметить, что в этом процессе участвуют одни и те же морфологические структуры - средняя оболочка и эластические мембраны интраорганных артерий, мышечно-эластические подушки в местах ответвления артерий и приносящих артериол клубочков интракортикальных и юкстамедуллярных почечных телец, а также изменяющиеся диаметры приносящих и выносящих артериол сосудистых клубочков различных зон коркового вещества почек. Для каждой возрастной группы и при каждом изученном заболевании степень изменения указанных структур влияет на зональное перераспределение кровотока в почках [16].
Современные сведения о путях почечной гемоциркуляции, подготовленные исследованиями В.З. Голубева, позволяют объяснить механизм развития различных патологических состояний: острой кровопотери [17], гидронефроза [18], вазоренальной гипертензии, гломерулонефрита, пиелонефрита [8], нефроурологических заболеваниях [19], кардиогенного шока [20, 21], мочекаменной болезни [22], кардиоренального синдрома при острой ишемической болезни сердца [23], артериальной гипертензии [7, 24, 25], внезапной коронарной смерти [26] и др. Таким образом, В.З. Голубев создал научную основу для изучения микроангиоархитектоники почек. Принципы, изложенные в его диссертации, предвосхитили появление работ, изучающих юкстамедуллярный кровоток и почечную гемомикроциркуляцию в норме и при патологии.
Литература
- Голубев В.З. О кровеносных сосудах в почке млекопитающих и человека. Дисс. Казань; 1894: 110.
- Marsh DJ, Postnov DD, Rowland DJ, Wexler AS, Sosnovtseva OV, Holstein-Rathlou NH. Architecture of the rat nephronarterial network: Analysis with micro-computed tomography. Am J Physiol Renal Physiol. 2017;313(2):F351-F360. DOI: 10.1152/ajprenal.00092.2017
- Trueta J, Barclay AE, Daniel P.N., et al. Studies of the renal circulaƟ on. Oxford: Charles Thomas, Springfi ld; 1947.
- Сучков В.В. Корковое и мозговое кровообращение почек при прессорных и депрессорных синокаротидных рефлексах. Кардиология. 1984;24(6):24-28.
- Алексеевских Ю.Г. К некоторым гистологическим особенностям строения артерий и вен почек у человека. Арх. патол. 1969;31(6):42-45.
- Макаренко Н.Ю. Возрастные особенности внутриорганных сосудов почки, факторы, их определяющие. Фундаментальные науки – медицине и здравоохранению. 1989;1:87-88.
- Каплунова О.А. Кровеносные сосуды почек. Ростов-наДону: Наука-Спектр; 2008.
- Серов В.В. Почки и артериальная гипертензия. М.: Медицина; 1993.
- Шхвацабая И.К., Некрасова А.А., Устинова С.Е. и др. Прессорные и депрессорные гуморальные системы при гипертонической болезни, протекающей с лабильным и стабильным повышением артериального давления. Артериальные гипертензии. М.: Медицина; 1980.
- Серов В.В., Варшавский Л.А., Куприянова Л.А. Иммунопатология почек. М.: Медицина; 1983.
- Серов В.В., Яргин С.В. Морфо- и патогенез нефросклероза: клинико-морфологический анализ. Терапевтический архив. 1986;58(8):4-9.
- Яргин С.В. Нозологические особенности морфогенеза нефросклероза. Архив патологии. 1986;7:55-63.
- Постнов Ю.В. Почка при хронической артериальной гипертонии, и «переключение» и роль почечной медуллы в его развитии. Кардиология. 1979;21(12):30-38.
- Кротовский Г.С., Пальцев М.А., Покровский А.В. и др. Математическое моделирование выраженности нефроангиосклероза при вазоренальной гипертензии. Хирургия. 1989; 6:23-27.
- Каплунова О.А. Морфофункциональная характеристика интраорганных артериальных сосудов почек в норме и при некоторых сердечно-сосудистых заболеваниях. Журнал фундаментальной медицины и биологии. 2014;2:25-29.
- Каплунова О.А. Морфологические аспекты возрастной адаптации артериальных сосудов почек человека при некоторых сердечно-сосудистых заболеваниях. Медицинский вестник Юга России. 2014; 2: 65-70.
- Воробьев А.И., Городецкий В.М., Шулутко Е.М. и др. Острая массивная кровопотеря. М.: ГЭОТАР-Медиа; 2001.
- Асфандияров Ф.Р., Абдулхакимов Э.Р. Микроциркуляторное русло почек при гидронефрозе по данным лазерной допплеровской интраоперационной флоуметрии и морфологического исследования. Вестник Волгоградского гос. мед. университета. 2009;3(31):32-34.
- Ольхова Е.Б. Интраренальное артериовенозное шунтирование у детей. Ультразвуковая и функциональная диагностика. 2004;2:67-77.
- Барбараш Л.С., Попков А.Н., Херасков В.Ю., Плотников Г.П., Шукевич Д.Л., Григорьев Е.В. Эффективность заместительной почечной терапии при кардиогенном шоке, осложненном полиорганной недостаточностью. Общая реаниматология. 2011;7(5):32. DOI: 10.15360/1813- 9779-2011-5-32
- Van den Akker JPC, Bakker J, Groeneveld ABJ, den Uil CA4. Risk indicators for acute kidney injury in cardiogenic shock. J Crit Care. 2019;50:11-16. DOI: 10.1016/j.jcrc.2018.11.004
- Асфандияров Ф.Р. Структурные преобразования системы почечной артерии на этапах пренатального онтогенеза, старения и патологических состояний. Автореф… докт дисс. Саратов; 2011: 42.
- Мухин Н.А., Моисеев В.С., Кобалава Ж.Д. Кардиоренальные взаимодействия: клиническое значение в патогенезе заболеваний сердечно-сосудистой системы и почек. Тер. Архив. 2004;6:5-10.
- Гогин Е.Е. Гипертоническая болезнь: основы патогенеза, диагностика и выбор лечения. Consilium medicum. 2004;6(5):324-330.
- Ruiz-Hurtado G, Ruilope LM. Microvascular injury and the kidney in hypertension. Hipertens Riesgo Vasc. 2018;35(1):24-29. DOI: 10.1016/j.hipert.2017.03.002
- Соколова Р.И., Волков В.И., Вихерт А.М. и др. Особенности микроциркуляции в почках при внезапной сердечной смерти. Архив патологии. 1986; 48 (8): 44-49.
Статья опубликована в журнале "Вестник урологии" № 1 2019, стр. 45-52










Комментарии